张子豪 李博瑶
(沈阳建筑大学市政与环境工程学院,辽宁沈阳 110168)
地下水是我国城镇和工矿企业的重要水源。然而我国许多地区的地下水源,尤其是东北地区和华北地区的主要城市和农村的地下水源中普遍存在铁、锰含量超标的现象,对居民的日常生活和工农业生产等均造成不利影响。自20世纪70年代以来,曝气接触氧化法便被广泛应用于国内的地下水除铁除锰工程中,该工艺流程主要是含铁锰地下水曝气后经滤池过滤,水中Mn2+,Fe2+在滤池中被氧化为高价的氢氧化物,并逐渐附着在滤料的表面上形成活性滤膜[1]。接触氧化除铁锰的理论认为铁锰氧化去除的关键不是滤料本身,而是附着在滤料表面的铁质及锰质活性滤膜的自催化氧化作用[2],水中 Mn2+,Fe2+被滤膜吸附氧化,又生成新的活性滤膜物质参与反应,形成这样一个自催化反应过程。同时,由于不同滤料在成分和性能上的差别,从而产生不同的除铁除锰效果[3]。多年工程实践表明,接触氧化法中铁质活性滤膜对铁的去除非常有效,其中铁离子的去除过程主要是化学氧化作用,Fe2+很容易被氧化形成Fe(OH)3被滤料截留吸附,但在除锰方面一直没有得到很好的解决[1,2]。受水质及环境因素的影响,Mn2+难以快速氧化为MnO2形成锰质活性滤膜,使得形成周期比较长,滤料成熟慢,且由于经常性反冲洗等外界因素的干扰,锰质滤膜有时根本不能形成,除锰效果更是呈现很不稳定的状态[4]。因此,为了保证合格的出水水质,对于锰砂吸附过滤能力的探究和对氧化除锰工艺的改进尤为重要。本文以辽宁省新民市柳河沿岸农村地下水为例,结合当地水文地质情况,采用二级曝气加单级过滤除锰的处理工艺去除水中超标锰,并探究不同锰砂滤料的除锰能力,分析该工艺的除锰效果,为新民市农村地下水除锰工程的实际运行提供可借鉴的科学依据。
1 地下水除锰工艺设计
1.1 设计实际工艺流程
由前期取水试验可知,新民市柳河沿岸农村地下水锰含量为1.44 mg/L ~2.26 mg/L,平均值为 1.85 mg/L,属低含锰量水质,且用水规模较小,拟设计小型地下水除锰构筑物,其地下水除锰工艺流程如下:

除铁、除锰滤池的曝气方式上,考虑到氧化的需要溶解氧量和建造费用经济合理的要求,本工艺选择二级跌水曝气法,既避免了自然空气接触氧化法氧化物不易过滤的弊端,又弥补了出水不稳定的不足[5]。且由于该水源地下水中锰离子较铁离子更难去除,因此,可采用二级曝气加单级过滤除锰的处理工艺[6]。
1.2 确定实验工艺流程
为检验该工艺处理效果,以便在后期对工艺进行优化和改进,笔者通过三个月的相关动态实验,模拟实际运行条件,用曝气塔保证曝气效果,采取“二级跌水曝气+一级过滤”的工艺方式进行试验研究,其实验工艺流程为:含锰地下水→曝气塔→滤柱→出水。在运行过程中冲洗时间不宜过长,以免滤料表面活性滤膜脱落过多,影响除锰效果。本实验冲洗历时为7 min~10 min。除锰滤池滤速不宜过高,一般可控制在5 m/h~7 m/h。原水经过一、二级曝气后,水中pH,DO值都会有不同的变化。溶解氧值在1.65 mg/L ~6.82 mg/L 之间变化,平均值为 4.05 mg/L,pH 值在6.94 ~7.32 之间变化,平均值为 6.97。
2 地下水除锰效果实验
2.1 实验目的
通过对比不同性能的滤料,掌握其成熟期,了解其滤后水含锰量峰值及测量值变化,分析其除锰效果,从而对工艺进行优化设计。
2.2 实验材料与装置
1)实验材料。原水水质见表1。滤料:选取2种不同品质的锰砂及活化沸石作为滤料,分别命名为甲、乙、丙,其中甲柱为河南巩义天然锰砂,乙柱为锦西天然锰砂,丙柱为活化沸石。2)试验装置。采用直径100 mm,高2 m的玻璃滤柱。每根滤柱各10个取样口。滤料规格及填料厚度如表2及表3所示。

表1 原水水质情况

表2 滤层滤料规格
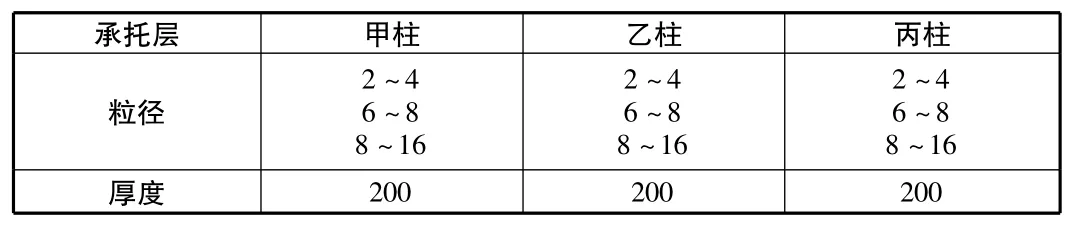
表3 承托层滤料规格 mm
2.3 实验方法
实验滤柱进水中溶解氧DO和pH值的改变,通过放置在净水车间地面上及用铁架支起的水箱在不同跌水高度上曝气的方法来实现。
原水经过装有天然锰砂的滤柱过滤后,水中Mn2+应被去除或含量降低。实验采取定量分析法来进行,即对同一滤柱控制不同的滤速,然后测定滤后水中的锰离子含量。将不同的滤料分装在三组滤柱中。原水经过一、二级跌水曝气后,进入装有滤料的滤柱进行过滤,在不同时间内测定其滤后水中锰离子的含量,其中锰离子采用过硫酸铵分光光度法来检测。
2.4 实验结果分析
本实验通过检测滤柱滤后锰离子浓度不同时刻的数值,绘制了不同滤柱滤后锰离子浓度的历时变化曲线,见图1~图3。通过锰离子浓度变化曲线可以分析其成熟期,本文以滤后锰离子浓度下降到0.1 mg/L时的时间为锰砂滤料的成熟期。
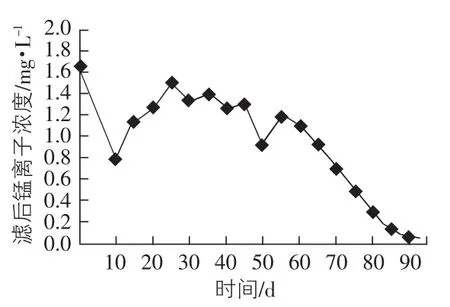
图1 甲柱滤后锰离子浓度历时变化曲线
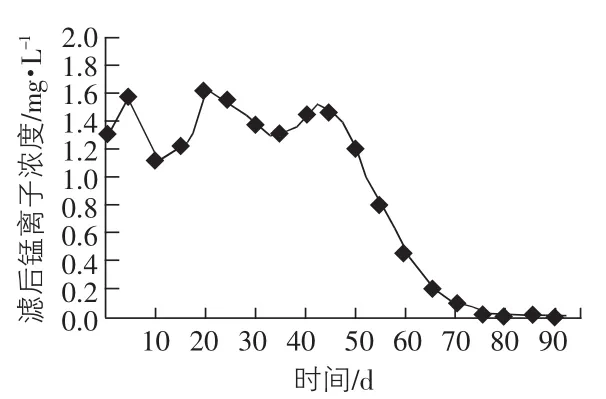
图2 乙柱滤后锰离子浓度历时变化曲线
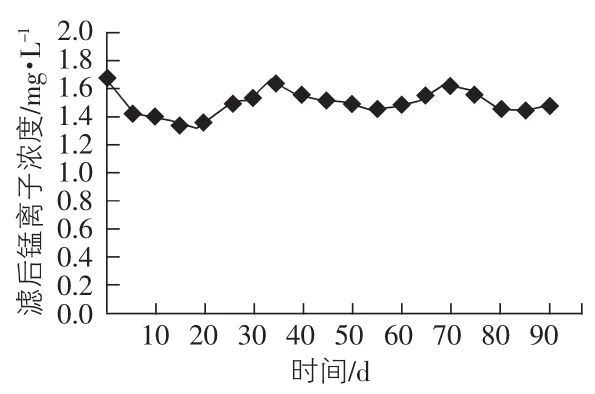
图3 丙柱滤后锰离子浓度历时变化曲线
由图1可知,甲柱为河南巩义天然锰砂,在60 d之前甲柱滤后锰离子浓度在0.8 mg/L~1.60 mg/L之间变化,在60 d后锰质滤膜开始形成,曲线斜率较大[2],锰离子浓度逐渐下降,在85 d后才达到饮用水标准0.1 mg/L且稳定。这表明A柱天然锰砂滤料稳定成熟期为85 d,是由于巩义锰砂MnO2含量偏低,且滤料表面光滑,孔隙率较小吸附能力差,活性滤膜形成时间长,因此导致除锰率较低[7]。由图2可知,在运行初期时,乙柱滤后锰离子浓度在1.05 mg/L~1.50 mg/L之间变化,降解率比较低,而在45 d后,锰离子浓度下降较快,同时形成了活性滤膜,第45天~第65天滤后水锰离子质量浓度从1.50 mg/L逐渐下降到0.15 mg/L,在第70天后滤后锰离子浓度才降到0.05 mg/L且稳定,满足饮用水标准,稳定成熟期为70 d,因此表明锦西天然锰砂具有较高含量的MnO2,能更好的吸附水中的锰离子,且成熟期短[2]。由图3可知,在整个运行过程中,丙柱活化沸石滤料上未形成具有催化作用的锰质活性滤膜,锰离子浓度始终在1.20 mg/L~1.32 mg/L变化,锰离子浓度降幅很小,基本没有体现出除锰能力。其主要原因是活化沸石属于吸附能力较弱的滤料,对Mn2+的吸附作用较差,且其成分缺少对Mn2+的催化氧化作用,另外在运行过程中,反冲洗对滤料上附着的少量MnO2具有洗脱作用[3-8],所以MnO2很难在滤料上大量积累而形成锰质活性滤膜,因此除锰效率极低。
综上,通过分析滤后水含锰量峰值和稳定成熟期时长可知,乙柱锦西天然锰砂成熟期最短,吸附能力较强,降解速率快,滤后锰离子浓度最低,对水中锰离子的去除效果最佳。
3 结语
1)本实验原水平均含锰量为1.85 mg/L,属低锰类型地下水,通过实验已证明采用二级跌水曝气加单级过滤处理工艺是可行可靠的,滤后锰离子浓度达到0.1 mg/L的饮用水标准。2)铁锰氧化去除的关键是锰质活性滤膜的自催化氧化作用,滤料经长期使用,会形成以细砂为核心的球形锰质滤料,且表面的锰质滤膜愈积愈厚,接触氧化能力很强,对除锰有益,直到细砂外包物过厚使粒径过粗,影响出水水质时才需部分更换。3)通过比较3种不同的滤料对新民市农村地下水的处理,并测得甲柱河南巩义天然锰砂和乙柱锦西天然锰砂的滤料稳定成熟期分别为85 d和70 d,丙柱活化沸石上未形成锰质活性滤膜,不具有除锰能力。其中乙柱锦西天然锰砂成熟期最短,滤后锰离子浓度最低,对水中锰离子的去除效果最佳,是较为理想的优质天然锰砂滤料。
[1]陈心凤.接触氧化法和吸附法对水中铁锰的去除试验研究[D].杭州:浙江大学,2011.
[2]陈宇辉,余 健,谢水波.地下水除铁除锰研究的问题与发展[J].工业用水与废水,2003,34(3):1-4.
[3]毛艳丽,罗世田,师军帅.不同滤料去除地下水中铁锰效果的试验研究[J].平顶山学院学报,2006,21(5):41-43.
[4]栾 岚,詹 健,贾俊松.地下水除铁除锰技术的分析及其发展方向初探[J].江西化工,2006(1):103-105.
[5]刘仁锋.成套地下水除铁除锰装置的工艺设计[J].江西化工,2007(1):35-38.
[6]朱秀芹,李灿波.地下水除铁除锰技术发展历程及展望[J].黑龙江水利科技,2008(6):78-80.
[7]陈正清,别东来,钟 俊.不同滤料除铁除锰效果研究[J].环境保护科学,2005,31(129):22-24.
[8]薛 罡,邹联沛,刘建勇,等.接触氧化法除地下水铁锰时不同滤料性能的对比研究[J].东华大学学报(自然科学版),2002(6):212-213.



