汪春晖
(江西省会昌县人民医院神经外科,江西 赣州 342600)
高血压性脑出血(HICH)是高血压患者最严重的并发症之一,因长期高血压导致脑内小动脉管壁发生变性、缺血、坏死、微小动脉瘤等病理改变,因此,当血压急剧升高时,颅内小血管破裂导致脑出血。临床表现为典型的三偏征,即对侧偏瘫、偏侧感觉障碍以及偏盲[1-2]。壳核和丘脑是高血压性脑出血最常见的病发部位,称为高血压性基底节区脑出血[3]。高血压性基底节区脑出血发病急,发展快,致残和致死率极高,但通过积极合理的治疗,可以挽救患者的生命。及时清除血肿是临床公认的治疗手段,可有效降低患者颅内压,减少对神经功能的损伤。随着微创技术的不断发展,微创颅内血肿清除术对治疗HICH具有良好的效果,且可有效改善患者的预后[4]。但仍存在术后再出血的情况,术后再出血对患者的预后影响较大,致死率较高。为进一步了解HICH术后再出血的原因,本研究对HICH患者进行回顾性分析,旨在为临床防治HICH术后再出血提供新思路。
1 资料与方法
1.1一般资料:经本院伦理委员会审核通过,回顾性选取2018年1月~2021年5月在本院行微创颅内血肿清除术的80例高血压性脑出血患者,男54例,女26例,年龄55~78岁,平均(66.45±5.29)岁。根据微创颅内血肿清除术后是否发生再出血分为出血组(16例)和未出血组(64例)。①纳入标准:符合高血压脑出血诊断标准[5];均为基底核区出血;均为首次发病行微创颅内血肿清除术者;均在发病24 h行手术治疗;微创颅内血肿清除术均采用额部及颞部入路;临床资料完整。②排除标准:合并颅内动脉瘤者;合并颅脑外伤性出血者;有脑动静脉畸形者;有脑疝形成者;合并严重感染性疾病者;有凝血功能障碍者。
1.2方法:80例HICH患者在入院时均给予降压、维持水电解质平衡,预防感染等基础对症治疗,术后均常规给予甘露醇脱水、维持血压平衡、止血、抗感染及营养支持等对症治疗。均采用额部入路微创颅内血肿清除术:术前行头颅CT进行定位,确定穿刺点和穿刺深度,选择合适型号的穿刺针在血肿量最大平面进行操作,用电钻在额颞部区钻孔后进针,避开大血管和重要功能区,放置引流管,拔出穿刺针,轻轻抽吸液体血肿,抽出量控制在总血肿量的30%~40%,将引流管置入引流瓶,根据患者情况给予尿激酶,夹管2~4 h后开放持续引流4~7 d,复查CT,血肿清除量在总血肿量的4/5时即可拔出引流管。80例患者手术均由同一组医师完成。
1.3术后再出血判断标准[6]:术后对患者进行颅脑CT复查:①术后24 h内经颅脑CT复查表明原有出血部位血肿,且血肿范围较术前大;②术后24 h后经颅脑CT复查血肿消失,再次经颅脑CT 复查发现原有血肿部位再次出现血肿;③术后CT复查发现颅内血肿体积较术前血肿体积增加30%以上。
1.4观察指标:自制调查表,通过查阅病例的方式收集患者的一般资料,包括:年龄、性别、围术期血压、术前血肿量、发病至手术时间、术前格拉斯哥昏迷指数(GCS)评分、合并基础疾病、术中及术后是否使用镇静镇痛药物,术中是否出现止血困难等。
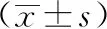
2 结果
2.1出血组与未出血组临床相关资料比较:HICH患者微创颅脑血肿清除术后再出血可能与其收缩压、术前GCS评分、术前血肿量、是否使用镇静镇痛药物有关,差异有统计学意义(P<0.05)。见表1。
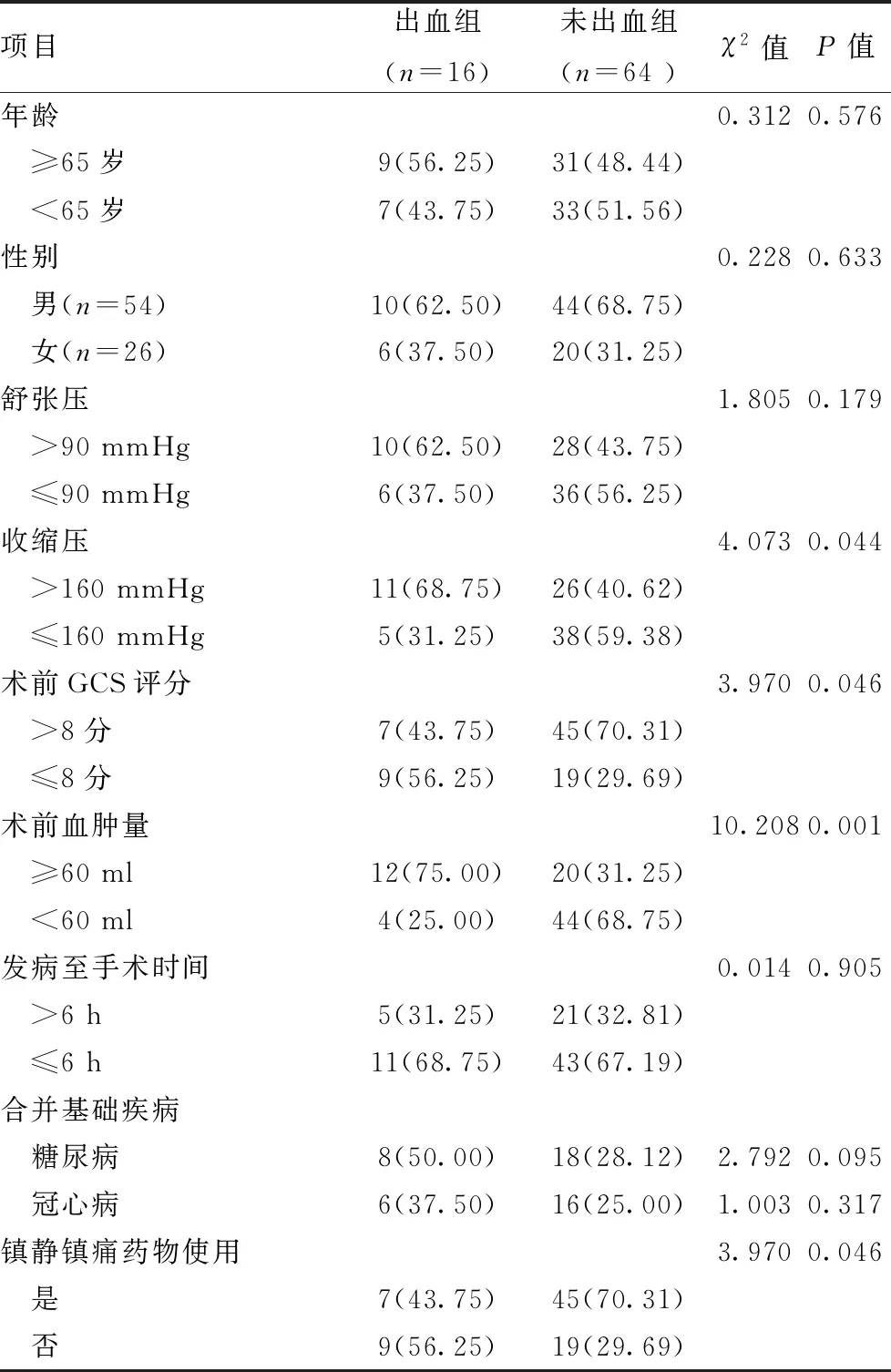
表1 出血组与未出血组临床相关资料比较[n(%)]
2.2影响因素变量赋值:影响因素变量赋值,见表2。

表2 影响因素变量赋值表
2.3HICH患者术后再出血多因素Logistic回归分析:收缩压>160 mmHg,术前血肿量≥60 ml是影响HICH患者术后再出血的独立危险因素,差异有统计学意义(P<0.05)。见表3。
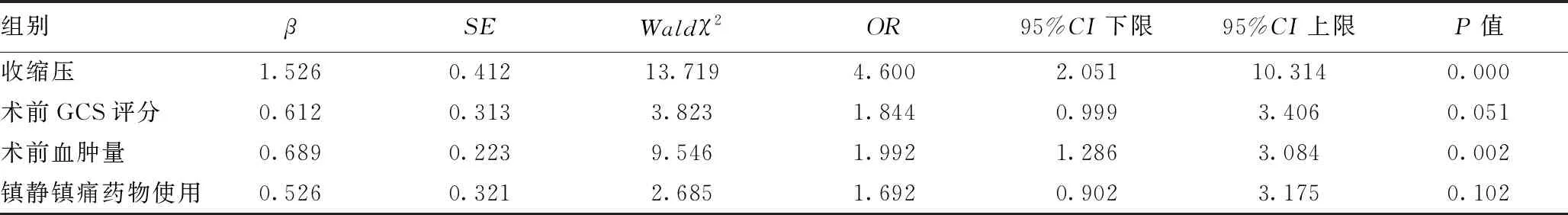
表3 HICH患者术后再出血多因素Logistic回归分析(r值)
3 讨论
HICH起病急、发展快,血肿的形成会对脑组织进行压迫,导致脑组织的进一步损伤[7]。如不及时进行干预处理,最终可能导致患者的脑组织坏死,神经功能障碍,严重者导致死亡,对患者的生命安全有很大的威胁。清除颅内血肿是治疗HICH的主要手段,及时清除血肿可有效降低患者神经功能的损害率,微创颅脑血肿清除术是临床常用的手术方式,在减轻患者的负担的同时具有良好的临床疗效[8]。术后再出血是HICH术后并发症的一种,致死致残率极高,严重威胁着患者的生活质量和生命安全,因此了解HICH术后再出血的危险因素,对危险信号进行预警,提前采取干预措施,是减少再出血发生率的关键。本研究结果显示,HICH患者微创颅脑血肿清除术后再出血可能与其基础收缩压,术前GCS评分,术前血肿量,是否使用镇静镇痛药物有关,现对此结果进行逐一分析。
3.1围术期收缩压对HICH患者术后发生再出血的影响:经多因素Logistic回归分析显示,围术期收缩压>160 mmHg是导致术后再出血的独立危险因素。认为可能与血压控制不稳有关,血压升高使脑血流量和颅内压增高,使原本凝固的小血管再次发生破裂。既往研究[9]表示,当收缩压高于200 mmHg时血肿扩大的概率会升高。调查[10]显示,在脑出血发病后的收缩压超过140 mmHg,其死亡率和致残率均增大约1倍左右。Zhang等研究[11]也表示,血压变异性与HICH术后再出血的发生具有一定的相关性,本研究与其相似,提示早期降低患者的收缩压且进行稳定控制有助于减少术后再出血发生的概率。但降低血压并不能盲目的进行降压,需根据患者的病史及基础疾病来进行降压治疗,以防止因过度降压而导致的脑灌注量不足[12]。临床也应对HICH患者进行严密的血压监护,进行实时监测,动态观察患者的血压波动情况以及时采取干预措施。
3.2术前GCS评分对HICH患者术后发生再出血的影响:术前GCS评分与HICH患者术后发生再出血有关。GCS评分可反映患者意识障碍程度,评分越低,说明患者的意识障碍程度越重[13],说明患者脑出血对其脑神经功能的损害程度越重。患者脑出血后形成的血肿对患者脑组织进行压迫,其脑水肿的程度越深,术后患者可能出现抽搐、躁动不安等情况出现,可能导致血压波动大,导致再出血的发生。临床对于术前GCS评分较低的患者应提高警惕,且GCS评分可用于患者术后预后的一项评估指标[14],于患者围术期可每日进行评估,观察患者评分曲线变化,判断患者病情变化。
3.3术前血肿量及镇静镇痛药物的使用对HICH患者术后发生再出血的影响:上述脑出血产生的血肿会对脑组织进行压迫,血肿量越大,对患者脑组织压迫越严重,对其脑损伤的程度越重,增加脑部组织的水肿及坏死程度可能会导致患者脑部更多的血管受到损害,增加再出血的风险。本研究显示,术前血肿量是影响HICH患者术后再出血的独立危险因素。因而对于血肿量大的患者应及时行血肿清除术,以解除血肿对周围组织的压迫,减低脑损伤程度,改善患者预后。临床认为从发病至手术时间在6 h内最好,既往研究[15]也提到,手术时机对HICH患者术后再出血的发生具有较大的影响。本研究结果未在此项体现,原因可能在于本研究所纳入病例多数于6 h行手术治疗。
HICH患者术后疼痛会使患者产生烦躁不安的情绪,极易导致患者术后血压的波动。近年来,HICH术后镇痛镇静得到了临床广泛的关注。既往研究[16]提出,术后合理的使用镇痛镇静药物可有效提高患者的舒适度,降低患者的应激反应,对术后血压的稳定有一定的帮助,从而防止术后再出血的发生。
综上所述,HICH患者微创颅脑血肿清除术后再出血可能与其收缩压、术前GCS评分、术前血肿量、是否使用镇静镇痛药物有关,收缩压>160 mmHg、术前血肿量≥60 ml是影响HICH患者术后再出血的独立危险因素。在HICH患者的治疗中应对患者的血压进行严密的动态检测,加强患者血压控制,规范使用镇痛镇静药物,严密观察患者的意识、瞳孔及生命体征的变化,及早采取干预措施。



