刘 燕,王 辉,张 伟,丁小娟,吕 凌
(1.安徽食品药品检验研究院,安徽合肥 230051;2.安徽贝克联合制药有限公司,安徽太和 236604;3.安徽中医药大学药学院,安徽合肥 230031)
核苷类药物广泛用于乙型肝炎的治疗,如拉米夫定、恩替卡韦、阿德福韦等,但乙肝病毒随着核苷类抗病毒药物的应用,其耐药性问题也渐渐突显出来。富马酸替诺福韦作为一种新型核苷酸逆转录酶抑制剂,美国FDA于2001年批准用于治疗艾滋病治疗后,在临床应用中发现其能有效抑制乙型肝炎病毒的复制,2008年后替诺福韦相继被美国和欧洲批准用于治疗成人慢性乙型肝炎的治疗,成为第五个治疗乙肝病毒的核苷类似物[1-4]。根据其合成工艺路线,替诺福韦中可能残留的有机溶剂有N,N-二甲基甲酰胺、二氯甲烷、乙腈、乙醇、N-甲基吡咯烷酮、乙酸乙酯、异丙醇、氯甲基异丙基碳酸酯,由于使用的有机溶剂多数对人体有较大的危害,故为确保其治疗效果,降低毒副作用,对其在合成过程中所使用的有机溶剂的残留进行检测。
1 仪器与试剂
岛津GC-14C气相色谱仪,N2000色谱工作站。乙醇、异丙醇、二氯甲烷、乙腈、乙酸乙酯、N,N-二甲基甲酰胺、氯甲基异丙基碳酸酯、N-甲基吡咯烷酮。
2 方法与结果
2.1 色谱条件与系统适用性 色谱条件:色谱柱为VF-17ms毛细管柱(30 m ×0.25 mm ×0.25(m),FID检测器,进样口温度150℃,检测器温度250℃,不分流进样。程序升温:初始30℃,保持6 min,每分钟40℃升至220℃,保持8 min。进样体积为 1 μL,载气为高纯氮气 99.99%。
系统适用性试验:取混合对照品溶液按2.1项下色谱条件进样,记录色谱图,见图1。测得乙醇、异丙醇、二氯甲烷、乙腈、乙酸乙酯、N,N-二甲基甲酰胺、氯甲基异丙基碳酸酯、N-甲基吡咯烷酮理论塔板数分别为:15 410、5 886、16 815、21 548、4 035、45 609、283 424、291 096。乙醇、异丙醇、二氯甲烷、乙腈、乙酸乙酯、N,N-二甲基甲酰胺、氯甲基异丙基碳酸酯、N-甲基吡咯烷酮的分离度均大于1.5。
空白溶剂测定:取二甲亚砜,按2.1项下色谱条件进样,结果见图2。
2.2 溶液配制 对照品溶液配制:精密称取乙醇0.50 g、异丙醇 0.50 g、二氯甲烷 0.06 g、乙腈 0.041 g、乙酸乙酯 0.50 g、N,N-二甲基甲酰胺 0.088 g、氯甲基异丙基碳酸酯0.50 g、N-甲基吡咯烷酮0.053 g,置同一50 mL的量瓶中,加二甲亚砜适量充分振摇使溶解,稀释至刻度,摇匀,即得混合对照品贮备液,精密量取混合对照品贮备液5 mL,置50 mL的量瓶中,用二甲亚砜稀释至刻度,摇匀,即得混合对照品溶液。
供试品溶液的制备:精密称取本品适量,用适量二甲亚砜溶解并稀释成每1 mL中约含0.2 g的溶液,摇匀,即得供试品溶液。
2.3 方法学考察 (1)标准曲线的制备:精密称取乙醇0.499 5 g、异丙醇0.503 9 g、二氯甲烷0.057 2 g、乙腈 0.042 9 g、乙酸乙酯 0.500 0 g、N,N-二甲基甲酰胺0.089 3 g、氯甲基异丙基碳酸酯0.495 1 g、N-甲基吡咯烷酮0.048 6 g,置同一10 mL的量瓶中,加适量二甲亚砜振摇溶解后稀释至刻度,摇匀,作为混合对照品贮备液,精密量取混合对照品贮备液,用二甲亚砜稀释成一系列不同浓度的混合对照品溶液,按2.1项下色谱条件进样,记录色谱图,以各峰的峰面积(A)对相应质量浓度(C)进行线性回归,结果见表1。
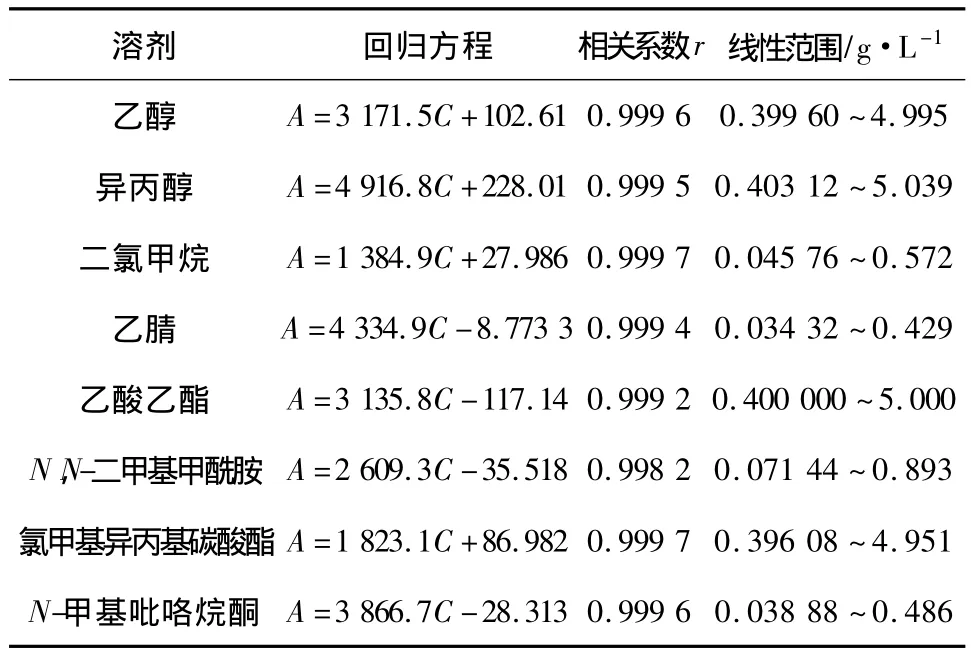
表1 有机溶剂标准曲线测定结果
(2)精密度实验:精密取混合对照品溶液1 μL,按2.1项下色谱条件,连续进样6次,记录色谱图并计算RSD值,结果乙醇、异丙醇、二氯甲烷、乙腈、乙酸乙酯、N,N-二甲基甲酰胺、氯甲基异丙基碳酸酯、N-甲基吡咯烷酮的 RSD分别为 6.02%、3.62%、5.56%、9.19%、3.74%、7.94%、3.71%、6.43%,表明仪器精密度良好,方法重现性合格。
(3)检测限:分别按照对照品溶液的制备方法精密称取8种溶剂适量,不断用二甲亚砜稀释制成供试液,精密量取1 μL注入气相色谱仪,直至信噪比(S/N)≥3,记录色谱图。结果乙醇、异丙醇、二氯甲烷、乙腈、乙酸乙酯、N,N-二甲基甲酰胺、氯甲基异丙基碳酸酯、N-甲基吡咯烷酮的检测限分别为39.96、40.312、45.76、34.32、40、71.44、39.608、38.88 ng。
(4)加样回收率实验:精密称取已测定乙醇、异丙醇、二氯甲烷、乙腈、乙酸乙酯、N,N-二甲基甲酰胺、氯甲基异丙基碳酸酯、N-甲基吡咯烷酮含量的腺嘌呤衍生物9份,每份约5 g,按2.2项下配制供试品溶液,按2.1项下色谱条件进样测定,计算各对照品的平均加样回收率和RSD值,结果显示各对照品的平均回收率为 104.55%、106.44%、106.59%、102.25%、95.78%、98.53%、99.38%、95.83%,RSD 分别为 1.35%、1.46%、2.11%、3.22%、2.17%、1.79%、2.33%、2.92%(n=9)。
2.4 样品测定 取三批样品,按2.2项下供试品溶液配制方法配制溶液,按2.1项下色谱条件进样,记录色谱图,见图3,结果显示,样品中测出乙酸乙酯和N-甲基吡咯烷酮两个组分,其余6个溶剂均未检出,见表2。
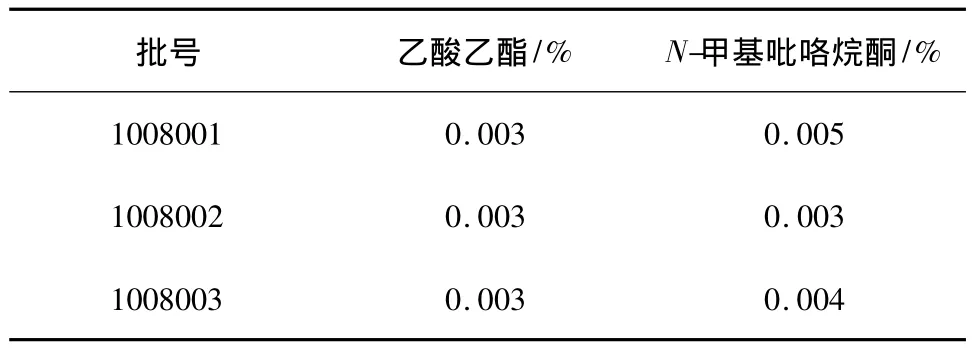
表2 有机溶剂残留量的测定结果(n=3)
3 结果
本实验建立了一种腺嘌呤衍生物中有机溶剂残留的气相色谱测定方法,该方法灵敏度高,具有较好的重现性,在三批样品中检测到乙酸乙酯和N-甲基吡咯烷酮的残留,未检测到乙醇、异丙醇、二氯甲烷、乙腈、N,N-二甲基甲酰胺、氯甲基异丙基碳酸酯。
4 讨论
药品中的有机溶剂残留系指药品原料药、辅料以及制剂生产中使用的,但在工艺过程中未完全除去的有机挥发性化合物,由于这些溶剂大多对人体有害,故要严格控制其在药品原辅料及其制剂中的残留量,确保用药的安全性和有效性。
[1]张 宁,罗生强.替诺福韦治疗慢性乙型肝炎的新进展[J].中国新药杂志,2013,22(11):1269-1273,1310.
[2]何雅婧,孙 剑,侯金林.抗乙型肝炎病毒治疗新药替诺福韦[J].药学与临床研究,2011,19(5):385-387.
[3]席小莉,杨曼曼,杨 频.8-氮杂腺嘌呤及其金属配合物与DNA的作用机理[J].光谱学与光谱分析,2006,26(12):2272-2275.
[4]Lok AS,McMahon BJ.Chronic hepatitis B:Update 2009[J].Hepatalogy,2009,50(3):661-662.
[5]李继昌.替诺福韦治疗重型乙肝临床疗效分析[J].海南医学院学报,2012,18(10):1455-1457.
[6]张 林,江艳燕,顾雪梅,等.替诺福韦治疗慢性重型乙型肝炎临床研究[J].现代生物医学进展,2012,12(36):7089-7091.
[7]邓晓军,阳 辉,欧 松,等.替诺福韦、拉米夫定、依非韦伦联合治疗HBV/HIV合并感染的疗效和安全性[J].中国感染与化疗杂志,2014,14(2):132-133.
[8]朱浩翔,张继明.抗HBV药物—替诺福韦[J].肝脏,2011,16(2):145-147.
[9]姚彦斌,陈 剑,徐宇虹.替诺福韦阳离子脂质体的制备及其对人体肝细胞SMMC-7721摄取和细胞毒性研究[J].中国药房,2007,18(34):2655-2658.
[10]吴亚松,张福杰.替诺福韦肾脏毒性及其遗传易感性[J].中国病原生物学杂志,2010,5(7):539-540,543.



