阎 博,吴 芳,刘海静,,唐瑜蓉,乔蓉霞
(1.陕西中医学院,陕西 咸阳 712046;2.陕西省食品药品检验所,陕西 西安 710061)
HPLC-ELSD法测定葛兰心宁软胶囊中绞股蓝皂苷XL IL的含量
阎博1,吴芳2,刘海静1,2,唐瑜蓉1,乔蓉霞2
(1.陕西中医学院,陕西 咸阳712046;2.陕西省食品药品检验所,陕西 西安710061)
摘要:目的建立以HPLC-ELSD法测定葛兰心宁软胶囊中绞股蓝皂苷XL IX含量的方法。方法色谱柱为Kromasil C18(250 mm × 4.6 mm,5 μm),流动相为乙腈—水(35∶65),检测器为蒸发光散射检测器,流速2.8 L·min-1,漂移管温度105℃。结果绞股蓝皂苷XL IL的线性良好,Y(峰面积)=1.56X+5.25,r=0.999,平均回收率(n=6)为101.56%,绞股蓝皂苷XL IX在0.513~10.254 μg范围内线性关系良好。。结论该方法专属性强、重复性良好,可用于葛兰心宁软胶囊的质量控制。
关键词:葛兰心宁软胶囊;HPLC;绞股蓝皂苷XL IX;含量测定
葛兰心宁软胶囊处方由葛根总黄酮、山楂提取物和绞股蓝总苷组成,有活血化瘀,通络止痛的功效,用于瘀血闭阻所致的冠心病、心绞痛。绞股蓝中主要含皂苷类成分,此外还含有黄酮类、氨基酸、糖、微量元素等成分。对机体代谢、应激性反应、抗癌作用、对神经系统的影响、增强机体免疫功能。据文献记载,绞股蓝皂苷具有较好的抗癌作用并且能明显提高小鼠空斑形成细胞和血凝抗体[1];也有采用荧光光谱法研究绞股蓝皂苷对人血清白蛋白(HSA)的猝灭作用[2]。葛兰心宁软胶囊现行质量标准中未对绞股蓝总苷进行质量控制。绞股蓝总苷的企业标准中薄层色谱鉴别项和含量测定项均以绞股蓝皂苷-A为对照品,但绞股蓝皂苷-A对照品不能从中国食品药品检定研究院和其他机构获得,故目前标准中未对绞股蓝总苷进行有效的控制。
葛兰心宁软胶囊是2012年国家药品标准提高行动计划品种,根据国家药典委员会要求,我们对处方中绞股蓝总苷的质量控制方法进行了研究。近年来我省食品药品行业通过测定绞股蓝皂苷XL IL的含量控制绞股蓝总苷的质量。我们使用购自西安鸿程生物科技有限公司的绞股蓝皂苷XL IL对照品进行了以下含量测定方法学试验,本文参考相关文献[3-4],采用HPLC-ELSD法测定绞股蓝皂苷XL IL的含量,以对绞股蓝相关制品质量控制提高参考依据。
1仪器、试剂及试药
1.1仪器高效液相色谱仪(Waters HT系统、Waters Allance系统),Alltech 2000ES蒸发光散射检测器,德国塞多利斯公司BP2110电子分析天平,BS224S电子分析天平。
1.2试剂乙腈(色谱纯,TEDIA公司)、葛兰心宁软胶囊(批号分别为20120221、20120222、20120223、20120224、20120225、20120226、20120227、20120228、20120229、20120231)、高纯水,其余试剂均为分析纯。
1.3样品绞股蓝皂苷XL IX对照品购自西安鸿程生物科技有限公司,批号为20100718,HPLC纯度为99.9%。
2方法与结果
2.1色谱条件色谱柱(Kromasil 100-5C18250 mm×4.6 mm,E59030);流速:1.0 mL·min-1;柱温:35℃;Alltech ELSD 2000ES蒸发光散射检测器,流动相为乙腈—水(35∶65),流速2.8 L·min-1,漂移管温度105℃;理论板数按绞股蓝皂苷XL IL峰计应不低于2 000。
2.2溶液的配制
2.2.1对照品溶液的制备称取80 ℃减压干燥3 h的绞股蓝皂苷XL IX对照品适量,精密称定,加甲醇制成每1 mL含0.5 mg的溶液,即得。
2.2.2供试品溶液的制备取本品10粒内容物(尽量取尽胶囊内壁残留),将内容物混匀,取约1.5 g,置锥形瓶中,加10%甲醇40 mL,水浴回流40 min,用少量棉花滤过,用10 mL水洗涤玻璃容器和棉花,滤液合并于分液漏斗中,用乙醚40 mL振摇提取,弃去乙醚液,水液用水饱和的正丁醇振摇提取3次,每次40 mL,合并正丁醇液,再分别用氨试液30 mL和正丁醇饱和的水30 mL洗涤,弃去洗涤液。正丁醇液蒸干,残渣加甲醇并定容于10 mL容量瓶中,摇匀,作为供试品溶液。
2.2.3测定法分别精密吸取对照品溶液10、20 μL,与供试品溶液各10 μL,注入液相色谱仪,测定,以外标两点法对数方程计算,即得。
2.3专属性试验按上述方法制备缺绞股蓝总苷提取物的阴性溶液、对照品溶液、供试品溶液,分别进入液相色谱仪,阴性样品的色谱图在与绞股蓝皂苷XL IX对照品色谱峰相同保留时间处未见明显色谱峰,见图1。
2.4线性关系考察称取绞股蓝皂苷XL IX 12.83 mg,置于25 mL的容量瓶中,用甲醇稀释至刻度,摇匀,浓度为0.5132 g·L-1。按上述色谱条件进行测定,分别进样1、2、4、6、8、10、15、20 μL,以对照品的进样量(μg)对数值为横坐标,以峰面积积分值对数值为纵坐标,绘制标准曲线,其回归方程为:Y(峰面积)=1.56X+5.25,r=0.999,结果表明绞股蓝皂苷XL IX在0.513~10.254 μg范围内线性关系良好。
2.5重复性试验取样品(批号:20120226 )按供试品溶液的制备方法制备6份溶液进行测定。测得取样量,代入公式计算。绞股蓝皂苷XL IX的平均含量为每粒1.27 mg,RSD为2.1%。
2.6加样回收率试验精密称定绞股蓝皂苷XL IX 30.35 mg,置于25 mL的容量瓶中,用甲醇稀释至刻度,摇匀,浓度为1.214 g·L-1。取6份上述对照品溶液2 mL置锥形瓶中,蒸干甲醇。取已知含量的样品(批号:20120226)适量,精密称定6份,分别置上述各锥形瓶中,按供试品溶液的制备方法制备溶液,测定回收率,结果得平均回收率为101.56%,RSD为2.4%。见表1。
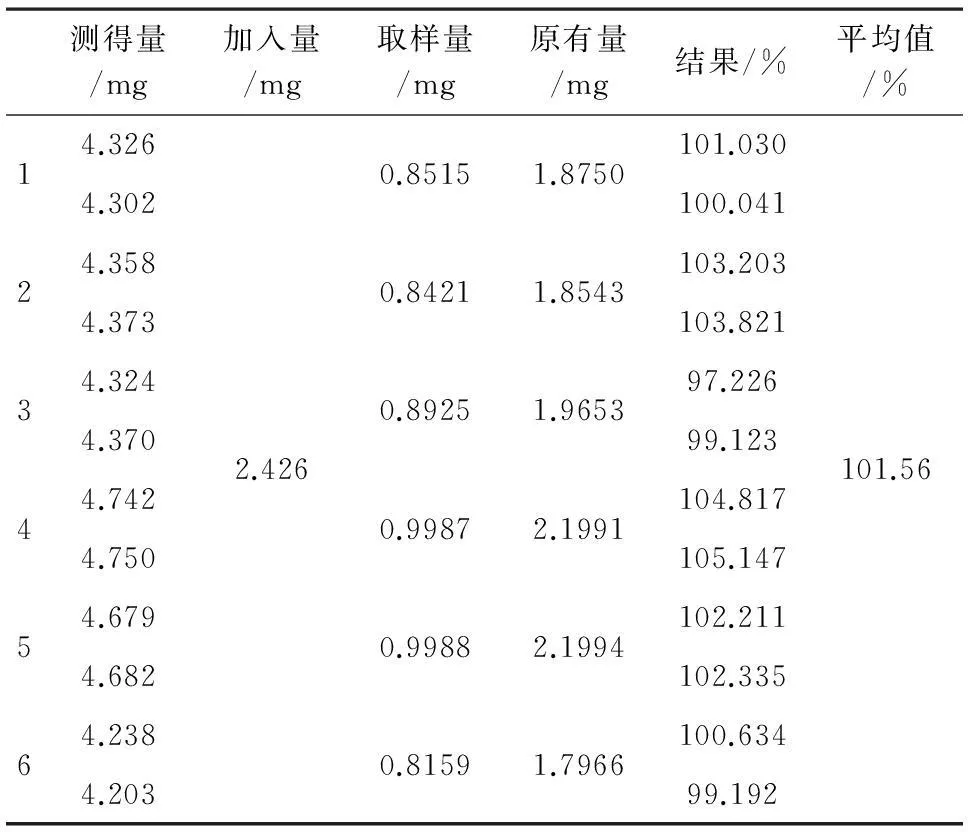
表1 加样回收率试验结果
2.7精密度试验取对照品溶液连续进样6次进行测定。绞股蓝皂苷XL IX的保留时间和峰面积RSD分别为0.2%和1.0%,表明精密度良好。
2.8稳定性试验取样品(批号:20120226)按供试品溶液的制备方法制备5份溶液,分别于制备后0、5、10、15、19、22、26、31、35、40 h后测定峰面积,绞股蓝皂苷XL IX含量的RSD为3.0%。表明样品溶液在制备后40 h内,绞股蓝皂苷XL IX的量值稳定。
2.9样品测定采用上述2.1和2.2项下的方法,对 10批样品进行含量测定,葛兰心宁软胶囊中绞股蓝皂苷XL IX的含量为每粒1.28~1.40 mg。
3讨论
3.1提取方法考察对提取溶剂甲醇、水、10%甲醇为溶剂分别进行了考察;对超声、水浴回流等提取方式进行了考察;考察了水饱和正丁醇的提取2、3、4次的样品的含量以及正丁醇饱和的水洗涤的效果进行了考察,根据样品含量测定的结果,最终确定了以10%甲醇为提取溶剂进行水浴回流,以水饱和正丁醇提取3次后,以正丁醇饱和的水进行洗涤。
3.2转移率测定取生产用的同批次绞股蓝总苷的原料,测定其中绞股蓝皂苷XL IX的含量,根据含量和处方量折算葛兰心宁软胶囊的理论值。实际测量值与理论含量的比值即为转移率,测定的10批样品的转移率为87.5%~98.1%。
3.3关于绞股蓝总苷的质量控制方法据文献报道:有人以参皂苷Rb1为对照,利用UV法测定含量测定[5-6],以绞股蓝皂苷为对照品进行定性鉴别[7],进行HPLC法绞股蓝皂苷含量测定时利用的对照品还有人参皂苷Rb1[8]、绞股蓝中绞股蓝皂苷B[9]、绞股蓝皂苷A。还有采用SPME-GC-MS法对5个不同地区绞股蓝中挥发性成分进行分析[10]。 以绞股蓝皂苷XL IX为对照品进行质量控制为首次报道。
参考文献:
[1]李杰,杨舟,詹琤琤.绞股蓝化学成分与药理作用研究概况[J].湖北中医杂志,2012,34(10):74-76.
[2]何丽君,霍彩霞,李生英,等.荧光光谱法研究绞股蓝皂苷与人血清白蛋白的相互作用[J].甘肃联合大学学报(自然科学版),2012,26(6):41-51.
[3]李长根.HPLC-ELSD法测定十味芪术通窍合剂中黄芪甲苷含量[J].安徽医药,2013,17(3):402-403.
[4]汤兴球,汪伍承.HPLC-ELSD法同时测定烟腈丁醇片中盐酸乙胺丁醇和异烟肼的含量[J].安徽医药,2012,16(5):616-617.
[5]乐圆,肖娅萍,张宁,等.HPLC-ELSD法测定绞股蓝中绞股蓝皂苷A的含量[J].光谱实验室,2010,19(5):1734-1737.
[6]李风华,陈素红,吕圭源.7个不同产地绞股蓝皂苷含量测定[J].中华中医药学刊,2012,30(4):887-888.
[7]熊野娟.复方绞股蓝胶囊质量标准研究[J].药物鉴定,2011,20(15):29-30.
[8]陈丹,李柯,吴梅青,等.HPLC法测定湖南省不同产地绞股蓝药材中人参皂苷Rb1的含量[J].中国保健营养,2013,18(4):557-558.
[9]刘春祥,张群,谢二磊,等.RP-HPLC法测定绞股蓝中绞股蓝皂苷B的含量[J].中国药品标准,2013(1):7-9.
[10] 牛俊峰,肖娅萍,姜东亮,等.5个不同地区绞股蓝中挥发性成分的SPME-GC-MS 分析[J].药物分析,2012,32(4):578-582.
Determination of Gypenoside XL IL in Gelan
Xinning soft capsule by HPLC-ELSD
YAN Bo1,WU Fang2,LIU Hai-jing1,2,et al
(1.ShaanxiUniversityofChineseMedicine,Xianyang,Shaanxi712046,China;
2.ShaanxiInstituteforFoodandDrugControlDrugControl,Xi’an,Shaanxi710061,China)
Abstract:ObjectiveToestablishadeterminationmethodofGypenosideXLILinGelanXinningsoftcapsulebyHPLC-ELSD.MethodsSampleswereanalyzedonaKromasilC18column(250mm× 4.6mm,5μm).Themobilephasewasacetonitrile-water(35:65).TheELSDdetectorwasused,withaflowrateofatomizerat2.8L·min-1andthetemperatureofdrifttubewas105℃.ResultsThemethodhadalinearrelationshipintherangeof0.513~10.254μg(r=0.999)andtheaveragerecoveryratewas101.56%(n=6).ConclusionsThemethodishighlyspecific,accurate,sensitiveandreproducible,whichcanbeusedforthequalitycontrolofGelanXinningsoftcapsule.
Keywords:GelanXinningsoftcapsule;HPLC;GypenosideXLIL;determination
(收稿日期:2014-03-12,修回日期:2014-06-09)
通信作者:刘海静,女,主任药师,硕士生导师,研究方向:药物分析,E-mail: liuhaijing1@163.com
作者简介:阎博,女,硕士研究生
基金项目:陕西省科技统筹创新工程计划项目(No 2013KTCQ03-14)
doi:10.3969/j.issn.1009-6469.2015.02.015



