张 冕,万 芳
(荆楚理工学院化工与药学院,湖北荆门 448000)
川芎嗪是一种生物碱单体,近年来其在眼科领域的应用研究得到了广大学者的关注。大量研究表明,川芎嗪对视网膜损伤性疾病有一定的疗效,包括对糖尿病视网膜病变和视网膜缺血再灌注损伤的保护作用、对原发性慢性闭角型青光眼术后的眼压具有良好的调节作用、对高眼压下视网膜神经节细胞和双极细胞损伤尚有保护作用[1-5],为川芎嗪在眼部应用奠定了广泛的实验基础。
对于眼部给药,由于结膜囊内充斥着不断更新的泪液,泪液对制剂表面可产生类似眨眼的剪切作用,水溶性凝胶在眼内逐渐溶蚀并释放其中的药物,因此可能存在不同的释药机制。目前文献报道的体外释药特性的研究方法可分为有膜释药试验和无膜释药试验,有膜释药多采用立式扩散池或透析袋法,无膜溶出模型除去了有膜释药试验中的半透膜,更好地模拟眼内泪液不断分泌溶蚀的情况,因此无膜溶出模型更适合于眼用凝胶剂体外释药特性的研究[6]。
温敏原位凝胶以溶液状态给药[7],给药后能立即在用药部位发生相转变,成为半固体的凝胶状态。和传统眼用制剂相比,温敏原位凝胶给药剂量准确,重现性好,滞留时间长,具有良好的应用前景。本文笔者采用泊洛沙姆为温敏基质制备凝胶,并采用无膜溶出模型考察其释药行为,并对其释放机制进行初步的探讨。
1 仪器与试药
梅特勒—托利多电子天平(上海梅特勒—托利多仪器有限公司);RCZ-6C3智能溶出试验仪(上海黄海药检仪器有限公司);HZS-H水浴振荡器(哈尔滨东联电子技术开发有限公司);R2010型恒温水浴锅(巩义市予华仪器有限责任公司);LVDV-C型数显转子黏度计(美国博勒飞);TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);Agilent 1100高效液相仪(美国 Agilent公司)。
盐酸川芎嗪对照品(批号110817-201307,中国食品药品检定研究院);盐酸川芎嗪(济南德瑞丰环保化工有限公司提供,含量99.8%);泊洛沙姆407(P407)、泊洛沙姆188(P188)均由BASF提供;人工泪液(将氯化钠 6.7 g、二水氯化钙 0.08 g、碳酸氢钠2 g、氯化钾1.4 g,加纯化水1 L溶解,用硼酸调节pH为7.4,自制);甲醇为色谱纯;其余所用试剂均为分析纯。
2 方法与结果
2.1 含量测定方法
2.1.1 最大吸收波长的测定 分别配制盐酸川芎嗪在水、人工泪液中的溶液,在波长200~400 nm范围内进行紫外扫描,其最大吸收波长为295 nm,人工泪液对检测无干扰。
2.1.2 色谱条件 色谱柱:ZORBA×SB-C18柱(5 μm,4.6 mm ×250 mm);流动相:甲醇—水(45∶55);流速:1.0 mL·min-1;检测波长:295 nm;柱温:30℃;进样量:20 μL。
2.1.3 标准线性方程 精密称取105℃干燥至恒重的盐酸川芎嗪对照品10 mg,置于10 mL容量瓶中,用甲醇溶解并稀释至刻度,摇匀,用0.45 μm微孔滤膜过滤,作为储备液备用。精密量取上述储备液,分别用人工泪液稀释成浓度为 5.0、10.0、15.0、20.0、25.0、50.0 mg·L-1的系列溶液,照“2.1.2”项下条件测定峰面积,以峰面积(Y)对浓度(X)进行线性回归,得回归方程为Y=2 566.4X+3 389.4(r=0.999 5),表明盐酸川芎嗪在 5.0 ~50.0 mg·L-1浓度范围内线性关系良好。色谱图见图1,由图1可知,盐酸川芎嗪峰形良好,无杂质峰干扰,保留时间为 7.5 min。
2.1.4 精密度试验 精密吸取浓度为20.0 mg·L-1的盐酸川芎嗪对照品溶液,按“2.1.2”项下方法进样,连续进样5次,记录色谱峰面积后代入回归方程,计算日内精密度,RSD值为0.57%。将样品放置5 d,每天进样测试一次,计算日间精密度,RSD值为1.23%,结果表明仪器精密度良好。
2.1.5 重复性试验 分别精密吸取盐酸川芎嗪储备液适量,配制5份浓度均为20.0 mg·L-1的溶液,按“2.1.2”项下方法进样,分别记录 5 份供试液的峰面积,计算RSD值为1.29%,结果表明该方法重复性良好。
2.1.6 稳定性试验 精密吸取浓度为20.0 mg·L-1的盐酸川芎嗪对照品溶液,按“2.1.2”项下方法进样,对供试液分别在0、2、4、8、24、36、72 h 同上法进行测定以考察其稳定性。结果供试液72 h内峰面积无显着性变化,表明稳定性良好。
2.1.7 加样回收率试验 取实验室自制的盐酸川芎嗪眼用温敏凝胶3份,分别精密加入盐酸川芎嗪对照品适量,制备成供试品溶液,按“2.1.2”项下方法进样测定,计算加样回收率,结果见表1。
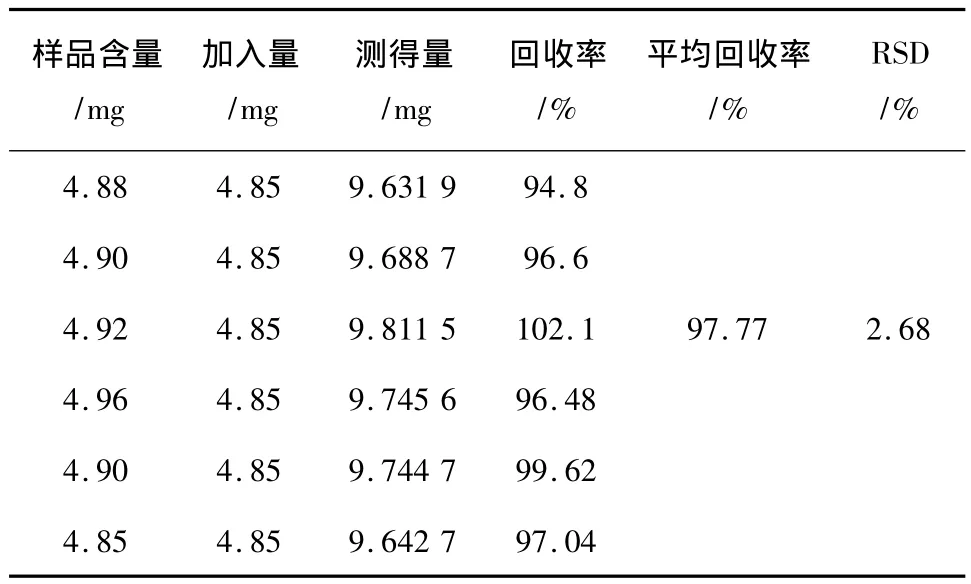
表1 加样回收率试验
2.2 盐酸川芎嗪眼用温敏凝胶的制备 取盐酸川芎嗪20.0 mg,用适量蒸馏水溶解,加入5 mg泊洛沙姆 P188和22.5 mg泊洛沙姆P407,4℃ 低温贮存至泊洛沙姆完全溶解后制成100 mL,所制得凝胶为均匀稍带黏性的澄清溶液[7]。
2.3 温敏凝胶的胶凝温度考察 采用流变学测定温敏凝胶的胶凝温度[8]。量取30.0 g凝胶样品于一定温度水浴的烧杯中,将温度计插入凝胶溶液中,用数显转子黏度计测定,调节速率为100 r·min-1,测定每个温度下的黏度值,缓慢升温,每升高1.0℃平衡5.0 min,绘制黏度随温度的变化曲线,如图2所示。由图2可知,胶凝温度在27℃左右,具有较显着的温度敏感性。
2.4 泪液的稀释对胶凝温度的影响 由于溶液型眼用制剂进入结膜囊内,会被泪液稀释,而结膜囊内泪液的体积约为7 μL,溶液型眼用制剂每滴的体积为 25 ~56 μL,平均约为 40 μL,将凝胶样品与模拟的人工泪液按体积比40∶7混合,同“2.3”项下条件绘制黏度随温度的变化曲线,考察凝胶溶液与人工泪液混合前后胶凝温度的变化,进一步反映凝胶的体内过程,如图2所示。由图2可知,模拟人工泪液稀释后胶凝为33℃,符合眼用制剂的要求。
2.5 凝胶溶蚀实验与药物释放度测定[9-13]采用无膜溶出模型进行试验。在2~5℃温度条件下,将约5 g川芎嗪眼用凝胶加入到预先称重的横截面积为2.54 cm2的圆柱形试管中,将该试管置于34.5℃的水浴振荡器中预热30 min,使溶液完全形成凝胶。加入提前在34.5℃条件下预热的人工泪液2 mL作为释放介质,在一定频率下恒温振荡20 min,立即倒出全部释放介质,并将试管的外表面用滤纸吸干,迅速称重并记录。再将圆柱形试管重新放入振荡器内平衡15 min,补充同温人工泪液适量并继续振荡20 min。如此反复操作直至剩余凝胶量不足10%,相邻时间点的质量差异即为凝胶溶蚀量。计算药物的累积溶蚀百分率,以累积溶蚀百分率对时间作图,绘制累积溶蚀曲线,见图3。由图3可知,随着时间的递增,凝胶的累积溶蚀百分率不断增加。
在考察凝胶的溶蚀动力学的同时考察凝胶中药物的释放,凝胶溶蚀后每次取出的释放介质用流动相稀释成5 mL,经0.45 μm微孔滤膜过滤后测定其中盐酸川芎嗪的含量,计算药物的累积释放百分率,以累积释放百分率对时间作图,绘制累积释放曲线,见图4。由图4可知,随着时间的递增,凝胶的累积释放百分率不断增加,同一时间点凝胶的累积溶蚀百分率大于累积释放百分率,进一步说明了凝胶溶蚀是控制药物释放的主要因素。
2.6 释放模型及释放机制拟合 通过对实验数据进行拟合进而建立适宜的药物模型,是有效模拟和预测药物体外释放行为的必要手段,目前用来评价药物释放特性的常用动力学模型主要有零级释药模型、一级释药模型、Higuchi模型、Ritger-Peppas模型等,将体外释放曲线分别采用上述模型进行拟合,结果见表2。

表2 释放曲线不同模型的拟合结果
式中Mt为t时间药物的累积释放量,M∞为时间趋于∞时的药物的累积释放量,则Mt/M∞为药物在某一时间的累积释放百分率;t为释放时间。
上述拟合方程的的相关系数表明,川芎嗪的释放规律用零级释放动力学模型拟合效果最好。采用Ritger-Peppas模型分析川芎嗪眼用凝胶的释药机理,Ritger-Peppas模型方程为:Mt/M∞=Ktn[或用对数形式表达为ln(Mt/M∞)=nlnt+lnK],K为常数,其大小是表示释放速率大小的重要参数,该常数会随着不同药物或不同释放条件而产生变化;n为释放参数,用来表征药物的释药机理。对于圆柱形制剂,当 n<0.45时,服从 Fick扩散;当 n>0.89时,为骨架溶蚀机制;当 0.45 < n <0.89 时,药物的释放为药物的扩散和骨架溶蚀双重机制。川芎嗪眼用凝胶经拟合后模型方程为:ln(Mt/M∞)=0.753 3lnt-3.645 5,这里释放参数n 为0.753 3,介于0.45和0.89之间,表明其释药是混合性的,即由药物扩散和凝胶溶蚀双重机制控制的。
3 讨论
一般认为,温度敏感型原位凝胶的形成机制是由于温度改变后氢键或疏水作用也随之改变,从而导致聚合物的物理状态发生改变。由于温度的改变相对容易控制,且这种凝胶在体内外均适用,给药部位滞留时间长,生物利用度高[14]。本实验制备的盐酸川芎嗪眼用原位温敏凝胶为均匀稍带黏性的澄清溶液,具有显着的温度敏感性。凝胶溶液的胶凝温度为27℃,经模拟人工泪液稀释后胶凝温度为33℃,符合眼用制剂的要求。
凝胶溶蚀是控制药物释放的主要因素,对药物的溶蚀特征进行研究,可避免药物突释,进而提高药物的安全性。实验室所制备的川芎嗪眼用温敏原位凝胶处方中有泊洛沙姆等较高分子量的聚合物,半透膜的截留作用会阻碍聚合物的扩散,进而影响到药物的释放。而无膜溶出模型由于除去了半透膜的限制,能够更好地模拟人工泪液在振荡条件下所产生类似眨眼的剪切作用,因而更适合于反映在体内泪液不断分泌溶蚀的情况下眼用凝胶剂的释放特性。同时,在实验过程中应保证振荡频率的一致性,以确保在整个实验过程中凝胶溶蚀面积的恒定。
对于原位温敏凝胶,其释药特点包括药物扩散和骨架溶蚀2个过程。本实验由Ritger-Peppas模型方程可知,川芎嗪眼用温敏原位凝胶中药物的释放是由药物扩散和凝胶溶蚀双重机制控制的,其体内角膜的吸收情况有待于进一步研究确定。
[1]叶明花.近五年川芎嗪眼科应用研究概述[J].江西中医学院学报,2006,18(3):78-80.
[2]张丽霞,李静贞,高健生,等.川芎嗪对眼压控制下原发性开角型青光眼患者视功能和视网膜血循环的影响[J].中国中医眼科杂志,2006,16(3):129-132.
[3]宋宗明,崔守信,张德秀.川芎嗪对兔眼高压下视网膜神经节细胞和双极细胞损伤的保护作用[J].第四军医大学学报,2001,22(6):514-517.
[4]高 玮,杨慧芳,王文娟.川芎嗪注射液对糖尿病视网膜病变眼血流动力学的影响[J].中国中医眼科杂志,2012,22(1):23-25.
[5]焦军杰,万 千,李晓鹏,等.川芎嗪对术后眼压正常的原发性慢性闭角型青光眼血流动力学的影响[J].眼科新进展,2012,32(5):476-478.
[6]杨辛欣,李超英.眼部给药系统体内外评价方法的研究进展[J].中国新药杂志,2008,17(13):1101-1104.
[7]张 冕,李瑶瑶.星点设计-效应面法优化盐酸川芎嗪眼用温度敏感型原位凝胶的处方[J].山东化工,2014,43(7):15-18.
[8]苏珊珊,韩 博,陈 文,等.维药溃结安温敏凝胶的制备与其释药性能研究[J].中草药,2015,46(6):840-845.
[9]袁 园,王晓辉,张 莉,等.无膜释放模型考察直肠用温敏型原位凝胶的体外释放情况[J].中国药房,2011,22(29):2750-2752.
[10]郑建灵,陈 鹰,董少华,等.眼用西罗莫司壳聚糖包覆脂质体-原位凝胶的体外释放特性与刺激性[J].中国药师,2012,15(5):609-612.
[11]刘树扬,冯伟红,杜茂波,等.中药复方双秦眼用凝胶体外释药性能[J].中国实验方剂学杂志,2012,18(8):9-11.
[12]王 军,谈 弋,何 文.眼用盐酸倍他洛尔脂质体—原位凝胶的研制及体外释药的研究[J].安徽医药,2013,17(6):921-923.
[13]胡拥军,宋 玲,田鹏程.阿昔洛韦壳聚糖眼用温敏性原位凝胶的研制及其体外释药研究[J].安徽医药,2014,18(1):30-32.
[14]舒 予,李小芳,吴 珊,等.原位凝胶给药系统在中药制剂中的应用研究进展[J].成都中医药大学学报,2014,37(3):120-123.



