石织宏,黄织春
近年来随着生活方式、饮食结构、环境和人口老龄化的改变,虽然胃癌的发病率较前有所下降,但胃癌仍是国内临床极为常见的癌症类型,居所有癌症第二位,且其病死率持续居高不下,严重影响健康[1]。由于胃癌病人早期临床症状并不明显,相当比例的病人一旦确诊常常已至晚期,因此非手术疗法便成为此类病人最为重要的治疗手段。约有25%~30%的胃癌病人会合并人类表皮生长因子受体-2(HER-2)表达阳性,因其在肿瘤浸润、生长和转移中发挥着重要的作用,HER-2高表达往往预示着病人预后不良[2-4]。曲妥珠单抗是对HER-2基因受体具有高度选择性的大分子单克隆抗体,具有抑制HER-2基因表达,从而抑制肿瘤生长和转移的作用[5]。但研究证实,此类病人曲妥珠单抗单药或单纯化疗治疗效果并不显着,因此在化疗方案基础上联合曲妥珠单抗是目前治疗HER-2阳性胃癌最常用的方式[6-7]。伊立替康+顺铂(IP方案)或替吉奥+奥沙利铂(SOX方案)联合曲妥珠单抗是目前临床常用的两种联合治疗方式,目前国内外研究尚缺乏头对头的研究。因此,本文通过分析曲妥珠单抗联合IP方案或SOX方案在晚期HER-2阳性胃癌病人中的效果,旨在为临床实践提供一定的理论基础。
1 资料与方法
1.1一般资料连续性纳入自2015年6月至2017年6月内蒙古医科大学附属医院收治的HER-2阳性晚期胃癌。纳入标准:(1)原发性胃癌;(2)年龄范围为18~75周岁;(3)TNM分期Ⅳ期;(4)免疫组化或荧光原位杂交法检测HER-2表达阳性;(5)卡氏评分(KPS评分)≥60分;(6)预期生存时间≥3个月;(7)无法手术或拒绝手术治疗。排除标准:(1)已行手术治疗;(2)合并其他肿瘤;(3)无可测量病灶;(4)合并严重感染性、免疫性疾病,或合并严重的脏器功能损伤;(5)严重的药物反应化疗无法继续;(6)临床资料缺失、死亡,或拒绝参与此研究。根据以上标准研究期间共纳入58例病人,采用随机数字表法将病人分为曲妥珠单抗联合IP化疗方案组(IP组)和曲妥珠单抗联合SOX化疗方案组(SOX组),每组29例。IP组中男性17例,女性12例,年龄(62.15±13.29)岁,体质量指数(BMI)(28.14±5.43)kg/m2;低分化腺癌14例,中分化腺癌8例,黏液性腺癌6例,印戒细胞癌1例;初治18例,复发再治11例;合并肺部转移5例,腹腔转移12例,肝转移6例,多发转移3例,其余3例未见转移。SOX组中男性19例,女性10例,年龄为(60.22±12.89)岁,BMI为(27.39±7.45)kg/m2;低分化腺癌13例,中分化腺癌7例,黏液性腺癌7例,印戒细胞癌2例;初治20例,复发再治9例;合并肺部转移3例,腹腔淋巴转移11例,肝转移7例,多发转移5例,其余3例未见转移。两组治疗前一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究经内蒙古医科大学附属医院医学伦理委员会批准,病人或近亲属均签署知情同意书。
1.2治疗方法两组病人基础治疗及曲妥珠单抗应用方法一致,曲妥珠单抗(上海罗氏制药有限公司,稀释液批号N3885,分装批号SH0176)使用方法:首剂量8 mg/kg,此后剂量为6 mg/kg,每周第1天静脉滴注。IP组化疗方案使用方法:伊立替康(江苏恒瑞医药股份有限公司,批号180706AF):剂量60 mg/m2,疗程第1天及第8天静脉滴注;顺铂(江苏豪森药业集团有限公司,批号180901):剂量30 mg/m2,疗程第1~3天静脉滴注。SOX组化疗方案使用方法:替吉奥(山东新时代药业有限公司,批号023180608);根据体表面积计算剂量:体表面积<1.25 m2,每次40 mg;1.25 m2≤体表面积<1.50 m2,每次50 mg;体表面积≥1.50 m2,每天60 mg,每天2次(早饭及晚饭后),疗程第1~14天口服;奥沙利铂(江苏恒瑞医药股份有限公司,批号181015AF):剂量130 mg/m2,疗程第1天静脉滴注。两组病人均21 d为一个疗程,均连续治疗两个疗程。
1.3观察指标治疗前及第2个疗程后两组病人均行影像学检查,并参照世界卫生组织(WHO)实体瘤疗效评估标准评估治疗效果,完全缓解(CR):可测量病灶完全消失>1月;部分缓解(PR):可测量病灶瘤体面积缩小≥50%并在时间上超过1月;疾病稳定(SD):无新发病灶或可测量病灶瘤体面积减少<50%或增大<25%;病情进展(PD):可测量病灶瘤体面积增大≥25%或者发现新发病灶。客观有效率(ORR)=(CR+PR)/总例数×100%,疾病控制率(DCR)=(CR+PR+SD) /总例数×100%。第2个疗程结束时两组病人均留取2份静脉血,每份5 mL,低速离心机3 000 r/min离心10 min后保留血清,存放于-80 ℃冰箱,集中采用酶联免疫吸附剂测定法(ELISA法)检测胃癌病人肿瘤标志物水平和新生血管标志物水平,试剂盒购于武汉云克隆生物有限公司,操作步骤参照说明书。所有病人在治疗过程中均每周至少复查1次血常规、肝肾功能、凝血常规等检验,不良反应评估参照WHO毒性反应分级标准,共分为0~Ⅳ级。
2 结果
2.1两组病人治疗后血清肿瘤标志物水平比较两个治疗疗程后,两组病人血清肿瘤标志物癌胚抗原(CEA),糖类蛋白19-9(CA19-9),糖类抗原125(CA125),以及组织多肽特异性抗原(TPS)水平均差异无统计学意义(P>0.05),见表1。
表1 两组治疗后血清肿瘤标志物水平比较
2.2两组病人治疗后血清新生血管标志物水平比较两个治疗疗程后,两组病人血清新生血管标志物内皮生长因子(VEGF)、血管生成素-2(Ang-2)、内皮抑素(ES)、色素上皮衍生因子(PEDF)水平均差异无统计学意义(P>0.05),见表2。
表2 两组治疗后血清新生血管标志物水平比较
2.3两组病人化疗效果比较两个治疗疗程后,SOX组ORR及DCR分别为44.83%和82.76%;IP组ORR及DCR分别为34.48%和69.97%,差异无统计学意义(P>0.05),见表3。
2.4两组病人不良反应比较IP组骨髓抑制和恶心呕吐发生率明显高于SOX组,差异有统计学意义(χ2=4.461、5.836,P=0.035、0.016),其余指标差异无统计学意义(P>0.05),见表4。
3 讨论
HER-2是人类表皮生长因子受体超家族成员之一,正常情况下在人体组织内少量表达,但却在乳腺癌、卵巢癌、胃癌等多种癌症细胞中高度表达,在肿瘤细胞增殖、浸润以及转移过程中发挥着重要的作用[8-11]。研究证实,相当比例胃癌病人会高度表达HER-2蛋白,而作为胃癌的独立危险因素,HER-2高表达往往代表着肿瘤恶性程度越高,预后越差[4,8,12-13]。曲妥珠单抗是美国FDA首先于1998年批准用于晚期乳腺癌转移病人的靶向治疗药物,近年来随着研究的深入,其在HER-2阳性胃癌病人中的临床价值越来越受到医务人员的重视[14-17]。
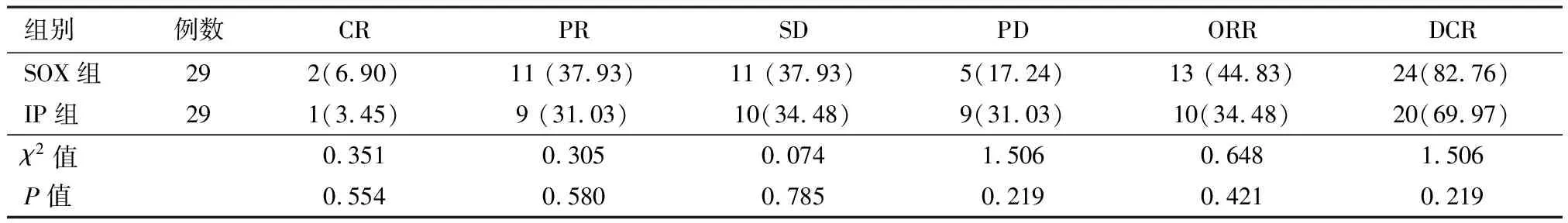
表3 两组病人化疗效果比较/例(%)
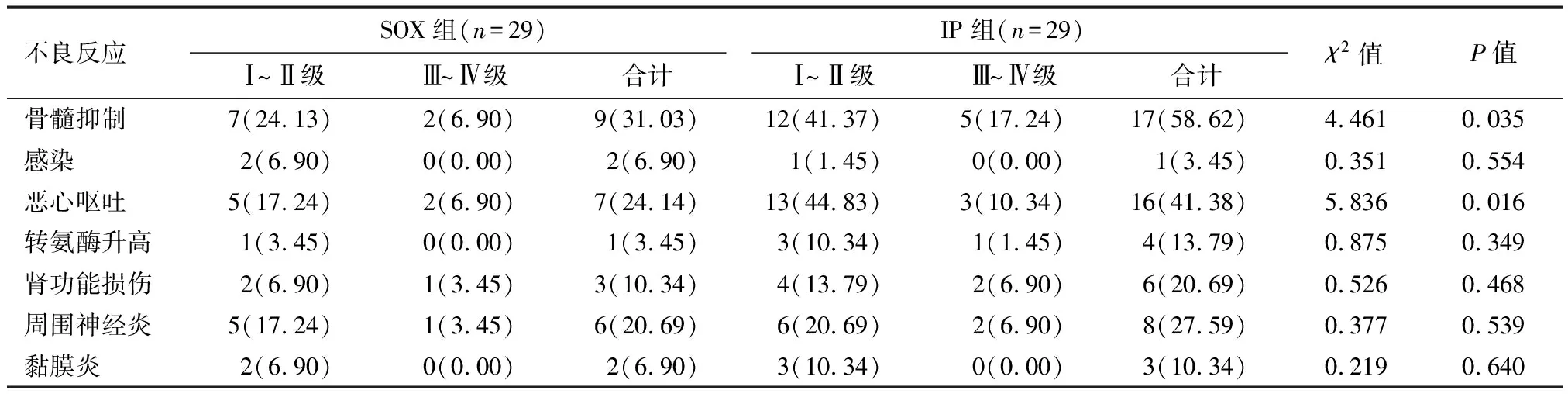
表4 两组病人不良反应比较/例(%)
但大量的研究证实,针对HER-2阳性胃癌,无论是单独化疗或是曲妥珠单抗单药靶向治疗,其效果均远不及曲妥珠单抗联合化疗治疗模式[6,15,18]。但目前曲妥珠单抗联合何种化疗方案尚无令人信服的结论。IP方案和SOX方案是目前临床常用的胃癌化疗方案,本文通过分析两组方案的临床治疗效果,以期为临床更好地选择曲妥珠单抗联合化疗方案的应用提供一定的理论基础。
本研究中,在治疗效果方面,SOX组和IP组差异无统计学意义(P>0.05)。在治疗后血清肿瘤标志物和新生血管标志物水平比较中,两组亦差异无统计学意义(P>0.05);但在安全性方面,IP组恶心呕吐和骨髓抑制不良反应发生率均显着高于SOX组,差异有统计学意义(P<0.05)。研究结果提示,曲妥珠单抗联合SOX化疗方案与曲妥珠单抗联合IP化疗方案疗效相当,但前者安全性可能更好。这可能是由于替吉奥是在替加氟的基础上增加吉美嘧啶,以减少有效成分氟尿嘧啶的降解来增加抗肿瘤效果,同时在此基础上再增加奥替拉西钾可减少病人消化道不良反应,从而保护病人胃肠道功能[19]。而伊立替康是拓扑异构酶I的抑制剂,其特异性作用于细胞分裂S期,阻断DNA合成和复制,从而起到抗肿瘤效果,大量的临床研究发现其最为常见的不良反应多为胃肠道反应,且程度更为严重[20-21]。此外奥沙利铂作为第三类铂类化疗药物,相比于第一代铂类药物顺铂在提高疗效的同时,其骨髓抑制、耳毒性、肾毒性等不良反应的发生率更少[22-23]。
综上所述,曲妥珠单抗联合SOX化疗方案或IP方案在HER-2阳性晚期胃癌病人中疗效相当,但SOX方案不良反应发生率较少,值得临床推广。但本研究为单中心、小样本研究,证据等级较低,且晚期胃癌预后极差,目前针对此类病人尚无公认的标准化疗方案,因此选择何种化疗方案与曲妥单抗联合应用,可以在改善治疗效果的同时,又能提高用药安全性,仍需进一步深入探讨。



