李志强,史军卿,王冠达,王雅靖,夏春辉
作者单位:华北理工大学附属医院重症医学科,河北 唐山 063000
围手术期液体治疗的剂量和类型对术后病死率和并发症发生率有至关重要的影响,因此越来越受到关注[1-2]。在大手术、创伤、休克等许多临床情况下液体复苏通常是治疗成败的关键,其原理在于快速补充有效循环血容量,维持内环境稳定,从而保证组织器官灌注及氧合,防止继发性器官功能障碍的发生[3]。
外科手术病人的液体管理通常由容量状态、液体维持量、第三间隙损失量来决定[4],然而,血流动力学指标变化(血管扩张、心肌抑制)和全身炎症改变(血管通透性增加)也是影响液体治疗的因素[5-6]。另外,最新研究表明液体治疗的量、类型和时机可能会影响手术病人的临床预后。比如,人工合成胶体可能增加急性肾损伤的风险[7-9],在脓毒症早期采用限制性液体治疗可能改善病人预后[10-11],对急性肺损伤病人延迟液体治疗可能增加机械通气治疗时间[12],此外,连续液体正平衡可能增加病人术后并发症发生率和病死率[13-15]。因此,本研究的目的在于评估围手术期液体治疗的剂量和类型对择期腹部手术病人术后ICU住院时间、病死率、术后并发症发生率的影响。
1 资料与方法
1.1 纳排标准和方法属性(1)纳入标准:2014年1月1日至2016年1月1日接受择期腹部手术后入住在华北理工大学附属医院ICU>48 h的病人。
(2)排除标准:①年龄<18周岁;②ASA>Ⅲ级;③单独或联合接受骨科、胸外科、心脏外科、神经外科、血管外科、整形外科和产科手术;④创伤病人;⑤≥2次入住ICU的病人,包括二次手术病人;⑥实施姑息手术的病人;⑦术后病人或代理人要求限制性治疗的病人。
(3)试验方法:病例对照研究。
(4)伦理问题:本研究符合《世界医学协会赫尔辛基宣言》相关要求。病人或其近亲属对治疗知情同意。
1.2 液体类型的定义晶体液包括0.9%生理盐水、乳酸林格液和平衡盐溶液;胶体液包括人工胶体(低分子右旋糖酐、羟乙基淀粉、琥珀酰明胶)和血液制品(人血清蛋白、血浆)。因临床实践中不以红细胞、血小板或冷沉淀作为液体治疗,所以上述血液制品的输注量计入到每日总液体入量中,但不列入本课题研究的液体类型中。
1.3 资料收集采用纸质的统一的数据填写表格收集以下数据:人口学数据,包括年龄和性别,体质量,基础疾病,围手术期急性生理与慢性疾病评估(Acute Physiology and Chronic Health Evaluation,APACHE-Ⅱ),手术名称,手术时间,术中是否使用升压药物。液体治疗:术中液体入量、术中液体出量。术后(最长记录到转出ICU或术后第5天)液体入量和输液类型。计算每天液体平衡量,累计液体平衡量,并计算累计晶体-胶体容积比。临床结局指标,主要结局指标包括ICU病死率、住院病死率,次要结局指标包括术后并发症发生率,例如急性肾损伤(KDIGO标准),需肾脏替代治疗;心血管并发症(包括急性心力衰竭、心肌梗死和心律失常);呼吸系统并发症(包括呼吸衰竭、肺水肿、肺炎和胸腔积液);伤口感染;胃肠道并发症(包括肠梗阻和肠瘘);ICU和总住院时间。
1.4 统计学方法按术后ICU滞留是否超过5 d为界,分为延时ICU住院组(>5 d)和非ICU延时住院组(≤5 d)[16]。
采用SPSS 17.0进行数据分析。正态分布连续变量采用±s表示,偏态分布则行对数转化。采用两因素重复测量方差分析、单因素方差分析或Mann-Whitney秩检验;分类变量采用例(%)表示,比较采用χ2检验或Fisher精确概率法;采用非条件logistic回归,以病人是否延时ICU住院为因变量,将单因素分析中P<0.05的变量作为自变量,筛查影响术后病人延时ICU住院的危险因素并建立风险预测模型;应用受试者工作特征曲线下面积和Hosmer-Lemeshow拟合优度检验判断模型的辨别力和校准度。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料等各项指标的比较该研究总共纳入186例病人,年龄(68.10±13.50)岁,其中男性占55.38%。围手术期APACHE-Ⅱ评分平均值为(15.30±2.91),胃肠道肿瘤切除术占所有手术类型的60.75%,其中胃癌30例,结肠癌56例,直肠癌18例,肝癌9例。所有纳入研究的病人术后均转入ICU进一步治疗,其中延时ICU住院的病人有72例,占所有病人的38.71%。通过单因素分析,延时ICU住院组与非延时ICU住院组相比在术中升压药物使用率、术中输血率、术后APACHE-Ⅱ评分、术后氧合指数、术后血乳酸水平等指标均差异有统计学意义(P<0.05),见表1。在手术类型及麻醉方式中差异无统计学意义,见表2。从术中到术后48 h液体出入量差异有统计学意义,见表3。
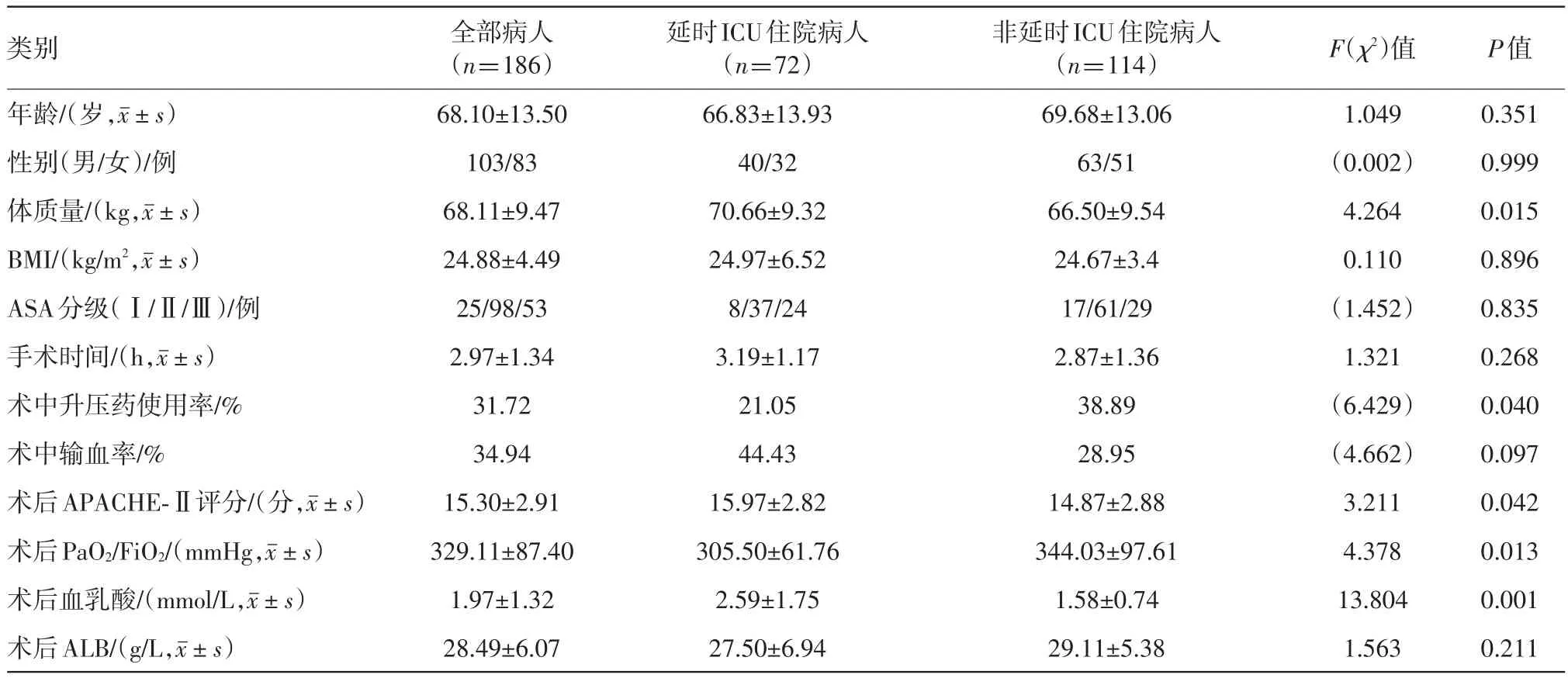
表1 接受择期腹部手术病人一般资料比较
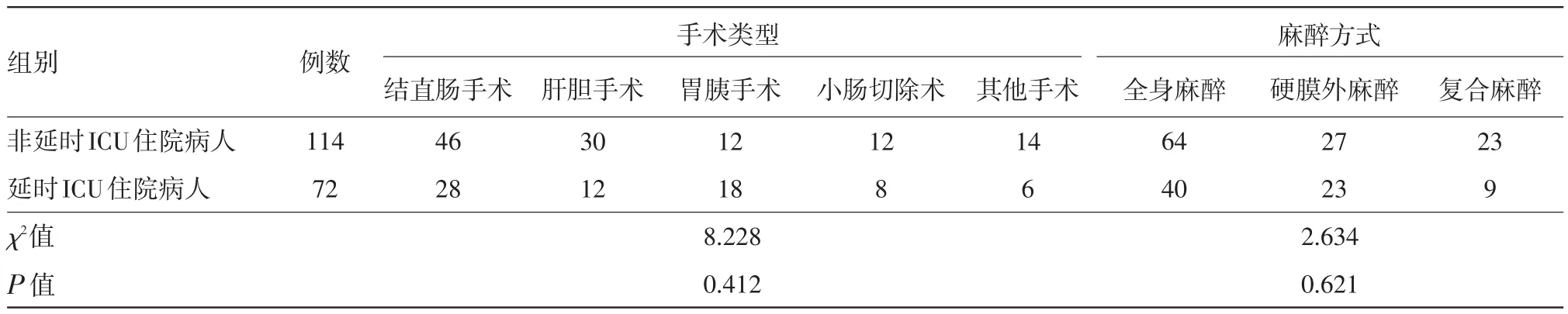
表2 接受择期腹部手术病人手术类型及麻醉方式分组比较/例
表3接受择期腹部手术病人围手术期液体出入量分组比较/(mL,±s)
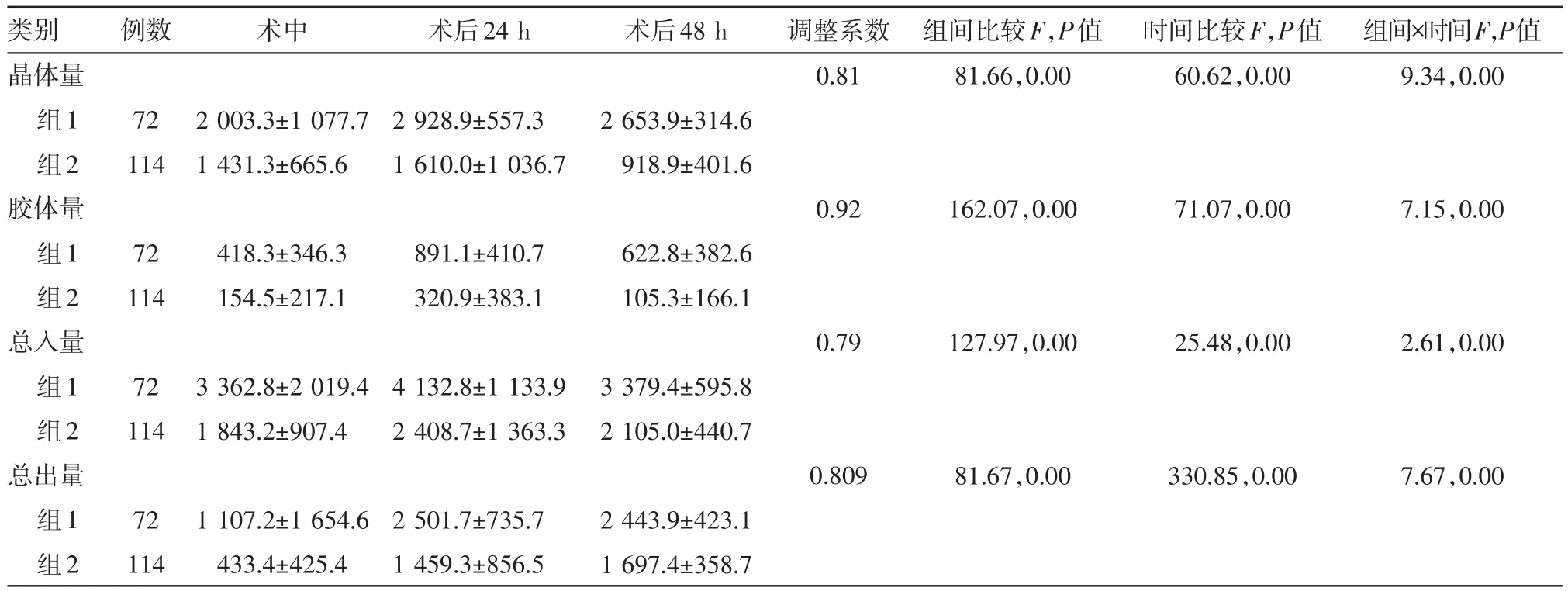
表3接受择期腹部手术病人围手术期液体出入量分组比较/(mL,±s)
注:组别1为延时ICU住院组;组别2为非延时ICU住院组
类别晶体量组1组2胶体量组1组2总入量组1组2总出量组1组2例数72 114 72 114 72 114 72 114术中2 003.3±1 077.7 1 431.3±665.6 418.3±346.3 154.5±217.1 3 362.8±2 019.4 1 843.2±907.4 1 107.2±1 654.6 433.4±425.4术后24 h 2 928.9±557.3 1 610.0±1 036.7 891.1±410.7 320.9±383.1 4 132.8±1 133.9 2 408.7±1 363.3 2 501.7±735.7 1 459.3±856.5术后48 h 2 653.9±314.6 918.9±401.6 622.8±382.6 105.3±166.1 3 379.4±595.8 2 105.0±440.7 2 443.9±423.1 1 697.4±358.7调整系数0.81 0.92 0.79 0.809组间比较F,P值81.66,0.00 162.07,0.00 127.97,0.00 81.67,0.00时间比较F,P值60.62,0.00 71.07,0.00 25.48,0.00 330.85,0.00组间×时间F,P值9.34,0.00 7.15,0.00 2.61,0.00 7.67,0.00
2.2 延时ICU住院的影响因素分析将单因素分析中筛选出的术中液体平衡量、术后5 d累计液体平衡量、术后5 d累计胶体-晶体容积比等7项可疑因素作为自变量,以是否延时ICU住院作为应变量(非延时ICU住院=0;延时ICU住院=1),纳入logistic二项回归分析模型中,采用逐步向前剔除法进行筛选(α=0.05),最终纳入模型的变量是术中液体平衡量、术后5 d累计液体平衡量、术后APACHE-Ⅱ评分、术后血乳酸水平及氧合指数,见表4。
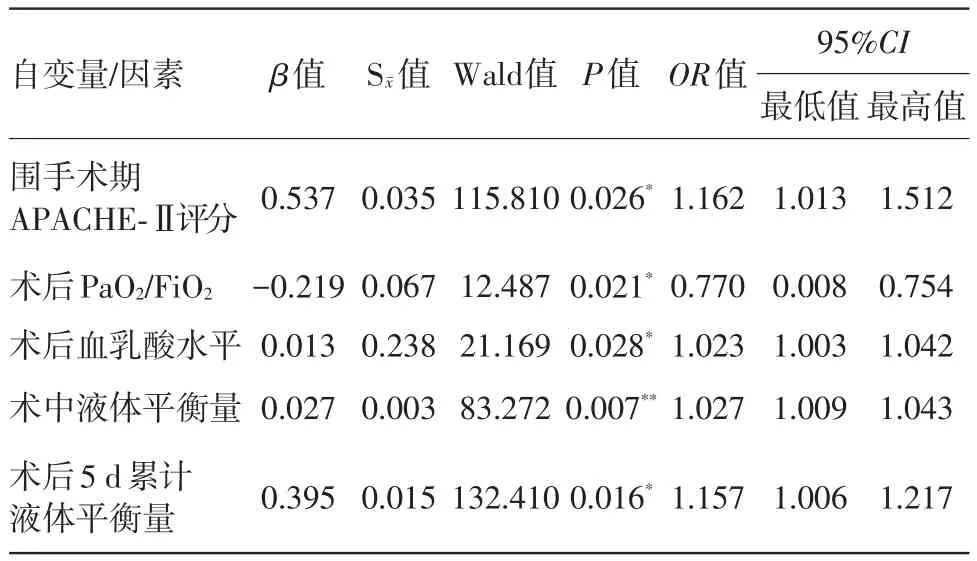
表4 接受择期腹部手术病人延时ICU住院的独立危险因素
2.3 各指标/参数的ROC分析对术中液体平衡量进行灵敏度及特异度分析,绘制受试者工作特征曲线(ROC曲线),曲线下面积AUC=0.785(0.720,0.859),P<0.001,说明术中液体正平衡量可以预测术后延时ICU住院,影响病人术后ICU住院时间的术中液体平衡量临界值是2 000 mL(灵敏度=0.611,特异度=0.816),见图1A。
对术后累积液体正平衡量进行灵敏度和特异度分析,绘制ROC曲线,曲线下面积AUC=0.716(0.638,0.795),P<0.001,说明术后累积液体正平衡量可以用来预测延时ICU住院,影响病人术后延时ICU住院的术后5d累计液体平衡量临界值是5 800 mL(灵敏度=0.389,特异度=0.895),见图1B。
对术后APACHE-Ⅱ评分进行灵敏度和特异度分析,绘制ROC曲线,曲线下面积AUC=0.605(0.523,0.687),P<0.001,说明术后APACHE-Ⅱ评分可以预测术后是否延时ICU住院,影响病人术后延时ICU住院的APACHE-Ⅱ评分临界值是17.5(灵敏度=0.333,特异度=0.799),见图1C。
对术后血乳酸浓度进行灵敏度和特异度分析,绘制ROC曲线,曲线下面积AUC=0.713(0.638,0.788),P<0.001,说明术后血乳酸浓度可以预测延时ICU住院,影响病人术后延时ICU住院的血乳酸浓度临界值是2.4 mmol/L(灵敏度=0.389,特异度=0.868),见图1D。
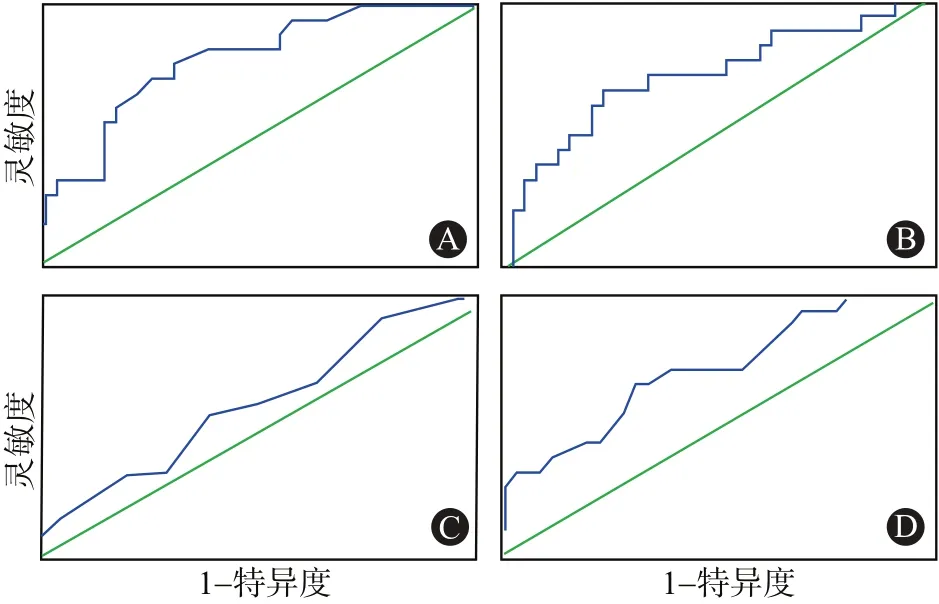
图1 影响接受择期腹部手术病人术后ICU住院时间ROC曲线(A为术中液体平衡量预测延时ICU住院的ROC曲线;B为术后液体累积平衡量预测延时ICU住院的ROC曲线;C为术后APACHE-Ⅱ预测延迟ICU住院的ROC曲线;D为术后血乳酸浓度预测延迟ICU住院的ROC曲线)
总之,在所有的独立影响因素中术中液体正平衡量的ROC曲线下面积最大,曲线最靠近坐标左上角,说明术中液体正平衡量预测术后是否延时ICU住院最可靠。当病人术中液体正平衡量>2 000 mL时术后病死率与其他病人相比明显升高(18.46%比5.78%,P<0.01)。
2.4 术后结果分析对术后结果分析显示,当病人术中液体正平衡量>2 000 mL时,术后机械通气时间[(5.25±3.18)d比(2.62±3.26)d,P<0.001]、术后ICU住院时间[(3.05±2.57)d比(7.05±4.16)d,P<0.001]及术后住院时间[(16.37±4.91)d比(12.85±5.37)d,P<0.001]明显延长;病人术后心血管并发症(32.31%比19.83%,P<0.05)、呼吸系统并发症(31.27%比10.74%,P<0.001)、消化系统并发症(26.15%比12.40%,P<0.05)及术后局部或全身感染(29.23%比14.05%,P<0.05)发生率也明显升高;而术后肾功能不全及神经系统并发症的发生率以及术后24 h尿量在两组之间均差异无统计学意义,见表5。
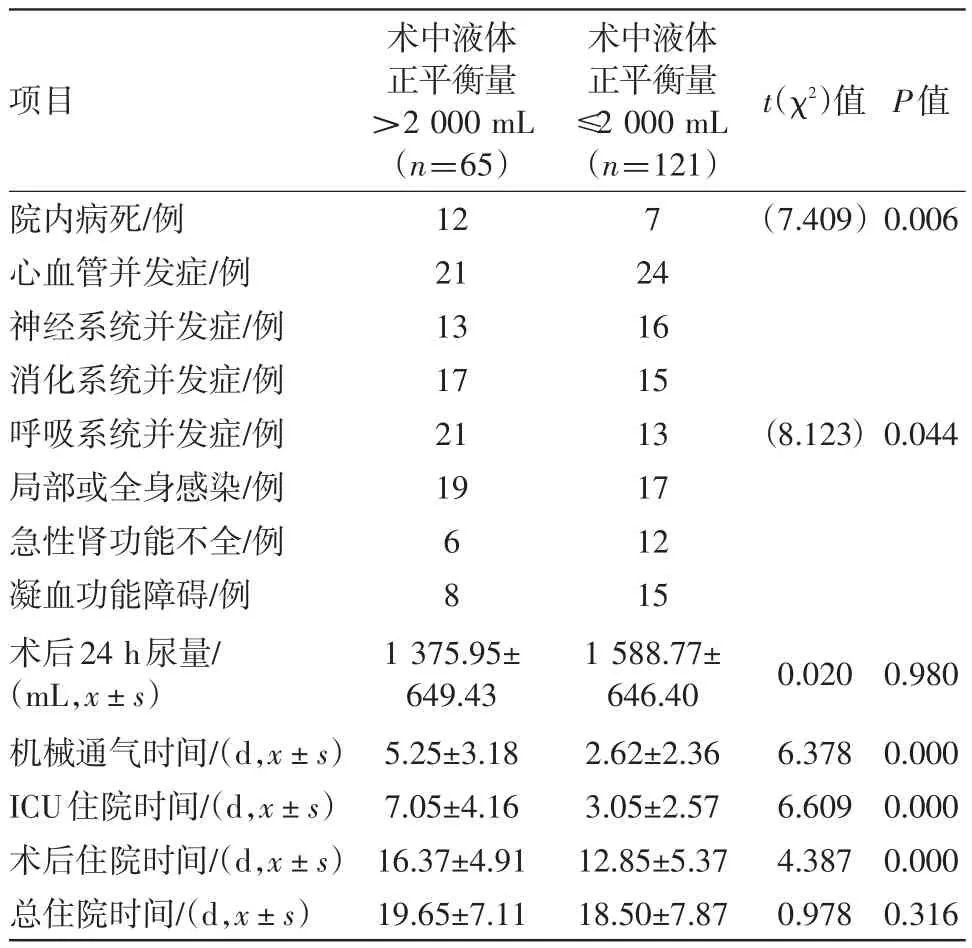
表5 术中液体正平衡过量与非过量对接受择期腹部手术病人临床预后的影响
3 讨论
本研究表明择期腹部手术病人术后ICU病死率、住院病死率、术后延时ICU住院、术后并发症(心血管系统、呼吸系统、消化系统)发生率以及院内局部或全身感染发生率均与围手术期液体正平衡量明显相关,而与液体治疗的类型无明显关联。同时,纳入研究的对象均为择期开放性腹部手术高危病人,术后都需要转入ICU进一步治疗,APACHE-Ⅱ评分为(15.30±2.91),所以该研究的结果对择期高危手术病人围手术期液体管理有一定指导意义。
当前,在临床实践中对于围手术期液体治疗策略仍存在争议。在比较了19篇关于围手术期液体治疗的RCT研究后,Kern和Shoemaker[17]指出开放性液体治疗策略通过早期优化血流动力学指标能够明显改善手术病人临床预后。
然而,随着研究的深入,关于围手术期开放性液体治疗带来的不良后果在临床实践中也越来越受到关注[18]。在开放性液体治疗中最容易出现的情况就是液体过负荷。而液体过负荷对于呼吸系统影响尤为明显,可能会引起急性肺水肿,阻碍气体交换,延长术后机械通气时间,进而使病人院内肺感染的风险也大大增加。对于消化系统,术中机械性刺激加围手术期液体过负荷可能会引起肠壁水肿,氧输送减少,延长胃肠道功能恢复,增加术后肠梗阻、吻合口瘘以及延迟性胃排空的发生[19]。总之,液体过负荷可能会引起组织或间质水肿,阻碍毛细血管血流及淋巴管引流,影响氧气及代谢产物的运输,从而加剧器官功能障碍的进程。该效应对于腹腔实质性脏器(肝脏、肾脏)的影响更为显着,因为这些脏器结构致密,组织水肿会使脏器内压力骤升而血流量会显着降低,从而影响脏器功能[20]。有研究指出,如果围手术期积极液体正平衡使体质量增加5~10%,危重病人发生器官功能障碍以及不良临床预后的风险也会大大增加。此外,该研究也证实术后24 h液体正平衡量与尿量无正相关,对术后肾功能没有任何益处[21]。
目前研究表明,围手术期输注更多的液体与术后心血管并发症的发生率也呈正相关。其机制可能在于围手术期输液量一旦超过代偿范围,Heart-Starling曲线就无明显位移,而心脏负荷和耗氧量却会急剧增加;心肌细胞水肿可能会使心室功能进一步恶化,导致氧供降低和心脏传导障碍[22],从而使术后心血管并发症的风险大大增加,这与我们的研究结果相符,对于高危择期开放腹部手术病人术中液体正平衡量>2 000 mL时,病人术后心血管并发症发生率(32.31%比19.83%,P<0.05)会明显升高。
我们的研究结果与Boland等[23]的研究也相似,围手术期容量过负荷与术后院内病死率、并发症发生率、延时ICU住院密切相关,但是围手术期最佳液体治疗量、时机及种类仍未明确。为了制定合理的围手术期液体治疗策略,近年来临床实践中做了大量关于液体治疗的随机对照试验。然而,由于缺乏“开放性”和“限制性”的标准定义,每个实验之间液体治疗时采用的标准、结局指标等都不一样,结果之间也差异较大。这些随机对照研究为排除临床混杂因素,纳入的大部分研究对象是身体状况良好、术前ASA评分较低的病人,对于高危手术病人的液体治疗研究甚少,因此,我们的研究对于指导高危择期手术病人围手术期液体治疗有一定的意义。
除了“干”与“湿”在临床实践中存在争论外,液体治疗时晶体溶液与胶体溶液的选择也存在争议[24]。在我们的研究中没有对晶体或者胶体的种类进行亚组分析,最终结果显示延时ICU住院的病人与其他病人相比术中胶体用量[(418.33±346.30)mL比(154.47±217.09)mL,P<0.001]明显增多,但是进行logistic二项回归分析显示术中胶体用量并不是影响病人术后延迟ICU住院的独立危险因素[OR=0.998,95%CI(0.995~1.008),P=0.411]。由于该研究为回顾性分析,术后病人ICU出院的标准可能存在一定的偏差,所以该结果需要大样本RCT研究进一步予以验证;在该研究中所有病人均有围手术期凝血四项的监测数据,但是液体治疗的剂量和种类相互混杂,所以暂不能明确术中胶体对术后凝血指标的影响。
综上所述,术中液体过负荷会增加病人术后ICU病死率及住院病死率,延长病人术后机械通气时间、术后ICU住院时间及术后住院时间,增加病人术后并发症(心血管、呼吸系统、消化系统)发生率,而液体治疗的类型对高危手术病人临床预后无明显影响,对凝血功能的影响暂不能确定。



