王蕊,王芹,杜文斌,张慧,马赛,胥爱文,汪佳,安峰
作者单位:1河北北方学院附属第一医院口腔科,河北 张家口075000;
2河北北方学院附属第二医院口腔科,河北 张家口075100
口腔扁平苔癣(OLP)为黏膜异常角化伴浅表性慢性炎性疾病,多发于口腔黏膜,临床多表现为局部溃疡、糜烂、疼痛及白色花纹病损等症状[1]。研究证明,OLP与机体免疫等复杂因素关系密切。因其病理病机尚不明确,临床常难以采取针对性治疗,临床疗效不尽满意,且极易复发,迁延不愈[2]。OLP病人长期存在的糜烂型病损存在恶变倾向,若无法获得有效治疗,部分病人可最终发展为口腔癌[3]。研究证明,炎症反应是推动糜烂型OLP发生发展的重要因素,控制炎症反应有助于糜烂型OLP病人的康复[4]。在糜烂型OLP恶变进程中,部分蛋白会发生一定的变化,探讨这些差异蛋白在治疗前后的表达变化,对于遏制糜烂型OLP的恶性发展,准确评价治疗方法的有效性具有重要意义[5]。本研究将硫酸羟氯喹口服联合康复新液、曲安奈德混合液含漱应用于糜烂型OLP的临床治疗,在评价其疗效的同时探究其对病人血清差异蛋白、白细胞介素-12(IL-12)、白细胞介素-17(IL-17)的影响。
1 资料与方法
1.1一般资料采用单盲法前瞻性研究,选取2018年1月至2019年6月于河北北方学院附属第一医院口腔科门诊就诊的糜烂型OLP病人100例,男42例(42.00%),女58例(58.00%);年龄(54.95±6.08)岁,范围为36~76岁;体质量指数(23.75±2.43)kg/m2,范围为20.62~26.92 kg/m2;病程(2.28±0.25)年,范围为3个月至6年。纳入标准:经病理证明,且符合《口腔扁平苔癣诊疗指南(试行)》[6]中糜烂型OLP诊断标准者;知情同意者。排除标准:合并其他口腔黏膜疾病者;1月内曾应用抗生素者;3月内曾应用免疫制剂者;重症系统性疾病者;其他因素导致苔癣样反应者;免疫性疾病病人;3月内吸烟、嗜酒者;合并恶性肿瘤者;肝肾功能异常者;妊娠、哺乳期女性;依从性差者。依照随机数字表法将上述100例糜烂型OLP病人分为试验组(n=50)与对照组(n=50),两组基线资料差异无统计学意义(P>0.05)。见表1。本研究经河北北方学院附属第一医院伦理委员会审核批准(201700102)。

表1 两组糜烂型口腔扁平苔癣病人基线资料比较
1.2方法
1.2.1 对照组 对照组给予硫酸羟氯喹(上海中西制药有限公司,生产批号201710080211,国药准字H19990263)口服。硫酸羟氯喹200 mg,口服,2次/天。连续治疗4周。
1.2.2 试验组 试验组给予硫酸羟氯喹(同上)口服联合康复新液(四川好医生攀西药业有限责任公司,生产批号201709131124,国药准字Z51021834)、曲安奈德(广东恒诚制药有限公司,生产批号201710220508,国药准字H10930202)混合液含漱治疗。硫酸羟氯喹用量用法同对照组。治疗期间每周检查视野缺失、视网膜、角膜、睫状体调节等眼睛反应,若发现异常需立即停药。康复新液、曲安奈德混合液含漱治疗。康复新液、曲安奈德(1∶1)混合液10 mL含漱5 min吐掉,3次/天。连续治疗4周。应用混合液后30 min禁止进食、饮水。
1.3观察指标治疗前后,观察两组糜烂面积、疼痛程度;血清人抗凝血酶-Ⅲ(AT-Ⅲ)、免疫球蛋白M(IgM)、锌α2糖蛋白(ZAG)等差异蛋白水平;血清IL-12、IL-17等炎性因子水平;不良反应。以有刻度标识的牙周探针测量糜烂面积,先测量糜烂部位最大径,然后再测量与前次垂直的最大径,两次最大径之积,即为糜烂面积。若糜烂面为多处,则逐个测量后取其和。疼痛程度以视觉模拟评分法(VAS)进行评价,满分10分,得分越低,疼痛程度越轻;以酶联免疫吸附测定(ELISA)检测血清AT-Ⅲ、IgM、ZAG、IL-12、IL-17水平。因硫酸羟氯喹可导致视网膜或视野改变,故对病人进行眼科检查;并观察病人是否出现味觉改变、胃肠不适等不良反应。
1.4疗效评价标准本标准依据《口腔扁平苔癣诊疗指南(试行)》[6]制定。显效:白色条纹轻微或无,充血、糜烂及疼痛完全消失;有效:白色条纹数量减少,充血、糜烂及疼痛程度减轻;无效:白色条纹数量未见减少或增加,充血、糜烂及疼痛程度未见减轻或加重。总有效=显效+有效。
1.5统计学方法采用SPSS 19.0统计软件分析,定量资料以表示,组内比较行配对t检验、组间比较行两独立样本t检验;定性资料以例数结合率描述,率的组间比较行χ2检验。检验水准α=0.05。
2 结果
2.1两组糜烂面积、VAS评分比较治疗前,两组糜烂面积、VAS评分均差异无统计学意义(P>0.05);治疗后,两组糜烂面积、VAS评分均减小(P<0.05);治疗后,试验组糜烂面积、VAS评分均小于对照组(P<0.05)。见表2。
表2 两组糜烂型口腔扁平苔癣病人糜烂面积、疼痛视觉模拟评分法(VAS)评分比较/

表2 两组糜烂型口腔扁平苔癣病人糜烂面积、疼痛视觉模拟评分法(VAS)评分比较/
组别对照组治疗前治疗后t值P值试验组治疗前治疗后t值P值两组比较t,P值治疗前治疗后例数50糜烂面积/mm2VAS评分/分48.72±5.00 6.53±0.77 58.971<0.001 8.14±0.81 0.80±0.10 63.593<0.001 50 48.76±5.03 5.97±0.72 59.546<0.001 8.19±0.84 0.72±0.09 62.524<0.001 0.040,0.968 3.756,<0.001 0.303,0.763 4.2047,<0.001
2.2两组AT-Ⅲ、IgM、ZAG水平比较治疗前,两组血清AT-Ⅲ、IgM、ZAG水平均差异无统计学意义(P>0.05);治疗后,两组血清AT-Ⅲ、IgM、ZAG水平均降低(P<0.05);治疗后,试验组血清AT-Ⅲ、IgM、ZAG水平均小于对照组(P<0.05)。见表3。
2.3两组血清IL-12、IL-17水平比较治疗前,两组血清IL-12、IL-17水平均差异无统计学意义(P>0.05);治疗后,两组血清IL-12、IL-17水平均降低(P<0.05);治疗后,试验组血清IL-12、IL-17水平均小于对照组(P<0.05)。见表4。
表3 两组糜烂型口腔扁平苔癣病人血清人抗凝血酶-Ⅲ(AT-Ⅲ)、免疫球蛋白M(IgM)、锌α2糖蛋白(ZAG)水平比较/
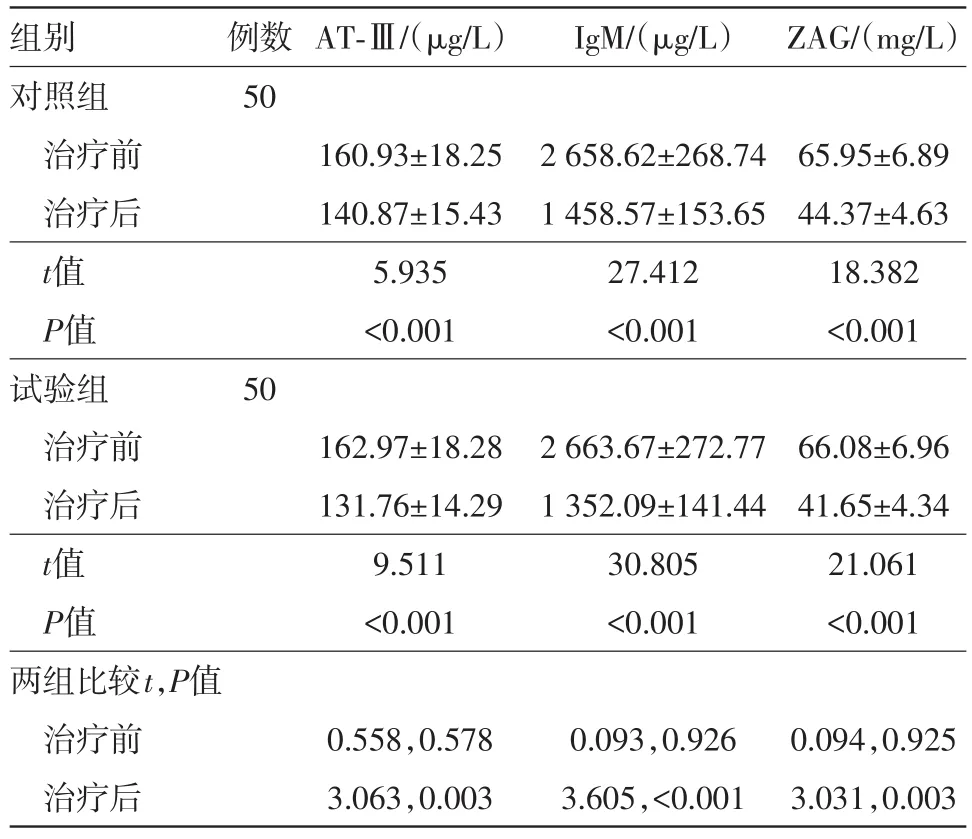
表3 两组糜烂型口腔扁平苔癣病人血清人抗凝血酶-Ⅲ(AT-Ⅲ)、免疫球蛋白M(IgM)、锌α2糖蛋白(ZAG)水平比较/
AT-Ⅲ/(µg/L)IgM/(µg/L)ZAG/(mg/L)65.95±6.89 44.37±4.63 18.382<0.001例数50 160.93±18.25 140.87±15.43 5.935<0.001 2 658.62±268.74 1 458.57±153.65 27.412<0.001 50组别对照组治疗前治疗后t值P值试验组治疗前治疗后t值P值两组比较t,P值治疗前治疗后162.97±18.28 131.76±14.29 9.511<0.001 2 663.67±272.77 1 352.09±141.44 30.805<0.001 66.08±6.96 41.65±4.34 21.061<0.001 0.094,0.925 3.031,0.003 0.558,0.578 3.063,0.003 0.093,0.926 3.605,<0.001
表4 两组糜烂型口腔扁平苔癣病人血清白细胞介素-12(IL-12)、白细胞介素-17(IL-17)水平比较/(ng/L,)
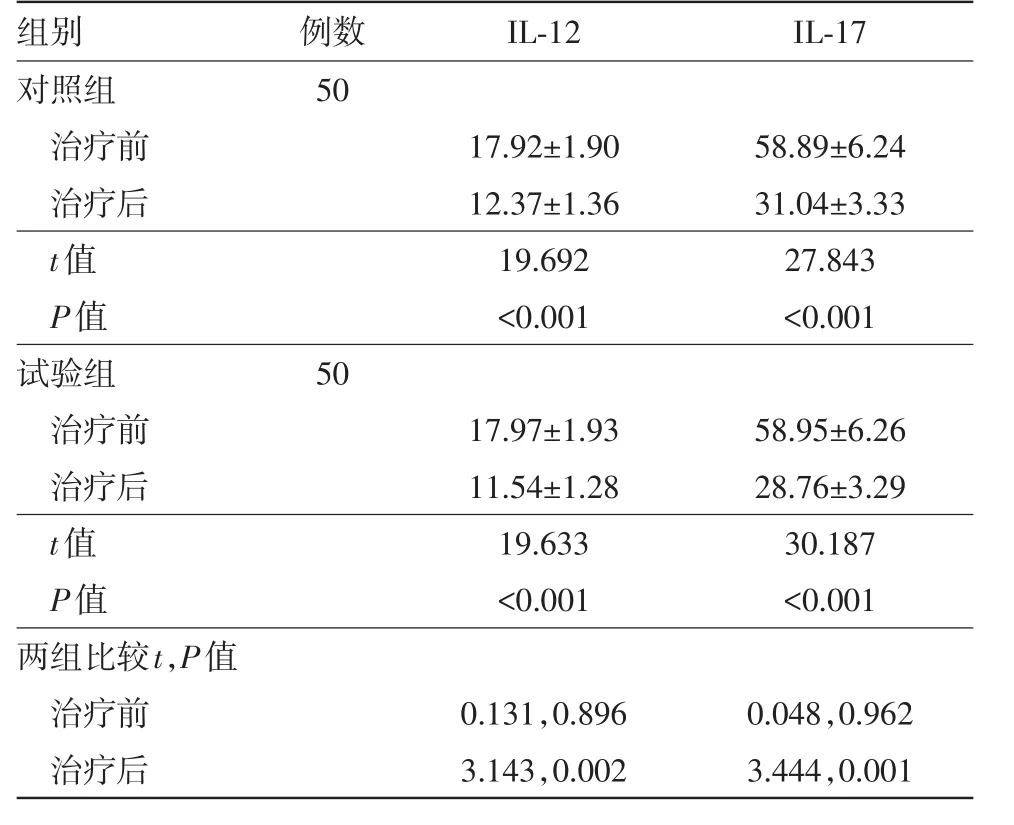
表4 两组糜烂型口腔扁平苔癣病人血清白细胞介素-12(IL-12)、白细胞介素-17(IL-17)水平比较/(ng/L,)
0.048,0.962 3.444,0.001组别对照组治疗前治疗后t值P值试验组治疗前治疗后t值P值两组比较t,P值治疗前治疗后例数50 IL-12IL-17 17.92±1.90 12.37±1.36 19.692<0.001 58.89±6.24 31.04±3.33 27.843<0.001 50 17.97±1.93 11.54±1.28 19.633<0.001 58.95±6.26 28.76±3.29 30.187<0.001 0.131,0.896 3.143,0.002
2.4两组临床疗效比较试验组总有效率(94.00%)大于对照组(76.00%)(P<0.05)。见表5。
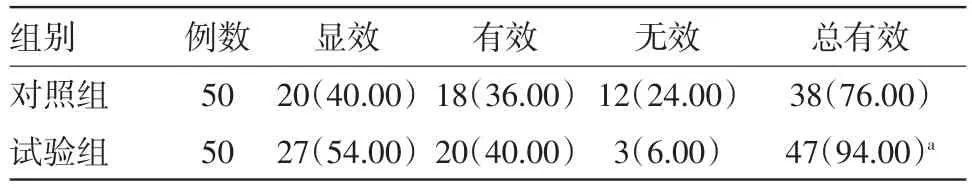
表5 两组糜烂型口腔扁平苔癣病人临床疗效比较/例(%)
2.5两组不良反应比较两组不良反应发生率差异无统计学意义(P>0.05)。见表6。
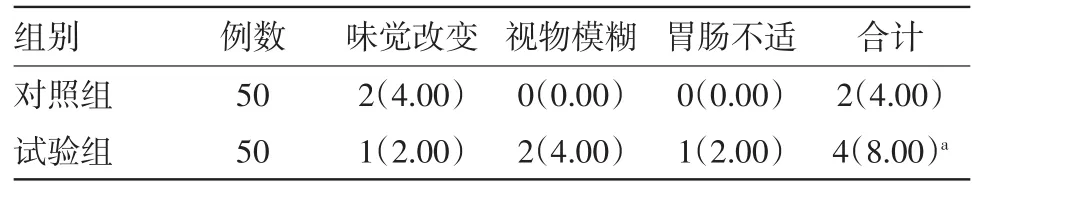
表6 两组糜烂型口腔扁平苔癣病人不良反应比较/例(%)
3 讨论
糜烂型OLP为常见口腔黏膜慢性疾病,临床治疗较为困难。康复新液为生物制剂,具有养阴生肌、通利血脉等功效。资料显示,康复新液含有多肽、促生长因子等多种有效成分,可促进局部新生血管形成,改善微循环,为创面修复创造物质、能量基础[7]。康复新液含黏糖氨酸,能够改善机体免疫,缓解炎症反应[8]。康复新液可促进局部表达TNF-β、成纤维细胞生长因子表达,诱导黏膜修复因子生成,促进糜烂创面愈合。康复新液可激活SOD,促进清除自由基,加快创面合成细胞外基质,促进生成新生肉芽组织,加快糜烂创面愈合速度[9]。曲安奈德为糖皮质激素,具有较强的抗变态反应及抗炎作用,可有效抑制炎性因子生成,降低细胞膜及毛细血管通透性,促进局部微循环,消除水肿[10]。曲安奈德可经抑制内皮细胞及内皮消除颗粒功能,抑制免疫反应[11]。康复新液、曲安奈德混合液含漱可使药物直接作用于糜烂创面,促进黏膜恢复。硫酸羟氯喹为免疫抑制剂,可经提高细胞溶酶体膜的稳定性,抑制溶酶体分泌,干预白细胞趋化,抑制抗原结合抗体及细胞复制,缓解细胞损伤,消除炎症反应[12]。硫酸羟氯喹可抑制生成组胺,促进降低中心粒细胞、巨噬细胞,减少炎性因子生成[13]。硫酸羟氯喹可抗血脂、抗氧化作用,可有效抑制血小板聚集,改善局部血流[14]。硫酸羟氯喹可促进分泌胰岛素,抑制胰岛素分解,并经干预葡萄糖转移因子-4影响葡萄糖代谢,促进降低血糖水平,缓解机体氧化应激及炎症反应,促进溃疡面愈合[15]。在本研究中,治疗后,试验组糜烂面积、VAS评分均小于对照组,总有效率大于对照组,提示硫酸羟氯喹口服联合康复新液、曲安奈德混合液含漱可促进糜烂型OLP创面修复,缓解病人疼痛。
研究证明,疾病可导致与其相关的遗传因子改变,进而导致相关蛋白也随之发生数量、种类的改变[16]。AT-Ⅲ为抗凝血酶蛋白,除抗凝作用外,AT-Ⅲ还可降低炎症细胞活性,诱导生成抗炎物质。AT-Ⅲ可结合内皮硫酸肝素,抑制细胞因子等物质生成,调节细胞信号通道,缓解炎症反应[17]。IgM为机体及免疫应答中最早生成的抗体,在评价机体感染中具有重要作用,其水平升高提示体液免疫激活[18]。ZAG为脂肪调节因子,可经识别免疫因子及经脂类配体路径递呈抗原参与免疫应答,其水平升高可导致恶性肿瘤的发生[19]。IL-12、IL-17为促炎因子,不但参与免疫应答,还可导致炎症反应。IL-12、IL-17可诱导NK细胞增殖,促进其分泌干扰素γ,诱发并推动免疫炎症反应[20]。在本研究中,治疗前两组病人血清AT-Ⅲ、IgM、ZAG、IL-12、IL-17水平均异常升高,提示两组病人机体均存在较强的免疫炎症反应,治疗后两组病人血清AT-Ⅲ、IgM、ZAG、IL-12、IL-17水平均降低,且试验组小于对照组,说明硫酸羟氯喹口服联合康复新液、曲安奈德混合液含漱可抑制机体免疫炎症反应,纠正差异蛋白及炎性因子异常改变。资料显示,硫酸羟氯喹可导致视网膜或视野改变,且其导致上述病变和剂量相关,若硫酸羟氯喹剂量<6.5 mg·kg-1·d-1,则发生视网膜或视野改变的风险相对较低[21]。本研究应用剂量为200 mg/d,剂量相对较小,故未出现眼部明显损害病人,仅2例病人出现视物模糊。但因应用硫酸羟氯喹存在一定风险,故临床应用期间要加强眼科检查,以避免风险事件发生。
总之,硫酸羟氯喹口服联合康复新液、曲安奈德混合液含漱治疗糜烂型OLP,可抑制机体免疫炎症反应,纠正差异蛋白及炎性因子异常改变,改善病人临床症状,缓解疼痛,抑制OLP恶性进程,安全可靠。



