王丽丽,孙启飞,张敏
作者单位:宣城市人民医院(皖南医学院附属宣城医院)影像科,安徽 宣城242000
胃癌是消化系统最常见的恶性肿瘤之一,发病率在全世界位居第5位,病死率位居第3位[1]。中国是胃癌高发地区,据报道,超过40%的胃癌新病例发生在中国[2],严重威胁人民健康。胃癌的分期与病人生存时间密切相关,亚洲国家Ⅱ期胃癌的5年生存率达70%,但Ⅲ~Ⅳ期胃癌病人5年生存率急剧下降[3]。虽然根治性手术是目前胃癌的首选治疗方式,但由于其早期症状不明显,许多病人被诊断时分期较晚,手术效果不佳或失去了手术机会[4]。术前新辅助化疗可促进肿瘤缩小、提高可切除率、延长总生存期。中国临床肿瘤学会推荐术前新辅助化疗用于T3~4期病人,但不推荐用于T2期以下病人[5]。因此,准确区分T1~2期与T3~4期胃癌极其重要。在此,本研究通过回顾性分析行胃癌根治术病人的多层螺旋CT(multi-slice spiral CT,MSCT)资料,探讨MSCT在区分T1~2与T3~4期胃癌中的应用价值,以期为临床决策提供影像学依据。
1 资料与方法
1.1 一般资料 选取2018年9月至2021年12月在宣城市人民医院行胃癌根治术且具有术前CT检查的胃癌病人83例,其中男性57例,女性26例,年龄范围为37~86岁,年龄(65.2±10.2)岁。病人或其近亲属知情同意。本研究符合《世界医学协会赫尔辛基宣言》相关要求。
1.2 仪器与方法 采用Philips Brilliance 16排螺旋CT病人进行检查,管电压为120 kV,管电流为250 mA,矩阵为512×512,层间距为5 mm,厚层为5 mm,重建层厚2 mm。病人扫描前空腹8 h,15 min内摄入600~800 mL水后行CT扫描;采用头先进屏气扫描,扫描范围从膈顶至双肾下极,期相包括平扫、动脉期、静脉期及延迟期,平扫结束后使用高压注射器按300 gI/L注射欧乃派克注射液80 mL,注射速度为3 mL/s,以主动脉150 Hu阈值自动触发动脉期增强扫描,静脉期及延迟期分别于动脉期后30 s、90 s获得。
1.3 图像分析 CT图像由2名高年资放射科主治医师在不知病理结果的情况下,在PACS系统上对图像进行分析,两者意见存在分歧时,则与另外1位主任医师协商并达成一致。评估内容包括:
(1)肿瘤生长模式:①息肉样为腔内生长的肿块;②蕈样为病灶处胃壁增厚>1 cm,无论有无局限性凹陷;③溃疡样为局部胃壁增厚<1 cm的凹陷性病变;④弥漫性浸润为病变累及整个胃壁的50%以上[6]。
(2)肿瘤平扫密度和肿瘤强化模式:①均匀;②不均匀。
(3)肿瘤强化程度:采用复制、粘贴感兴趣区域(ROI)的方法测量肿瘤各期CT值。对比动脉期肿瘤与同层面竖脊肌CT值,以两者差10 Hu为界线,将肿瘤强化程度分为:①高:两者之差>10 Hu;②等:两者之差10 Hu以内;③低:两者之差<-10 Hu。
(4)肿瘤大小:测量肿瘤的最长径线和最宽径线。
(5)淋巴结转移:定义存在短径>0.8 cm的区域淋巴结为可疑淋巴结转移[7]。
(6)术前CT肿瘤分期:MSCT按以下标准评估肿瘤的T分期,T1期为胃黏膜局限性增厚并明显强化,黏膜下低密度条纹连续;T2期为胃壁局限性或弥漫增厚,低密度条纹中断或消失,病灶局部浆膜面清晰光滑,胃周脂肪间隙清晰;T3期为胃壁呈结节状增厚,外缘不规整,浆膜面毛糙、连续性欠佳,胃周脂肪浸润;T4期为肿瘤和邻近器官间的脂肪间隙消失或有侵犯邻近器官的直接表现[8]。
1.4 病理评估 一位高年资病理科主治医生根据美国癌症联合会(the American joint committee on cancer, AJCC)第8版胃癌分期标准对手术切除标本进行T分期:T0为切除标本中未发现肿瘤;Tis为肿瘤位于上皮内,未侵犯黏膜固有层;T1为肿瘤侵犯固有层、黏膜肌层或黏膜下层;T2为肿瘤侵犯固有肌层。T3为肿瘤穿透浆膜下结缔组织,但未侵犯脏层腹膜或邻近结构;T4为肿瘤侵犯浆膜或邻近结构[9]。
1.5 统计学方法 统计分析采用SPSS 26.0和Med-Calc 16.8.4软件,连续变量符合正态性分布者使用描述,不符合正态性分布者使用中位数(第25、75百分位数),即M(P25,P75)描述,两组比较采用t检验或Mann-WhitneyU检验;定性资料使用例(%)描述,采用χ2检验或秩和检验。将两组间有统计学差异的指标纳入logistic多因素回归分析并建立预测模型,通过绘制受试者操作特征(receiver operating characteristic,ROC)曲线,使用曲线下面积(area under curve,AUC)评估预测模型的诊断效能。使用Delong法比较不同AUC之间的差异。P<0.05为差异有统计学意义。
2 结果
2.1 临床资料 根据AJCC胃癌分期标准,T1期15例,T2期15例,T3期21例,T4期32例。根据病人病理T分期是否≥3,将所有病人分为T1~2和T3~4两组。T1~2组30例,男性21例,女性9例,年龄(65.5±8.2)岁;T3~4组53例,男性36例,女性17例,年龄(65.0±11.2)岁。两组性别、年龄差异无统计学意义(P>0.05)。
2.2 CT征象评估 T1~2组病人肿瘤以溃疡性生长为主(22/30)、平扫密度均匀者多见(22/30)、强化以均质为主(19/30),T3~4组则多表现为浸润性生长(38/53)、平扫密度不均匀(27/53)、强化不均质(40/53),两组肿瘤生长方式、平扫密度、强化方式、强化程度、肿瘤长径及宽径、出现可疑淋巴结转移的比例、肿瘤静脉期及延迟期CT值均差异有统计学意义(P<0.05)。两组平扫及动脉期CT值差异无统计学意义(P>0.05)。见表1。

表1 T1~2与T3~4两组病人胃癌CT各征象比较
T1~2组术前CT肿瘤分期为T1期13例,T2期9例,T3期5例,T4期3例;T3~4组术前CT肿瘤分期为T1期0例,T2期2例,T3期12例,T4期39例,两组术前CT肿瘤分期比较,差异有统计学意义(χ2=77.37,P<0.001)。术前CT肿瘤分期整体准确率为67.47%(56/83),浆膜面毛糙用以区分T1~2与T3~4,其准确率为87.95%(73/83),诊断错误主要源于术前CT对T1~2组病人的过高分期。典型病例胃癌CT影像见图1。
2.3 预测术后病理T3~4的logistic回归分析 单因素logistic回归分析显示CT图像上肿瘤呈非溃疡样生长、平扫密度不均匀、不均质强化、静脉期CT值、延迟期CT值、肿瘤长径、肿瘤宽径、可疑淋巴结转移及CT分期T3/4在预测病理T3~4期中差异有统计学意义。将P<0.05的变量纳入多因素logistic回归分析中,采用向前LR逐步回归法筛选有统计学意义的变量(P<0.05)构建模型。结果显示非溃疡样生长、可疑淋巴结转移及浆膜面毛糙为术后病理T3~4期的独立危险因素(表2),基于该结果建立的预测模型AUC为0.92,95%CI:(0.84,0.97),灵敏度为92.5%,特异度为83.3%;而术前CT肿瘤分期预测T3~4期的AUC为0.82,95%CI:(0.72,0.89),灵敏度为73.6%,特异度为90.0%,两者差异有统计学意义(Z=3.34,P<0.001)。
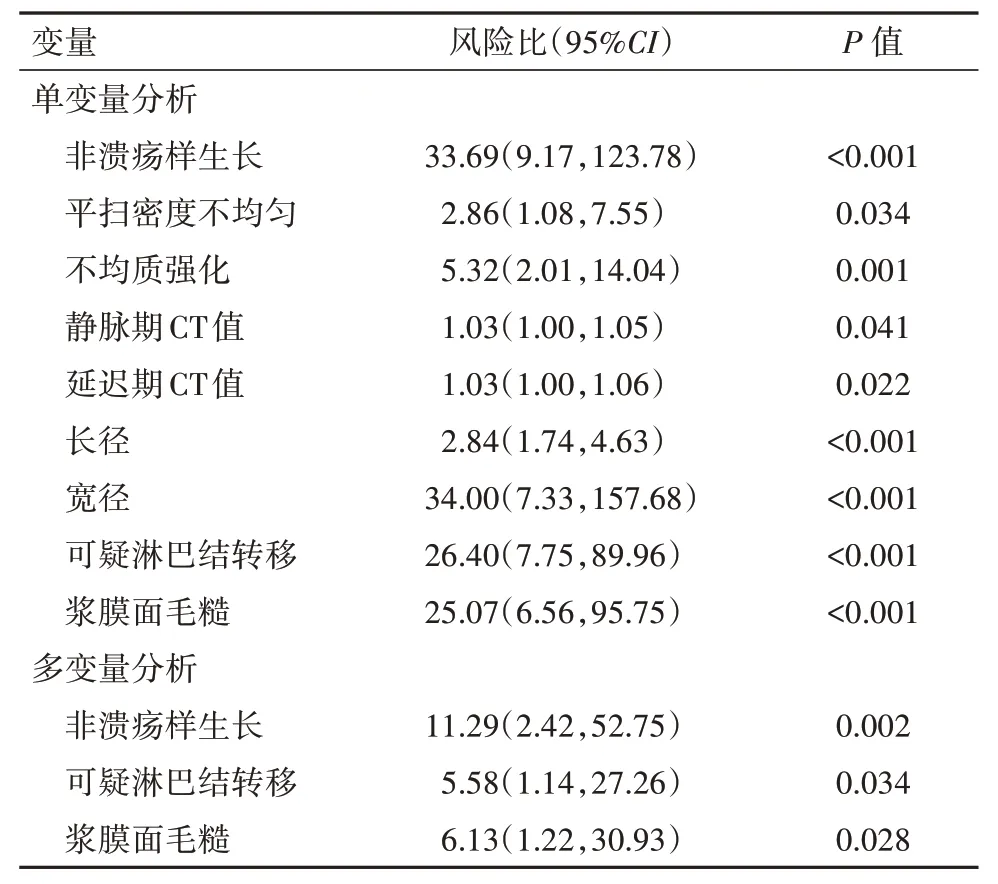
表2 预测术后病理T3~4单因素及多因素logistic回归分析
3 讨论
术前准确评估胃癌的T分期对于制定其治疗方案及评估预后非常重要。T1~2与T3~4期的准确区分有助于筛选合适的病人行术前新辅助化疗,从而提高手术切除率及改善预后。目前,MSCT是我国胃癌术前T分期评估的常用手段,研究[10]显示,术前MSCT对胃癌T分期的总体准确率约为43%~82%,与本研究相一致。然而,在本研究中,术前MSCT区分T1~2与T3~4的准确率为87.95%,高于文献[11]报道的77.0%~79.2%,可能原因是我们将Tis归入T1期病人也纳入研究人群中,T1期胃癌在CT上较容易与T3/4期相区分,这导致了整体准确率的提高。
MSCT区分胃癌T1~2与T3~4的依据主要是肿瘤是否侵犯浆膜下层,但在CT图像上区分胃壁固有肌层与浆膜下层较难,特别表现为单层胃壁时,很难区分T2与T3期肿瘤,此外胃周边细小迂曲分支血管,或多个聚集小淋巴结紧贴胃壁、周围炎性索条及病人消瘦等因素,易导致T2与T3期肿瘤的分期存在误判[12],这也是本组病例中T1~2组病人出现过高分期原因。如何减少过高分期,提高诊断准确率,可能需要结合更多的影像特征,如肿瘤的形态、淋巴结等情况进行综合考虑。本研究显示,除了肿瘤侵犯胃壁的深度之外,其他MSCT征象也可能有助于胃癌分期。相对于T1~2期胃癌,T3~4期胃癌更倾向于呈非溃疡性生长、CT平扫密度更不均匀、增强扫描更容易表现为不均质高强化、肿瘤体积更大、局部区域出现可疑淋巴结转移的概率更高。多因素logistic回归显示,除了肿瘤浸润深度外,非溃疡样生长和可疑淋巴结转移也是预测术后病理T3~4期的独立危险因素。溃疡样生长多见于T1~2期的原因可能是MSCT上能观察到的溃疡多较表浅,以浸润黏膜下层与固有层为主,若溃疡进一步发展浸润更深层胃壁,则局部胃壁增厚更加明显,侵犯范围也更大,胃壁厚度多大于1 cm,表现为蕈样或弥漫性浸润样生长。本研究中息肉样生长的胃癌病例数较少,但多以T3~4期为主,原因并不明确,可能与MSCT上能观察到呈息肉样生长的胃癌体积一般较大且基底往往较深,浸润浆膜面的概率增大有关。此外,淋巴结转移被证实与胃癌T分期密切相关[13],在本研究83例病人中,T1、T2、T3、T4期胃癌病理上证实淋巴结转移的概率分别为6.67%(1/15)、46.67%(7/15)、85.71%(18/21)和93.75%(30/32),因此,在MSCT上观察到0.8 cm以上淋巴结时提示肿瘤可能处于较高的T分期。
我们的研究显示,联合非溃疡样生长、可疑淋巴结转移及浆膜面毛糙三个CT征象建立的预测模型在区分T1~2及T3~4期胃癌上较单纯使用肿瘤浸润深度的判断标准更准确。此外,判断肿瘤生长方式及测量淋巴结直径较为容易、客观,在对胃癌进行CT分期的同时即可进行,并不会显着增加影像医师的工作量及难度,有利于在临床开展。
本研究有一定的局限性。这是一个单中心回顾性分析,病例数较少,预测模型的性能需要多中心前瞻性研究进一步验证。另外,本研究未对每个CT征象的可重复性进行研究。
总而言之,MSCT在区分T1~2和T3~4期胃癌中具有较高的准确率,联合非溃疡样生长、可疑淋巴结转移及浆膜面毛糙、周围脂肪间隙模糊三个CT征象建立的预测模型较术前CT肿瘤分期更准确,值得临床推广使用。



