刁晓艳 何燕
(1.贵州医科大学附属医院心血管科,贵州 贵阳 550004;2.贵州医科大学分子生物学教研室,贵州 贵阳 550004)
原发性高血压(EH)是当今社会的最常见疾病之一,它的发病机制一直处于研究和探讨之中,它是由遗传因素与环境因素相互作用所致的复杂性疾病[1]。基因的研究不断进展,但仍众说纷纭。近年来研究认为细胞色素p450c17alpha蛋白(CYP17A1基因)多态性及成纤维细胞生长因子5(FGF5基因)多态性与EH的发病的有一定的相关性,但结论不一致[2-6,8-12]。本研究选择贵州省贵阳市部分汉族人群作为研究对象,探讨他们的基因多态性与EH的发病关系,现报告如下。
1 资料与方法
1.1研究对象 EH组:选择在贵州医科大学附属医院心内科门诊或住院部高血压患者191例,血压诊断标准按中国高血压指南(2010年)标准;排除继发性高血压、瓣膜疾病、心肌病及肝、肾衰竭,孕妇、哺乳期妇女以及精神疾病史或滥用药物者等;患者中男86例,女105例,平均年龄(58.86±11.67)岁。对照组:选择在贵州医科大学附属医院门诊的健康体检者196例,无高血压家族史,无各类心血管、脑血管、肾、内分泌等方面疾病的健康人群;患者中男85例,女111例,平均年龄(55.07±11.08)岁。两组性别差异无统计学意义(P>0.05),年龄差异有统计学意义(P<0.05)。两组均为贵州籍汉族人,且互相均无血缘关系。
1.2方法
1.2.1生化指标测定 清晨空腹抽取静脉血检测血脂(包括甘油三酯、总胆固醇)、血糖和尿酸。
1.2.2体质量指数(BMI)计算 采用国际标准化方法测量身高、体重。BMI=体重/身高2(kg/m2)。
1.2.3基因分型 按经典常规法(酚-氯仿法)抽提白细胞DNA,溶于TE;紫外吸收法定量后标化为30 ng/μL,-40℃备用。应用TaqMan 实时荧光定量PCR技术对CYP17A1基因和FGF5基因进行基因分型。PCR反应为10 μL体系:DNA(浓度为30 ng/μL)1.5 μL,通用TaqMan PCR Master Mix 5 μL,双蒸水3.25 μL,20×基因分型探针及引物0.25 μL。其中TaqMan PCR Master Mix、基因分型探针及引物均购自美国ABI公司,探针分别用FAM、VIC染料标记。反应条件为:95℃ 10 min活化AmpliTaq金牌酶后,95℃ 15 s,60℃ 1 min 20 s,共55个循环。仪器采用美国ABI公司生产的Step one Plus PCR仪,读取FAM/VIC荧光判断基因分析结果。FAM荧光探针识别T等位基因,VIC荧光探针识别C等位基因。每块96孔板设3孔阴性对照,并随机抽取5%样本复测,一致性为100%。

2 结 果
2.1一般资料及临床生化指标比较 两组年龄、血糖、甘油三酯及BMI比较,差异有统计学意义(P<0.05)。见表1。

表1 一般资料及临床生化指标比较
2.2基因型和等位基因频率分布 两组CYP17A1 C/T基因型及FGF5 T/A基因型的分布均符合Hardy-Weinberg遗传平衡(P>0.05)。经χ2检验CYP17A1 C/T两组间基因型分布差异有统计学意义(P<0.05),两组间等位基因频率分布差异有统计学意义(P<0.05)。两组间FGF5 T/A基因型及等位基因型差异无统计学意义(P>0.05)。见表2。

表2 两组CYP17A1 C/T与FGF5 T/A基因型和等位基因频率比较[n(%)]
2.3原发性高血压的患病风险分析 去掉性别、身高、体重、尿酸等混杂因素(P>0.05)进行Logistic回归分析,年龄、FGF5 TT基因型、CYP17 A1 TT基因型和空腹血糖高于正常标准的人群具有更高的患病风险,特别是当空腹血糖高于正常标准时较对照组患病风险提高4倍。见表3。
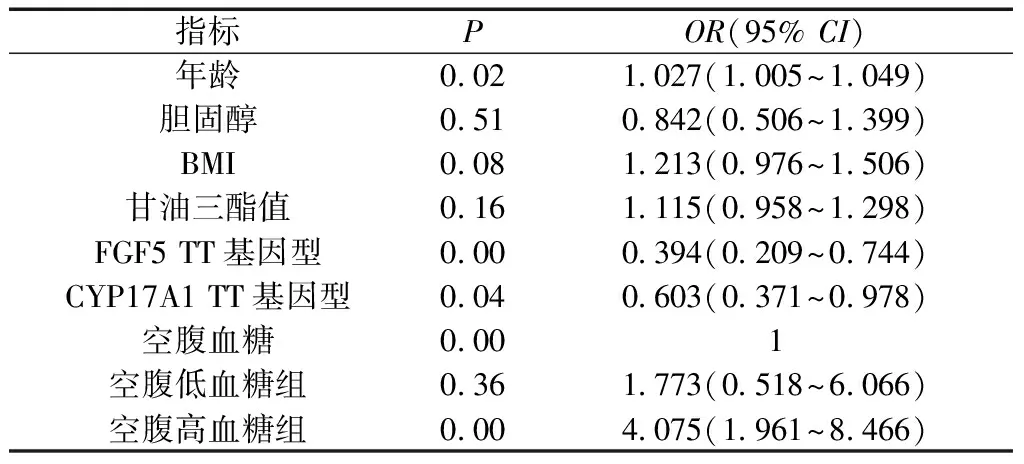
表3 高血压的患病风险分析
3 讨 论
原发性高血压的发病具有相当的遗传因素,但至今候选基因仍很多。近年发现4q21区域的FGF5(成纤维细胞生长因子5)基因内的rs16998073位点主要是与盐敏感性相关,该基因遗传变异与血压可能相关[7,12]。迄今为止,盐敏感性高血压的发病机制仍有争论。有研究[11]认为FGF5可以促进细胞生长和在多种细胞增殖,包括心肌细胞,能够促进心脏血管形成。然而,现在没有证据证明这个基因与高血压发病机理的关系。目前有研究[8]表明在韩国人中FGF5(rs16998073)遗传变异与盐敏感性密切相关。全基因组关联分析(GWAS)研究认为8个与血压相关基因变异,其中包括FGF5(rs16998073)为一个可能性的因素。在日本人中认为FGF5是与高血压发病关系最明显的基因位点。FGF5在日本人群中对收缩压和舒张压的影响是欧洲人群中1.4倍[10]。
CYP17A1基因编码细胞色素P450c17alpha蛋白,影响类固醇17alpha-羟化酶和17,20 裂解酶活性,在类固醇的生存途径的调控中起着重要的作用。CYP17A1rs11191548位点的突变可导致17alpha-羟化酶/17,20 裂解酶缺陷症,从而损害肾上腺和性腺中类固醇激素的合成,刺激肾上腺皮质增生和17-脱氧类固醇前体如孕酮、孕烯醇酮、脱氧皮质酮、皮质酮等发挥盐皮质激素功能,引起水钠潴留,血压增高[9]。近年来很多研究致力于rs11191548与高血压相关性,但是结论有所争议,C.Newton-Cheh[2]在欧洲家系及印度—亚洲家系的样本进行研究中认为位于10q24.3的CYPl7A1基因的rs11191548与收缩压(SBP)相关。K.W.Hong[3]等选择了7 551例韩国人,发现CYPl7A1基因rs11191548位点携带C最小等位基因能显着降低SBP、舒张压(DBP)及高血压的患病风险。而X.M.Li[5]研究结果表明CYPl7A1基因rs11191548位点携带C最小等位基因的能增加高血压的患病风险。Y.H.Lin[6]与先前的欧洲人群和中国汉族人群不同,在畲族人群中未发现rslll91548突变与高血压有显着的相关性。
本研究结果显示,CYPl7A1基因C/T基因型与等位基因频率在贵州省汉族的EH组和对照组中差异有统计学意义(P<0.05),均明显高于对照组组。提示CYPl7A1基因C/T基因型与高血压的发病可能相关。虽然本研究未得出FGF5基因多态性与高血压的明显关系,但在多元回归分析中提示FGF5 TT基因型可能患高血压的风险较大(P<0.05),而且CYPl7A1 TT基因型 FGF5 TT基因型在高血压的风险分析中同时具有统计学意义,提示两种基因型同时存在时可能会增加高血压的发病。在两组FGF5的基因型和等位基因比较中也可看到TT基因型和T等位基因在EH组中较多,但无统计学意义,目前对FGF5基因与高血压的关系大部分集中在与盐敏感性的关系上,故推测是否与入组病人中盐敏感性高血压类型少有关。
目前对上述两种基因与高血压的关系仍无定论,本研究结果显示,年龄、空腹血糖、甘油三酯、体重指数是高血压发病的危险因素,但如果加入基因多态性的影响,就只显示年龄和血糖与高血压患病风险更高。总的看来高血压的发病机制很复杂,遗传、环境及获得性因素对高血压发病均有关系。本研究也进一步提示对高血压的基因研究还存在很多复杂性,包括神经体液因素对高血压的发病机制的影响。



