张朝霞 董璇
(西安大兴医院内分泌科,陕西 西安 710002)
2型糖尿病(type 2 diabetes,T2DM)是由于胰岛素抵抗和胰岛素分泌不足引起血糖升高的一种内分泌疾病,在全球有着很高的流行率[1-2]。二甲双胍的药物反应个体差异性比较明显,这导致很多患者单纯使用二甲双胍治疗的降糖效果有限,需要联合其它药物治疗。利拉鲁肽是一种人胰高血糖素样肽-1 (Glucagon-like peptide-1,GLP-1)受体激动剂,是治疗T2DM的新型降糖药物。本研究采用利拉鲁肽联合二甲双胍治疗T2DM。报告如下。
1 对象与方法
1.1一般资料 选择2020年4月至2021年10月我院接诊的89例T2DM患者,纳入标准:明确诊断的新发2型糖尿病患者,既往未使用过降糖药物;18~70岁;体重指数(BMI)≥24.0 kg/m2;糖化血红蛋白<9%的2型糖尿病患者;精神状况良好,无认知障碍和老年痴呆;心、肝、肾功能基本正常;临床资料完整,自愿签署知情同意书。排除标准:合并甲状腺疾病及其它内分泌疾病;合并糖尿病酮症酸中毒;近期服用过对糖脂代谢有影响的药物;对本研究药物有禁忌;不可控制的高血压;不遵医嘱用药、饮食及运动;有甲状腺髓样癌病史或家族史;急性、慢性胰腺炎病史;有明确的精神疾病史,如抑郁、精神分裂、双向情感障碍;明确的胃肠动力障碍类或梗阻类疾病,如胃轻瘫、胃食管反流病;明确的肿瘤病史;严重脂代谢障碍:TG≥500 mg/dL(5.7 mmol/L);妊娠或哺乳期妇女;不能在试验期间采取有效避孕措施的男女受试者;研究者认为不适合入组者。随机分为两组,研究组46例:男27例,女19例;年龄45~77岁,平均(56.04±7.15)岁。对照组43例:男25例,女19例;年龄49~74岁,平均(54.82±10.09)岁。两组一般资料比较无统计学意义(P>0.05)。
1.2方法 研究组:二甲双胍片(中美上海施贵宝制药有限公司,国药准字H20023370 )500 mg/次,口服,3次/d;利拉鲁肽(丹麦诺和诺德公司,注册证号S20110046)0.6~1.2 mg/次,每日早餐前皮下注射,1次/d。对照组:仅口服二甲双胍片,500 mg/次,3次/d。两组患者每隔2~3 d自测指尖血糖,目标血糖:空腹血糖(Fasting plasma glucose,FPG)5~7 mmol/L、餐后2 h血糖(2h postprandial plasma glucose,2hPG)7~10 mmol/L。两组患者均观察12周。观察指标:两组患者治疗前后进行口服葡萄糖耐量试验检测FPG,检测标准馒头2hBG;检测糖化血红蛋白(glycatedhemoglobin A1c,HbA1c)和空腹胰岛素(fasting insulin,FINS)。采用稳态模式评估法评价胰岛素抵抗指数(homeostasis model assessment-insulin resistance index,HOMA-IR)=FINS×FPG/22.5。检测血清总胆固醇(Total cholesterol,TC)、甘油三酯(triglycerides,TG)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)水平。并进行体格检查,计算体质量指数(Body Mass Index,BMI)和腰臀比。
1.3统计学方法 采用SPSS24.0统计软件分析处理数据,计数资料以率表示,采用χ2检验;计量资料以表示,采用t检验。P<0.05表示有统计学意义。
2 结 果
2.1两组治疗前后血糖水平和HbA1c比较 两组治疗后FBG、2hBG、HbA1c均明显降低(P<0.05),且研究组FBG、2hBG、HbA1c均明显低于对照组(P<0.05)。见表1。
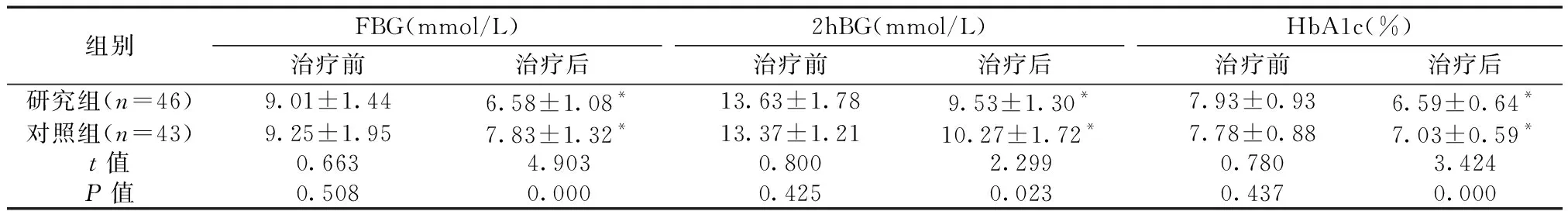
表1 两组治疗前后血糖和HbA1c水平比较
2.2两组治疗前后体格检查比较 治疗后研究组BMI和腰臀比明显降低(P<0.05),研究组BMI明显低于对照组(P<0.05)。见表2。
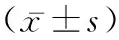
表2 两组治疗前后体格检查比较
2.3两组治疗前后HOMA-IR比较 治疗前研究组、对照组的HOMA-IR分别为(4.17±1.09)、(4.22±1.51),对比无差异(P>0.05);治疗后分别为(2.56±0.83)、(3.83±0.85),相比治疗前均降低,且研究组低于对照组(P<0.05)。
2.4两组治疗前后血脂比较 治疗后研究组血脂水平改善明显优于对照组(P<0.05),TC、LDL-C水平明显低于对照组(P<0.05)。见表3。
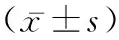
表3 两组治疗前后血脂比较
2.5两组不良反应发生情况比较 研究组出现低血糖2例(4.35%),胃肠道反应3例(6.52%);对照组出现低血糖1例(2.33%),胃肠道反应2例(4.65%),研究组不良反应较高于对照组,但大都轻微,均可耐受,两组比较无统计学意义(P>0.05)。
3 讨 论
GLP-1由肠道L细胞分泌,主要响应食物摄入,它具有广泛的生理作用,包括以葡萄糖依赖性方式刺激胰岛素分泌和减少胰高血糖素分泌,并导致肝葡萄糖产生减少[3]。在动物模型中,它可促进β细胞增殖和新生,同时减少细胞凋亡。利拉鲁肽作为长效GLP-1受体激动剂被批准用于T2DM的治疗,它可带来血糖和体重控制的双重益处,此外还可调节高血压、左心室功能、心脏脂肪变性、氧化应激和细胞凋亡等[4],对T2DM及其并发症具有独特的治疗潜力。
本结果显示,与对照组比较,研究组治疗后的FBG、2hBG、HbA1c水平控制更满意,证明利拉鲁肽联合二甲双胍治疗对高血糖的控制是可观的。一些研究表明,更早开始使用长效 GLP-1受体激动剂可对 T2DM患者产生更好的降糖作用[5]。Meta分析显示,当疗程<52周时,GLP-1受体激动剂对FPG的控制效果与胰岛素相当,但更长疗程时GLP-1受体激动剂对FPG的控制则不如胰岛素有优势[6]。BMI≥28 kg/m2定义为肥胖。本研究患者总体偏于肥胖,适度减重有利于改善血糖控制和胰岛素抵抗,并减少心脑血管疾病的风险因素。本结果显示,治疗后研究组BMI和腰臀比明显降低,而对照组虽有所下降,但尚未达到统计学意义,提示二甲双胍单药治疗的减重效果缓慢,而联合利拉鲁肽则能更快降低BMI。研究表明,利拉鲁肽可有效降低控制不佳的T2DM患者的肝脏脂肪含量[7]。对于2型糖尿病患者来说,减重尤其具有挑战性,一方面是由于存在肥胖相关的激素和代谢异常,另一方面是可用于减肥的药物选择很少,即便通过生活方式干预和使用降糖药将体重减轻,也可能面临体重反弹。利拉鲁肽可抑制食欲中枢增加饱腹感,并能延缓食物消化,延长胃排空,减慢胃肠蠕动,通过减少食物摄入而非增加能量消耗来达到减轻体重的目的[8],这种显着的胰外作用对于肥胖T2DM患者来说具有重要意义。相应地,研究组血脂(TC、LDL-C)水平改善明显优于对照组,即利拉鲁肽联合二甲双胍治疗也有利于促进T2DM患者脂代谢的改善。研究表明,利拉鲁肽对餐后乳糜微粒代谢具有特定作用,可将乳糜微粒中的apoB48合成减少60%,并提高乳糜微粒的甘油三酯/apoB48比率,降低乳糜微粒清除率,以及减少低密度脂蛋白1—甘油三酯的分泌[9]。本结果显示,两组治疗后HOMA-IR均明显降低,而对照组显然不及研究组,提示利拉鲁肽联合二甲双胍对胰岛素抵抗的改善具有叠加作用。利拉鲁肽改善胰岛素抵抗的内在机制复杂,可能与提高血浆高分子量脂联素的含量[10]。本研究显示研究组不良反应较高于对照组,但大都轻微,均可耐受,两组比较无统计学意义(P>0.05)。本研究较少出现不良反应,需长期评估药物安全性。
综上所述,利拉鲁肽联合二甲双胍治疗T2DM具有协同作用,对减轻体重、改善胰岛素抵抗、调节糖脂代谢可发挥更满意的效果。



