薛世航,黄芳,何瑛,张同成,陆振一
替吉奥胶囊治疗老年晚期胃癌的近期疗效和安全性探究
薛世航,黄芳,何瑛,张同成,陆振一
目的观察替吉奥胶囊(S1)治疗老年胃癌晚期患者的治疗效果及药物不良反应。方法53例老年晚期胃癌患者,均具有可测量指标,口服S1单药治疗,每次剂量40 mg/m2,2次/d;连续口服4周,停药2周为1个治疗周期,治疗2个周期以上,再进行疗效评价。结果53例中完全缓解2例、部分缓解13例、病情稳定16例、病情进展22例。有效率28.3%,肿瘤控制率58.5%,生活质量改善19例(35.8%)。胃肠道反应、骨髓抑制、皮肤色素沉着是主要药物不良反应表现,Ⅰ~Ⅱ°为主,并无化疗相关性死亡。结论S1治疗老年晚期胃癌有效、安全。
胃肿瘤;癌;晚期;替吉奥;疗效
胃癌是国内外最常见的实体恶性肿瘤,尽管在胃癌早期诊治上取得一定突破,但晚期胃癌的预后仍然很差,特别在经济条件落后地区,初治以进展期胃癌为主。对于晚期胃癌,化疗与单纯最佳支持治疗相比,在生存质量和生存时间方面均有益处[1]。随着我国老年化进程发展,老年患者的比例逐年增加,而老年人(联合国世界卫生组织定义60岁以上为老年人)表现进行性基础代谢下降,脏器功能逐渐衰退,治疗的耐受性降低以及毒副作用增加,难以耐受经典的多药联合化疗。宁波市第四医院于2011年12月至2014年12月对53例老年晚期胃癌患者应用替吉奥胶囊(S1)单药化疗,近期疗效明确,安全性好,现报道如下。
1 资料与方法
1.1一般资料本文收集53例晚期胃癌患者,其中男29例,女24例;年龄60 ~81岁,平均(73±10.3)岁;初治25例,复治28例;组织病理学分类:低分化腺癌30例,高中分化腺癌11例,黏液腺癌5例,印戒细胞癌7例;肝转移10例,肺转移6例,腹腔淋巴结转移18例,左锁骨上淋巴结转移5例,盆腔转移5例,骨转移1例;化疗前常规行血常规、血生化、腹部增强CT检查。
所有患者均符合以下标准:均经病理、影像学证实为晚期胃癌(Ⅲ~Ⅳ期);有可测量的肿瘤病灶;Karnofsky(KPS)评分≥60分,预计生存期≥3个月;既往未接受过化疗或复治者既往未用口服氟尿嘧啶类药物,距末次化疗时间超过4周;无心、肺、肝及肾等重要器官功能明显异常,血常规、肝肾功能正常;患者或家属知情同意,签署化疗同意书。
1.2治疗方法S1(山东鲁南制药集团新时代药业有限公司生产)单次剂量40 mg/m2,2次/d,餐后口服,连续口服4周,休息2周为1个周期;进行2个周期以上治疗再进行疗效评估。定期复查血指标,期间予止吐及护肝等对症治疗,必要时予重组人粒细胞刺激因子(G-CSF)、促红细胞生成素(EPO)、重组人白介素-11(IL-11)等支持。
1.3疗效评价化疗前均常规体格检查及血常规、血生化。可测量病灶均有化疗前的基线测量,以后每2个周期进行影像学评估。疗效评价按RECIST1.1标准分为完全缓解(CR)、部分缓解(PR)、病情稳定(SD)和病情进展(PD)。有效率(RR)以CR+PR统计,疾病控制率(DCR)以CR+PR+SD计算,完成2个周期以上后疗效评估。生活质量评估按照治疗前后KPS评分变化,分为改善、稳定、恶化,改善为增高≥10分,稳定为无变化,恶化为降低≥10分。
1.4不良反应评价按照美国NCI制定的不良评价标准(CTC,第3版)评价不良反应,按WHO标准分为0~Ⅳ级。
2 结果
2.1近期临床疗效评价全组53例均列入评价对象,均可评价客观疗效。53例患者共完成S1化疗192周期;完成2个周期化疗者9例,完成3个周期化疗者18例,完成4个周期化疗者14例,完成5个周期化疗者8例,完成6个周期化疗者4例。CR 2例(3.8%)、PR 13例(24.5%)、SD16例(30.2%)、PD22例(41.5%);RR 28.3%,DCR 58.5%。见表1。
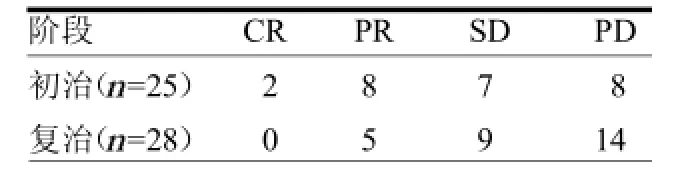
表1 不同阶段近期疗效 例
2.2生活治疗改善情况生活质量改善19例(35.8%),稳定24例(45.3%),恶化10例(18.9%)。
2.3不良反应主要药物不良反应为胃肠道反应、骨髓抑制及皮肤色素沉着,Ⅰ~Ⅱ°为主,无化疗相关死亡病例,见表2。

表2 S1治疗老年晚期胃癌的不良反应情况
3 讨论
晚期胃癌失去手术机会,化疗是主要治疗方法,目前的研究表明化疗与最佳支持治疗(BSC)相比,可明显改善晚期胃癌患者的生活质量,延长生存期,中位存活可达7.5~12个月[2]。然而目前胃癌无“金标准”的化疗方案,临床上根据肠癌的研究,采用一系列的相识方案,多且复杂。临床上晚期胃癌以老年人为多,随年龄增大,出现不同程度的脏器功能减退,储备能力下降,多药联合方案使患者生活质量明显下降,有的缩短生存期。对于年龄大、一般情况差,无法耐受联合化疗,可以考虑使用单药延缓疾病进程,以改善患者的生活质量[3]。
1999年S1在日本首先获批治疗胃癌,目前临床上已成为治疗胃癌的一线药物[4]。S1是氟脲嘧啶衍生物口服制剂,包括替加氟(FT)和2种修饰剂,包括吉美嘧啶(CDHP)及奥替拉西(OXO),FT 是5-Fu的前体药物,经肝脏P450系统生成5-Fu,有优良的口服生物利用度,半衰期较长,可达12 h。CDHP在肝脏分布,拮抗5-FU分解代谢酶二氢嘧啶脱氢酶(DPD),使5-Fu浓度增加,增强抗癌效果。OXO的作用是阻断5-FU磷酸化,以减少胃肠道不良反应。与传统5-FU制剂相比,S1能延长血液、肿瘤组织中5-FU的浓度、时效,以增加其抗肿瘤效果,减轻副作用,是安全有效的抗癌药物[5]。
据统计,在日本晚期胃癌化疗80%以上使用S1,有效率为24.7%~44.6%。Sakata等[6]报道一项51例晚期胃癌参加试验结果,S1每天80 mg/m2,饭后口服,2次/d,连续服药28d,6周为1个疗程。4个疗程后评价。其中CR 1例,PR 24例,总有效率为49%。不良反应发生率为 78%,Ⅲ~Ⅳ度不良反应发生率为20%,主要包括白细胞减少、中性粒细胞减少、血小板减少、皮疹、腹泻及蛋白尿,未发现严重反应。Koizumi等[7]报道晚期胃癌患者应用顺铂(DDP)+S1化疗,其有效率达74%;骨髓抑制达Ⅲ~Ⅳ°为15.8%,但无CR的患者。
本组S1单药化疗53例患者,年龄在60岁以上、一般情况较差,伴有不同程度脏器功能减退;结果显示CR2例(3.8%)、PR13例(24.5%)、SD16例(30.2%),RR为28.3%;稍低于国内外报道的 24.7%~44.6%。这可能和本组均为老年晚期胃癌患者,且本地区多为农村患者,发现疾病相对较晚期有关。本组2例CR患者均为未接受过其他化疗、放疗的初治患者,考虑与基因多态性、对药物比较敏感有关。同时研究表明S1单药化疗可改善患者生活质量,KPS评分改善率达35.8%,明显提高患者生活质量(QOL)[8]。
S1主要药物不良反应包括胃肠道反应、骨髓抑制及皮肤色素沉着和肝肾功能损害;Ⅰ~Ⅱ°显着,绝大多数经积极处理可改善,本组所有患者完成2个周期以上化疗,仅4例患者因出现Ⅲ°骨髓抑制而延缓,具有良好的治疗依从性。出现Ⅲ°不良反应包括腹泻、白细胞下降、血小板下降,发生率为5.7%,予以口服酸洛哌丁胺胶囊止泻、G-CSF升白细胞、IL-11升血小板等相应对症治疗后均好转。
[1]金懋林.抗癌新药治疗胃癌进展[M].北京:科学出版社,2000:55-64.
[2]Alberts SR,CervantesA,vande VeldeCJ, et al.Gastric cancer:epide-miology,pathology and treatment[J].AnnOncol,2003, 14(supp 12):S31.
[3]储大同.老年肿瘤学[M].北京:人民卫生出版社,2009:83.
[4]Shirasaka T.Development history and concept of an oral anticancer agent S-1 (TS-1):Its clinical usefulness and future vistas[J].JpnJClinOncol,2009,39(1):2-15.
[5]孙燕,石远凯.临床肿瘤内科手册[M].5版.北京:人民卫生出版社,2007:846.
[6]Sakata Y,Ohtsu A,Horikoshi N,et al. Late phaseⅡstudy of novel oral fluorop yrimidine anticancer drugsS-1(1M tegafur-0.4M gimestat-lM otastat potassium)in advanced gastric cancer patients[J].Eur J Cancer,1998,34(11):1715-1720.
[7]Koizumi W,Tanabe S,Saigenji K,et al. Gotoh M:PhaseⅠ/Ⅱstudy of S1 combined with cisplatin in patients with advanced gastric cancer[J].Br Cancer,2003, 89:2207.
[8]赵晓光,张艳珠.替吉奥治疗老年进展期胃癌临床观察[J].实用临床医药杂志, 2011,15(11):103-105.
10.3969/j.issn.1671-0800.2016.02.029
R735.2
A
1671-0800(2016)02-0195-03
2015-09-10
(本文编辑:姜晓庆)
315700宁波,宁波市第四医院
陆振一,Email:luzhengyi@ 126.com



