丁敏之
冠状动脉粥样硬化性心脏病是由于供应心脏血液的动脉出现血栓及粥样硬化,致使血管、血液流变学异常,造成动脉血管狭窄甚至闭塞,引起心肌血供不足所致局部组织缺血性坏死[1]。该病以老年患者居多,病死率、致残率较高,预后差。目前对于该病的治疗,药物洗脱支架置入术仍是非药物治疗的主流,但该技术因金属网格残留及聚合物基质等特点容易出现晚期血栓形成、支架内再狭窄等问题,因此也并非完美[2]。随药物涂层球囊扩张术在支架内再狭窄病变中取得了良好效果,同时在小血管病变中的应用效果也颇为显着。该扩张术由于无置入物残留,因此降低了支架内狭窄或血栓形成的发生率,同时可保留血管的正常生理结构,促进血管重塑,且涂层球囊的操作简单[3]。但目前该类研究还较少。本研究将采用药物涂层球囊扩张术应用在高龄冠状动脉粥样硬化性心脏病患者中,现将结果报道如下。
1 资料与方法
1.1 一般资料 选取2017 年12 月至2019 年12 月在浙江省诸暨市人民医院就诊的高龄冠状动脉粥样硬化性心脏病患者98 例,按照随机数表法分为对照组(45 例)与观察组(53 例)。对照组男29例,女16 例;年龄75 ~83 岁,平均(79.8±3.1)岁;病程2 ~12 年,平均(7.08±1.37)年;合并高血压25 例,糖尿病8 例,高血脂19 例;病变部位:左前降支19例,左回旋支14例,右冠状动脉10 例,其他2 例;靶血管直径(2.55±0.42)mm,狭窄率(65.36±5.36)%。观察组男33 例,女20 例;年龄75 ~85 岁,平均(80.1±3.7)岁;病程3 ~13 年,平均(8.07±1.84)年;合并高血压28 例,糖尿病10 例,高血脂22 例;病变部位:左前降支22 例,左回旋支15 例,右冠状动脉13 例,其他3 例;靶血管直径(2.59±0.38)mm,狭窄率(65.42±5.18)%。两组一般资料差异无统计学意义(P >0.05)。本研究已经院内医学伦理委员会批准。
1.2 入选标准 纳入标准:符合《高龄老年冠心病诊治中国专家共识》[4]诊断标准,年龄≥75 岁,CT 造影显示动脉血管狭窄,具有手术适应证;无手术禁忌史,签署知情同意书。排除标准:肝、肾功能不全,合并多种心血管疾病,免疫系统异常,凝血功能障碍,对研究药物过敏,临床资料不完整及精神认知异常。
1.3 方法 两组患者术前1 周均口服阿司匹林(规格100 mg,拜耳医药保健有限公司,国药准字J20130078)100mg/次,1 次/d;氯吡格雷[规格75 mg,赛诺菲(杭州)制药有限公司,国药准字J20180029]口服,75 mg/d,1 次/d。术后继续服用这两种药物至少3 个月。两组患者均行经皮冠状动脉介入治疗(PCI),手术开始给予100 U/kg 肝素注射,之后以1 000 U/h追加注射。采用标准Judkins 法,穿刺患者股动脉或右侧桡动脉,通过定量血管造影判断血管管腔口径,之后分别进行相应的球囊扩张。
1.3.1 对照组 采用切割球囊系统(Boston Scientific 波士顿科学国际有限公司),球囊到达病灶后以1 atm/5 s 的速度缓慢扩张球囊至6 ~8 atm,当压力达到最高时持续10 ~15 s。
1.3.2 观察组 采用紫杉醇药物涂层球囊(B.Braun Melsungen 德国贝朗医疗),血管直径与药物球囊直径比值为1∶(0.8 ~1),球囊到达病灶后以1 atm/5 s的速度缓慢扩张球囊至10 atm,压力最高在12 atm,并在压力达到最高时持续30 ~50 s。根据《药物涂层球囊临床应用中国专家共识》[5]相关标准操作。对于狭窄钙化严重的血管应先用切割球囊充分预扩张后再用药物球囊扩张。
1.3.3 手术成功标准 主支血管未受影响,血管狭窄减少>30%,残余狭窄<50%。
1.4 观察指标(1)血液流变学:分别于术前、术后3 个月取患者空腹静脉血5 ml,离心取血清,冰箱冷存,采用自动清洗旋转式黏度分析仪检测患者全血低切黏度、全血高切黏度、血浆黏度及红细胞聚集指数。(2)血清因子:分别于术前、术后3 个月取患者空腹静脉血5 ml,离心取血清,冰箱冷存,借助沈阳万泰医疗设备有限责任公司提供的OTA-400全自动生化分析仪,行免疫散射比浊法测定血清C 反应蛋白(CRP)水平;借助美国雅培公司AXSYM全自动免疫分析仪行放射免疫法测定内皮素1(ET-1)水平;采用化学发光法检测一氧化氮(NO)水平;试剂盒均购于上海酶联生物科技有限公司。(3)对患者进行6 个月随访,记录心血管不良事件(MACE)发生率,包括靶病变血运重建、心绞痛、心源性猝死、心律失常及急性心肌梗死。总发生率=MACE 例数/总例数×100%。
1.5 统计方法 采用SPSS 23.0 统计软件进行处理,计量资料以均数±标准差表示,两组比较采用独立样本t 检验,组内比较采用配对t 检验;计数资料比较采用2检验。P<0.05为差异有统计学意义。
2 结果
2.1 血液流变学 术前,两组血液流变学指标差异均无统计学意义(均P >0.05);术后3 个月,两组全血低切黏度、全血高切黏度、血浆黏度、红细胞聚集指数均有所降低,且观察组低于对照组(均P <0.05)。见表1。
2.2 血清因子 术前,两组血清因子水平差异无统计学意义(均P >0.05);术后3 个月,两组NO 均有所升高,CRP、ET-1 有所降低,且观察组改善优于对照组(均P <0.05)。见表2。
2.3 MACE 事件 观察术后6 个月内MACE事件发生率低于对照组,但差异无统计学意义(2=1.566,P>0.05)。见表3。
3 讨论
血管内皮损伤是诱发心血管疾病发生及发展的始动因素。有研究证实因置入支架导致的血管内皮损伤、慢性炎症反应等与MACE 发生率呈正相关[6]。血管内皮细胞作为血管壁与血流间的物理屏障,发挥着主动运输及物质交换的重要作用,并为血管内血栓的形成提供载体,释放血管活性物质,抑制血小板黏附,以保证体内基本稳态。冠心病冠脉狭窄,导致血管内皮功能稳定被打破,出现功能紊乱,降低NO释放,导致血管收缩,增加血液黏稠度及血栓形成,进一步加重冠脉狭窄程度。
相比药物洗脱支架置入术,球囊扩张无异物置入,可避免聚合物基质和金属网格残留等问题,降低血栓风险,减少血管炎症反应。本研究观察组血液流变学指标改善优于对照组,血清因子水平控制优于对照组。这表明药物球囊扩张能更有效减少晚期血管再狭窄及血管炎症反应[7]。切割球囊扩张压力小,手术即刻效果好,可减少血管内膜的无序撕裂;但血管内膜撕裂后,会损伤内膜,诱发局部炎症反应,增加粥样硬化斑块的形成、脱落及冠脉不良事件发生风险。药物球囊表面为抗增殖药物与造影剂的混合物,短时间的球囊扩张可使血管内皮与抗增殖药物紧密结合,抑制细胞结构生成与快速增殖、内膜炎性反应,从而减少晚期血管丢失;因此更利于血管病变远期预后[8]。此外,药物涂层球囊扩张术扩张程度较高,有利于改善血液流变学。

表1 两组血液流变学指标比较
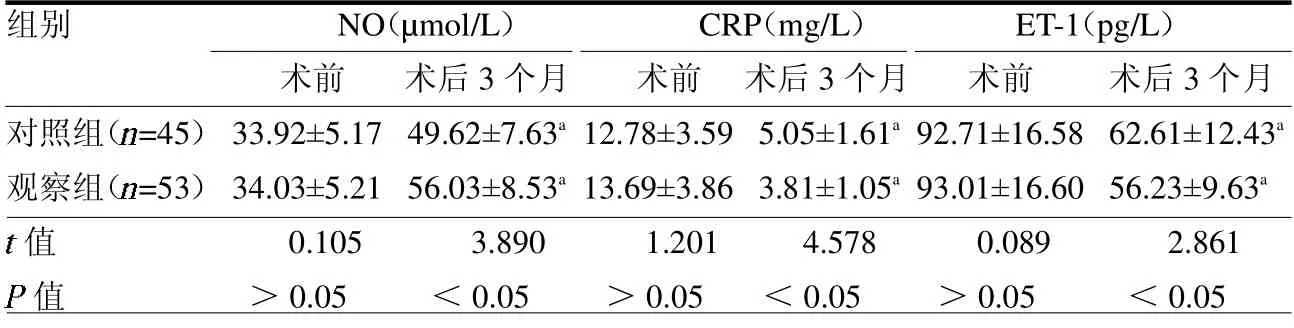
表2 两组血清因子比较比较
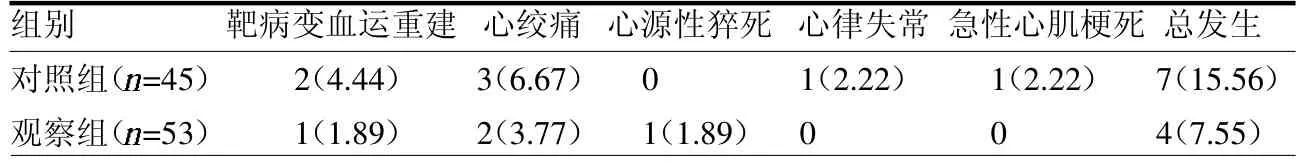
表3 两组MACE 事件比较 例(%)
对患者6 个月随访发现,观察组MACE 事件略低于对照组,但差异无统计学意义,这可能与样本量较少有关。但值得注意的是,药物球囊也存在局限性,无法克服管壁弹性回缩,因药物球囊的轮廓要较大,因此不易通过靶血管,对于纤维化、严重钙化病变患者疗效并不理想;同时在操作过程中,球囊表面涂层的药物成分容易被冲刷,且紫杉醇药物浓度若过高还会出现细胞毒作用。
综上所述,药物涂层球囊扩张术在高龄冠状动脉粥样硬化性心脏病患者中的应用价值较高,可有效改善血液流变学,减少炎性反应,降低MACE事件发生率。



