徐金迪,刘悦,徐文斌,钟辉,戴蓉丹,庄伟
骨质疏松症(OP)易造成脆性骨折,其中髋部最为常见,多见于老年人[1]。有脆性骨折史的患者发生二次骨折的风险显着高于同年龄、同性别和无脆性骨折史者,其10 年内再骨折风险为28%[2]。骨折联络服务(FLS)旨在通过对脆性骨折患者进行识别、确认、干预治疗及疗效评价,以达到降低再次骨折发生率。本文旨在分析骨折联络服务联合针药模式防治老年髋部脆性骨折的疗效,报道如下。
1 资料与方法
1.1 一般资料 收集2020 年1—12 月杭州市萧山区中医院收治的老年髋部脆性骨折患者共57 例,纳入标准:(1)年龄≥65 岁;(2)符合《原发性骨质疏松症诊疗指南(2017)》[3]及《中国骨质疏松性骨折诊疗指南—骨质疏松性骨折诊断及治疗原则》[4]中脆性骨折的诊断标准;(3)髋部X 线或CT 检查提示髋部骨折(股骨颈骨折或股骨转子间骨折);(4)同意接受手术治疗并愿意配合随访的患者。排除标准:(1)非典型性骨折、陈旧性骨折或肿瘤疾病造成的病理性骨折者;(2)合并有严重免疫系统疾病及内科疾病患者;(3)存在明显手术禁忌证者。患者及家属对本研究均知情同意,研究获得杭州市萧山区中医院医学伦理委员会审核批准。
采用随机数字表分法将57 例患者分为FLS 组(对照组)及FLS 联合针药组(观察组)。对照组29例,其中男11 例,女18 例;年龄60 ~82 岁;平均(80.1±7.9)岁;骨折类型为股骨颈骨折13 例,股骨转子间骨折16 例;手术方式为闭合复位髓内针内固定术18 例,切开复位内固定术5 例,人工髋关节置换术6 例。观察组28 例,其中男13 例,女15 例;年龄60 ~82 岁;平均(80.4±8.5)岁;骨折类型为股骨颈骨折10 例,股骨转子间骨折18 例;手术方式为闭合复位髓内针内固定术16 例,切开复位内固定术5 例,人工髋关节置换术7 例。两组基线资料差异均无统计学意义(P >0.05),具有可比性。
1.2 方法
1.2.1 对照组(1)成立FLS诊疗团队,包括骨科医师、骨科病区护士及康复科医师,其中抽调1 名骨科医师及骨科护士作为FLS 联络员,负责脆性骨折患者的识别,预约相关检查预约、患者OP 防治教育、患者饮食计划、患者治疗情况监督,患者随访计划安排等。(2)患者入院后,FLS 联络员采集病史并预约骨密度及骨代谢指标检查,识别出脆性骨折患者。(3)组织患者家属参加本研究团队主持的以OP 为主题的科普讲课并进行视频学习,结束后逐一发放OP 知识图册,预留患者家属微信。(4)术前予患者活血化瘀、补液退肿及抗凝等药物治疗;手术团队进行术前评估,术前讨论,告知患者及家属手术前后可能存在的风险,取得患者及其家属配合,病情告知记录及手术知情同意书完善签字;由同一骨科手术团队进行;术后常规补液抗炎抗凝治疗,定期切口清洁换药。(5)予患者抗OP 治疗:术后3 d,口服碳酸钙D3 片(Ⅱ)(北京康远制药有限公司,国药准字:H20093675)600 mg及骨化三醇软胶囊[正大制药(青岛)有限公司,国药准字:H20030491]0.5g,1 次/d;术后7 d,予林格氏液1 000 ml 静脉滴注唑来膦酸注射液(诺华制药)100 ml∶5 mg。(6)联络员为患者术后康复给予饮食建议,康复科医师制定术后康复计划:术后1 ~2 d,行主动踝泵运动,30 次/组,间歇1 min,5 ~8 组/d;术后3 ~6 d,行股四头肌群锻炼及屈膝锻炼,15 次/组,间歇1 min,10 组/d;术后7 ~14 d,患者扶助行器或床旁扶手主动站立15 ~30 min,身体直立,同时主动屈髋、中立位伸髋,锻炼组数及角度根据患者病情及耐受情况进行个性化调整;术后14d,切口拆线后予出院。(7)联络员通过微信定期回访监督患者服药依从性并对可能出现的药物不良反应进行反馈收集,告知患者保持术后康复锻炼,对患者返家期间康复相关问题进行答疑,预约并通知下次随访时间,患者来院后对每次随访结果进行记录。
1.2.2 观察组 FLS 诊疗方案同对照组,术后治疗中加入针药治疗。(1)电针疗法:采用电针仪(鑫升G6805-Ⅰ型)进行,1 次/2 d。患者取健侧卧位,取穴:足三里穴、肾俞穴、脾俞穴、肝俞穴、三阴交穴、关元穴及命门穴,施术部位常规碘伏消毒处理,选用一次性无菌针灸针(华佗,040.30×40 mm),针刺穴位得气后,针尾部予金属夹加持连接电针仪,疏密波连续频率2 Hz,电流8 ~10 mA,可适当进行频率及电流大小调整,以局部肌肉轻微抖动为宜;同时予生物灯电磁波治疗仪(中芝CQ-BS8)对施针部位进行照射加热,促进穴位得气,留针20 ~30 min 后拔出针灸针,局部再次消毒皮肤。以上治疗隔日1 次,7 次为一个疗程,治疗至出院前,出院后每2 周1 次至术后6 月。(2)药物治疗:术后2 d,予口服益骨汤协定方:补骨脂(盐)10 g、骨碎补9 g、丹参10 g、地黄15 g 及牛膝10 g 加入没过药面的纯净水浸泡药物约20 min,煎煮约30 min,去渣取液约300 ml,1 剂/d,早晚温服;口服金天格胶囊(西安金花制药)1.2g,每日3次,上述药物连续口服至术后12 个月。
1.3 观察指标(1)术前、术后2 周、术后3 个月、术后6 个月及术后12 个月采用疼痛视觉模拟评分(VAS)评价两组疼痛程度。(2)采用X 射线骨密度监测仪(美国GE Lunar Prodigy Advance 型)测量两组术前,术后3、6 及12 个月髋部骨密度值(BMD值)。(3)取两组患者清晨静脉血,采用电化学发光免疫分析法检测两组术前,术后3、6 及12 个月体内Ⅰ型胶原羧基端肽特殊序列( -CTX)、骨钙素N-端中分子片段(N-MID)及Ⅰ型前胶原氨基末端前肽(PINP)含量。(4)采用Harris评分评价两组关节功能。
1.4 统计方法 数据采用SPSS 25.0 软件分析处理,计量资料以平均数±标准差表示,采用t 检验;计数资料比较采用检验。P<0.05 表示差异有统计学意义。
2 结果
2.1 VAS 评分比较 观察组术后3 及6 个月VAS评分均低于对照组(均P <0.05),见表1。
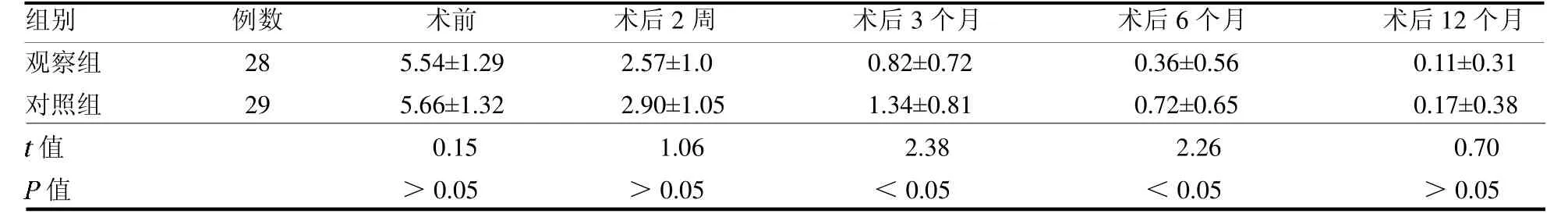
表1 两组治疗前后VAS 评分比较 分
2.2 BMD 值比较 观察组术后3、6 及12 个月BMD 值均高于对照组(均P <0.05),见表2。
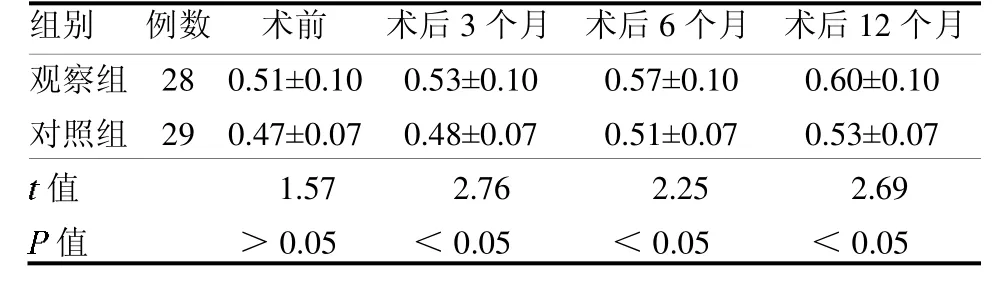
表2 两组治疗前后BMD 值比较 g/cm2
2.3 Harris 评分比较 观察组术后3、6 及12 个月Harris 评分优于对照组(均P <0.05),见表3。
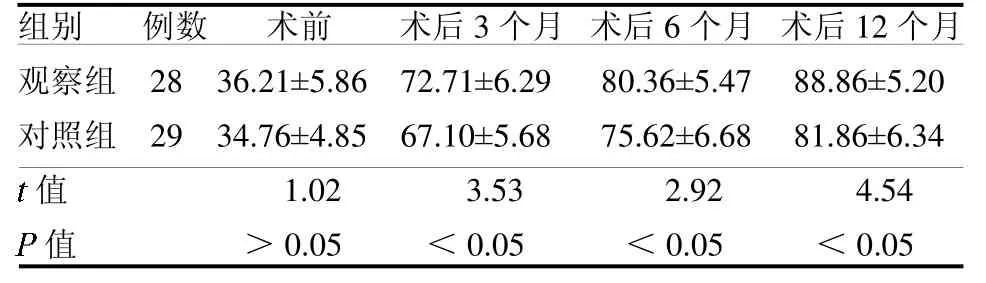
表3 两组治疗前后Harris 评分比较 分
2.4 骨代谢指标比较 观察组术后3、6 及12 个月-CTX 值及PINP 值均低于对照组(均P <0.05),NMID 值均高于对照组(均P <0.05),见表4 ~6。
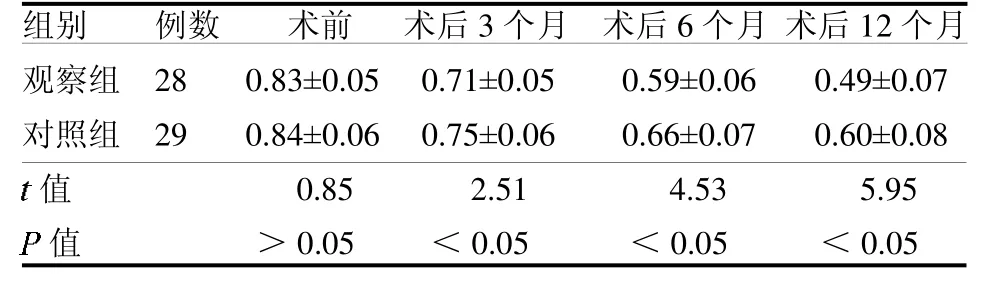
表4 两组治疗前后-CTX 值比较 ng/ml
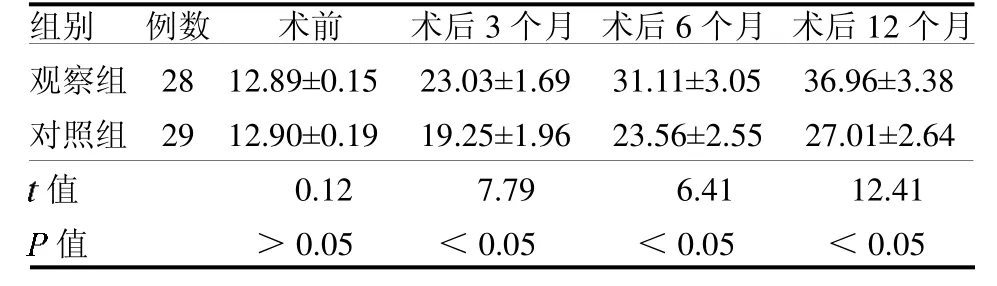
表5 两组治疗前后N-MID 值比较 ng/ml
3 讨论
以往对于老年髋部骨折治疗过程中,仅将治疗重点着眼于手术治疗也止步于手术,缺乏评估和治疗OP 的项目,即便有部分医师有OP 防治意识且采取了相应措施,患者出院后的治疗依从性远低于在院期间,随访时也并未持续关注患者骨健康情况及予以跟进治疗。另外,多数患者直至出现明显不适症状或出现脆性骨折才意识到需要就医,甚至部分患者会认为OP 不需要治疗。因此,对脆性骨折患者的明确诊断、准确识别、积极治疗、跟踪随访需成规范化及体系化。国际骨质疏松基金(IOF)为解决这一问题,于2012 年发起了“攻克骨折”行动,提出向全球推广FLS 作为防治脆性骨折的标准模式[5]。
以往FLS 研究中主要围绕护理相关事宜展开,常以护士作为联络员。本研究在参考其他研究的基础上,对FLS人员上做了调整,增加骨科医师与病区护士共同作为联络员,此举提高了骨科医师对于脆性骨折后患者OP 干预的敏感度和重视程度,也保证了实施过程的安全性及专业性。与此同时,鉴于快速康复理念在骨科中的广泛运用,本研究纳入康复科医师作为治疗环节中的重要组成部分,为患者术后制定相应康复训练计划以助患者尽早康复。近年来中医药在防治OP 方面发挥了其独特的作用,故本研究在治疗过程中将祖国医学相关治疗手段融入其中,充分发挥传统医学在治疗OP 中的作用。
本研究显示,观察组术后3 及6 个月VAS 评分均低于对照组(均P <0.05)。治疗中通过对特定穴位针刺,使不同种类神经肽物质得到分泌,如速激肽P物质、内源性阿片肽、促肾上腺皮质激素等,这些物质促使中枢神经肽释放加速,而电针所产生的电刺激在脊髓背角产生了“长时程抑制”,减轻了患者的痛敏和超敏,从而最终达到了相应的镇痛治疗效果[6]。
骨代谢指标是反应骨健康,预测评估骨折风险的重要指标。-CTX 是反映了破骨细胞骨吸收活性的有效标志物,可用于双膦酸盐类药物治疗的治疗监测[7-8];N-MID是成骨细胞分泌物,作为诊断OP的特异性指标反映骨形成与骨吸收偶联或解偶联情况[9];PINP反映成骨细胞活力及合成骨胶原能力,是骨形成特异性指标,在预测OP 的发生、评价骨量、监测抗OP 疗效等都有较高的特异性和敏感性,且不受激素影响[10-11]。观察组术后3、6 及12 个月-CTX 值及PINP 值均低于对照组(均P <0.05),N-MID 值均高于对照组(均P <0.05)。Harris 髋关节功能评分是目前临床应用广泛的常用的评价髋关节功能段的方法。本研究结果显示,观察组术后3、6 及12 个月Harris 评分优于对照组(均P <0.05),观察组在康复治疗的基础上加之以针药结合疗法,其关节功能提升效率较对照组优势更明显。
利益冲突 所有作者声明无利益冲突



