吴晨颖,杨 毅,陈光强,陆 宽,龚建平
(苏州大学附属第二医院影像科,江苏苏州 215004)
肺肉瘤样癌2例并文献复习
吴晨颖,杨毅,陈光强△,陆宽,龚建平
(苏州大学附属第二医院影像科,江苏苏州 215004)
肺肉瘤样癌(pulmonary sarcomatoid carcinoma,PSC)是指分化较差的非小细胞肺癌(non-small cell lung cancer,NSCLC),临床上较少见,PSC区别于其他种类肺癌的特征为肉瘤样分化或含有肉瘤成分,预后与普通肺癌不同,其发病率较低,占NSCLC的0.3%~4.7%[1],术前诊断较困难。现将2例PSC病例结合其影像学特征及相关文献报道如下。
1临床资料
患者1:男,73岁,因“痰血伴胸闷半个月”就诊,无胸痛、心慌、心悸等其他不适。吸烟史50年(每天20支),少量饮酒。听诊左上肺呼吸音低。胸部CT检查:左肺上叶见一椭圆形软组织占位灶,边缘光整,未见分叶及毛刺,大小约为91.0 mm×80.0 mm×104.0 mm,软组织肿块密度均匀,平均CT值约28.5 HU,其内可见散在多发点状钙化(图1A),病灶紧邻胸壁,与其呈锐角,临近胸膜稍增厚;增强扫描病灶动脉期未见强化,CT值为28.7 HU,病灶前缘紧贴左肺动脉上叶分支,内侧与降主动脉紧密相接(图1B);静脉期平均CT值分别为34.0 HU,肿块密度欠均匀(图1C)。冠状位(图1D)及矢状位(图1E)重建图像更清楚显示病灶与胸壁及肺内大血管间关系,外侧与胸壁紧密相连,但肋骨未见破坏,内侧与主动脉相接。纵隔内第10组见1枚增大淋巴结,直径为16.0 mm,强化模式与左肺肿块相同。
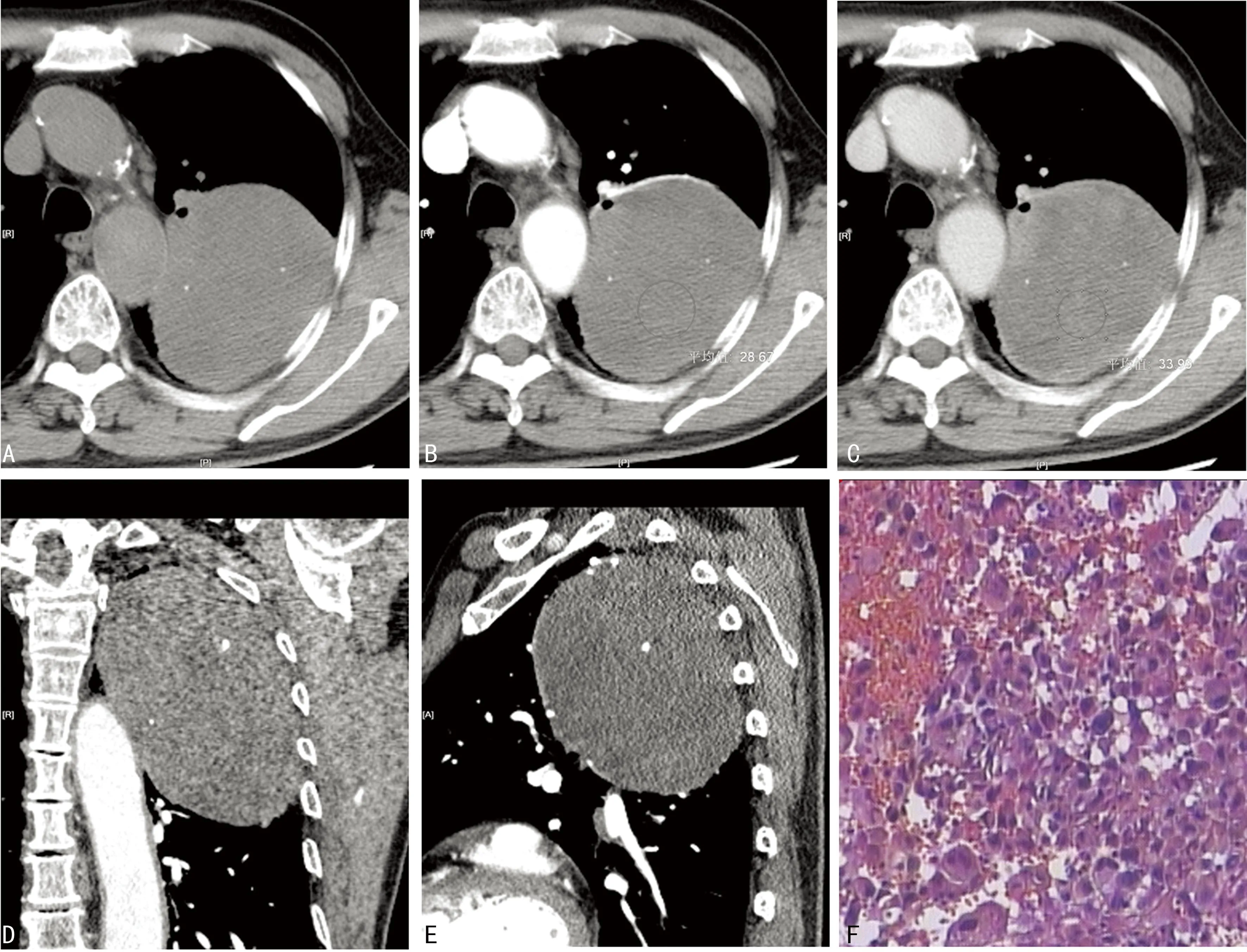
A:CT平扫;B:CT增强动脉期;C:CT增强静脉期;D:CT动脉期冠状位重建;E:CT动脉期矢状位重建;F:病理HE(×100)。
图1左上肺叶PSC影像及病理检查图像
入院8 d后行左上肺癌根治术。(1)术中见:肺裂发育不良,左肺上叶肿瘤,外侵胸壁,无明显胸腔积液。(2)大体所见:肺组织,计13.0 cm×17.0 cm×5.0 cm,距支气管切缘3.0 cm处切开可见一直径约7.0 cm的肿块,见部分坏死,境界不清楚,紧靠胸膜。送检第5组淋巴结:灰黄组织4块,大小3.0 cm×2.0 cm×1.0 cm 。送检第10组淋巴结:灰褐组织2块,绿豆大。(3)镜下所见及免疫组织化学染色:HE染色后镜下所见如图1F,免疫组化指标TTF1(-)、CK7(-)、CKpan(+)、34βE12(+)、P63(-)、S100(-)、HMB45(-)、CD56(-)、Syn(-)、CK5/6(-)。(4)病理诊断:左上肺叶PSC,侵及胸膜,支气管切缘未见癌累及,支气管旁淋巴结(0/4)、送检第5组淋巴结(0/5)未见癌转移,送检第10组淋巴结(1/1)见癌转移,淋巴结内见胶原结节。4个月后随访CT未见明显复发及转移灶。
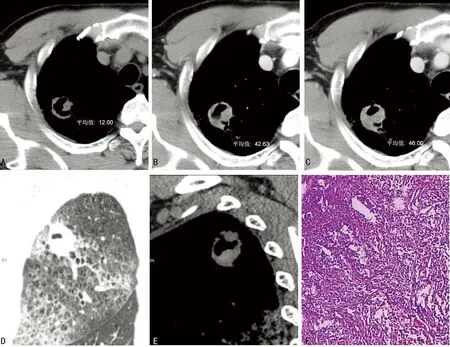
A:CT平扫;B:CT增强动脉期;C:CT增强静脉期;D:CT肺窗冠状位重建;E:CT平扫矢状位重建F:病理HE(×100)。
图2右上肺PSC伴腺样分化CT及病理检查图像
患者2:男,65岁,因“咯血1月余,声音嘶哑3 d”入院。患者1个月前出现咳痰,痰中带血,为暗红色,无胸痛、胸闷、气急不适。于当地医院就诊行胸部CT示右上肺阴影,并伴卫星灶,考虑肺结核可能。患者于当地医院进行住院治疗,行结核菌素试验(PPD试验)、痰培养等结核病检查,基本排除活动性肺结核,予抗感染治疗半月后复查胸片未见明显改变,咯血较前好转。病程中患者咳痰、咯血,近3 d患者出现声音嘶哑。患者吸烟40余年(每天30支)。胸部CT检查及冠矢状位重建示:右肺上叶尖段可见环形壁厚薄不均空洞病灶,大小约35.0 mm×23.0 mm×17.0 mm,空洞内外壁均欠光整,边界尚清,厚壁,密度欠均匀,内壁结节灶平扫CT值约12.0 HU,边缘可见分叶征(图2A),增强扫描见明显欠均匀强化,动脉期与静脉期内壁结节灶CT值分别约42.6 HU和46.0 HU(图2B、C);病灶周围还可见大片网格状/絮状斑片影及斑点状小结节影,叶间裂局部下凸改变(图2D、E)。右侧肺门可见一直径约11.5 mm淋巴结,静脉期CT值约69.0 HU,强化模式与肺内结节不同,纵隔内未见增大或/和强化淋巴结。入院8 d后行右上肺癌根治术。(1)术中见:右上肺实变,呈灰肝样,探查右上肺尖前段一直径约4.0 cm大小肿块,质硬,与周围组织分界欠清,无法推动,表面肺组织凹陷,中下肺未见明显异常,故决定切除右上肺。(2)大体所见:右上肺17.0 cm×14.0 cm×4.0 cm,剖开见一肿块直径3.0 cm,灰白质硬,中央见坏死,境界尚清送检淋巴结两枚合计1.5 cm×1.0 cm×0.5 cm。找见支气管旁淋巴结14枚。(3)镜下所见及免疫组织化学染色:HE染色后镜下所见如图2F,免疫组化指标:CK7(+)、CKlw(+)、CKhw(+)、Vim(+)、TTF1(+)、CgA(-)、CK20(-)。(4)病理诊断:右上肺低分化癌,考虑PSC伴腺样分化,支气管残端未见癌累及,送检淋巴结未见癌转移,支气管旁淋巴结(0/14)未见癌转移。随访3年零7个月无明显不适。
2讨论
2.1组织学特点2004年WHO将PSC分为5个亚型:肺母细胞癌(pulmonary blastoma,PB)、多形性癌(pleomorphic carcinoma,PC)、巨细胞癌(giant cell carcinoma,GCC)、梭形细胞癌(spindle cell carcinoma,SCC)、瘤肉癌(carcinosarcoma,CS)[2]。临床上这5种亚型均不多见。SC中的“肉瘤”一说最早由Vir-chow于1864年提出。1992年Ro等[3]建议以“SC”来命名这种肿瘤。SC在全身许多部位都可以发生,但是原发于肺部者比较少见。SC是一种来源于上皮细胞源性的肿瘤,是癌细胞因克隆进化而形成的肉瘤细胞,这种机制又称为“克隆进化”[4]。因此,SC既可以表现出间叶性肿瘤的组织学特点,又能够表现出上皮源性肿瘤的特征。上皮成分以鳞状细胞癌为主,其次为腺癌,部分可见少量小细胞癌或未分化癌。
2.2临床特点PSC好发于老年男性,常有吸烟史。PSC大体病理学可分为两种亚型,即中央型(支气管腔内型)及周围型(肺实质型)。中央型临床较少见,病灶多位于肺门处,肿瘤常呈结节样向支气管腔内突出,生长速度较缓慢,体积较小、边界较清,中央型较少侵犯淋巴结且远处转移少见,早期可有如咳嗽、痰血、胸痛等临床症状,肿块较大阻塞支气管时可引起肺炎、肺不张等,早期切除预后良好。周围型多为实质性肿块,肺边缘多见,生长速度快,体积大,纵隔、临近胸膜、肺内血管较易受侵犯,肿瘤内常因坏死脱落形成空洞,本文2例均为周围型,且都有纵隔淋巴结转移;肿瘤实质内可见多发钙化灶,常无明显临床症状或症状较轻微,以咳嗽、胸痛等为主,早期就可以发生远处转移,预后较差[5]。
2.3影像学特点PSC主要CT特点为:(1)部位。即依据病灶所处的位置分为周围型及中央型,多为周围型。据Kim等[6]报道PSC中有70.7%为周围型,并且肿瘤多发于肺上叶。本文2病例患者均为周围型且病灶都位于肺上叶。(2)大小及形态。由于PSC侵袭性大,恶性程度高,常无明显早期临床症状,故发现时肿瘤一般已较大,病灶边缘常较光滑,呈圆形或类圆形。患者1发现肿瘤时,肿瘤体积已较大,边缘光整;且由于肿瘤内成分生长速度不均一,故可呈分叶征。患者2病灶边缘即可见分叶征。(3)密度。病灶平扫时呈软组织密度,由于肿瘤体积较大,内部常可见坏死,增强后多呈不均匀强化,患者2肿瘤体积虽然不大,但是其内见坏死脱落形成的空洞。Kim等[6]发现胶原组织及肿瘤细胞增强扫描时呈明显强化,出血坏死区或黏液样变性区为无强化的低密度区,患者2病灶强化后呈明显强化,其内见斑片状低密度影未见明显强化,故强化不均匀(图2B)。部分病灶内可见多发钙化灶,如患者1(图1A)。(4)胸膜受侵。周围型病灶好发于胸膜下,且胸膜、胸壁易受侵[6-7],患者1与胸膜分界不清,胸壁受侵,易发生肋骨破坏,可伴胸腔积液。PSC影像学表现介于肺癌及肉瘤之间。有肺癌的临近支气管截断、分叶征、及液化坏死的特征,又有肉瘤边缘光整、直径大的特征。当成分以肺癌为主时,影像学表现偏癌样;当成分以肉瘤为主时,影像学表现偏肉瘤样。PSC早期常易误诊为肺结核及肺炎,晚期则与肺癌难以区分。但CT增强扫描对诊断PSC有一定的帮助,多是软组织肿块无明显强化而肿瘤边界呈不规则斑片状或环形强化,且一般体积较大,而肺癌常呈明显强化,强化不均匀,故增强CT扫描对肺肉瘤样癌与肺癌鉴别有一定价值。特别是当肿瘤出现钙化时,钙化灶位置对诊断肺肉瘤样癌极其重要,当钙化灶位于肿瘤中央位置时,提示肿瘤的侵袭性较高,恶性程度较大。
综上所述,对于60岁左右中老年男性,有长期吸烟史,无明显临床症状,胸部CT发现肺上叶胸膜下较大的软组织肿块,且增强后表现为周边环形强化或小斑片状强化,特别是肿瘤中央见钙化灶时,应考虑到PSC的可能,最终确诊需要病理学诊断。标本内含有50%以上肉瘤样组织才能诊断为PSC,否则应诊断为癌[8]。
参考文献
[1]Pelosi G,Sonzogni A,De Pas T,et al.Review article:pulmonary sarcomatoid carcinomas:a practical overview[J].Int J Surg Pathol,2010,18(2):103-120.
[2]Beasley MB,Brambilla E,Travis WD.The 2004 World Health Organization classification of lung tumors[J].Semin Roentgenol,2005,40(2):90-97.
[3]Ro JY,Chen JL,Lee JS,et al.Sarcomatoid carcinoma of the lung.Immunohistochemical and ultrastructural studies of 14 cases[J].Cancer,1992,69(2):376-386.
[4]Wick MR,Swanson PE.Carcinosarcomas:current perspectives and an historical review of nosological concepts[J].Semin Diagn Pathol,1993,10(2):118-127.
[5]庞颖,夏黎明,曾祥芹,等.肺肉瘤样癌的影像学表现[J].放射学实践,2011,26(2):168-171.
[6]Kim TH,Kim SJ,Ryu YH,et al.Pleomorphic carcinoma of lung:comparison of CT features and pathologic findings[J].Radiology,2004,232(2):554-559.
[7]陈利娜,曾庆思,刘勇彬,等.肺肉瘤样癌的CT表现[J].中国CT和MRI杂志,2012,10(4):15-17,36.
[8]李国栋,周正荣,杨文涛,等.肺肉瘤样癌的CT表现及文献复习[J].中国癌症杂志,2006,16(3):243-244.
作者简介:吴晨颖(1992-),住院医师,大学本科,主要从事胸部影像学研究。△通讯作者,Tel:18962113118;E-mail:cgq74158@163.com。
doi:·短篇及病例报道·10.3969/j.issn.1671-8348.2016.04.052
[中图分类号]R734.2
[文献标识码]C
[文章编号]1671-8348(2016)04-0574-03
(收稿日期:2015-06-08修回日期:2015-10-12)



