廖 伟,杨 红,王洪波,李广阔△,彭 兵,蔡云强
(1.重庆市中医院普通外科 400021;2.四川大学华西医院上锦院区,成都 611730)
胰腺实性假乳头状瘤(solid pseudopapillary neoplasm of the pancreas,SPN)又称胰腺乳头状和实性上皮性肿瘤、胰腺囊实性肿瘤、乳头状囊性上皮肿瘤。是一种罕见的胰腺外分泌肿瘤。最早由FRANTZ[1]于1959年首先报道,1996年世界卫生组织(WHO)正式将其命名为胰腺实性假乳头状肿瘤,该病临床上发病率低且术前诊断较为困难,容易误诊,为低度恶性肿瘤,可以有局部地区浸润,但远处转移极少发生,且该病多好发于胰腺体尾部,极少发生在胰头部。下面就本院1例儿童胰头实性假乳头状瘤的诊治做一系统性回顾。
1 病例资料
患者,女,12岁,学生。因体检发现胰头部占位3年余入院。2013年8月12日于当地某三甲医院行上腹部CT提示胰头部占位,大小约0.8 cm×0.7 cm(图1A),考虑假性乳头状瘤或腺瘤。因无任何不适,建议随访。患者于2014年7月28日于当地同一家三甲医院复查,行上腹部磁共振成像(MRI)提示胰头部占位,大小约1.3 cm×1.1 cm(图1B),考虑假性乳头状瘤或腺瘤。患者仍无明显不适,故继续采取观察,定期随访。患者于2016年8月2日再次复查上腹部MRI,结果提示胰头部占位,大小约2.1 cm×2.1 cm(图1C),考虑假性乳头状瘤或腺瘤。考虑到患者胰头部占位持续长大,有潜在恶变可能,故进一步行内镜诊断性穿刺,病理检查结果提示实性假乳头状瘤,未见明显癌细胞。
患者为手术治疗入住重庆市中医院外二科(胃肠、肝胆),完善相关检查无绝对手术禁忌证,考虑到患者系未成年儿童,术前邀请医院多科室联合术前会诊并上报医务科备案,于2016年9月20日在全身麻醉下行腹腔镜下胰头部肿瘤切除术,术中见肿瘤位于胰腺钩突部,凸向胰腺表面,大小约3 cm×2 cm(图2),术中发现肿瘤与周围组织间隙较清,无严重粘连,顺利将肿瘤游离并完整剜除,术后解剖见肿瘤直径约3 cm,包膜完整(图3),胰头部手术区域常规放置橡胶引流管。

A:上腹部CT,胰头肿块0.8 cm×0.7 cm(黄色箭头);B:上腹部MRI,胰头肿块1.3 cm×1.1 cm(黄色箭头);C:复查上腹部MRI,胰头肿块2.1 cm×2.1 cm(黄色箭头)
图1 上腹部CT及MRI
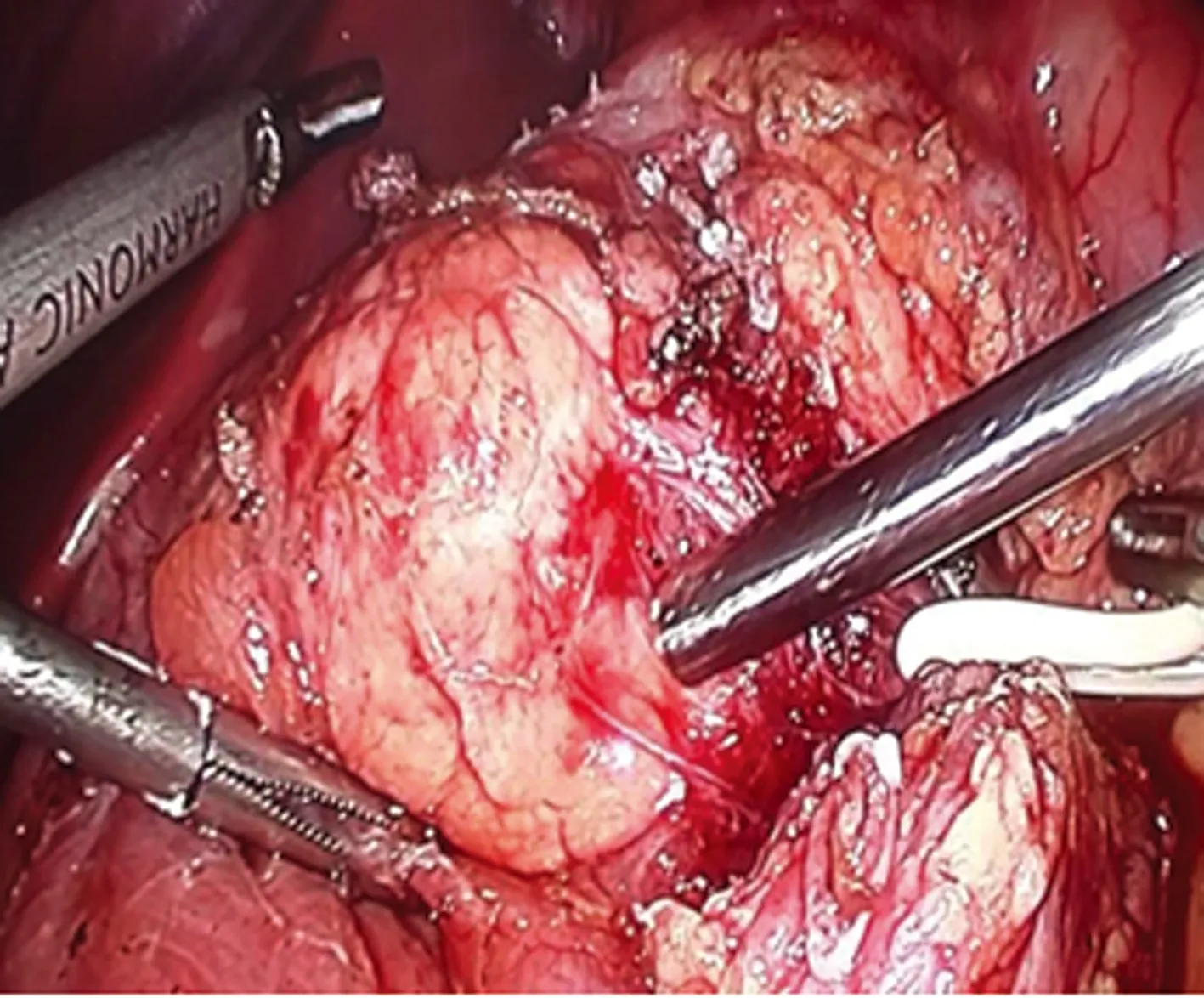
图2 腹腔镜下胰头部肿瘤切除术
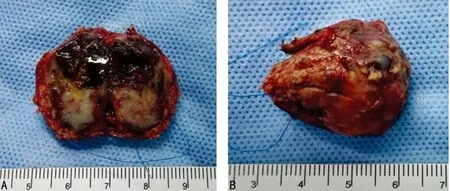
A:瘤体背面;B:瘤体正面
图3 肿瘤实体
术后病理检查,苏木精-伊红(HE)涂片见肿瘤细胞大小基本一致,可见局部假乳头形成,未见明显异形细胞,未见明确坏死,肿瘤组织周边包膜完整(图4);免疫组织化学结果提示:广细胞角蛋白(CK)阴性,波形蛋白(Vim)阳性,CD10阳性(局灶),Syn阳性,上皮膜抗原(EMA)阳性(局灶),S-100阴性,甲胎蛋白(AFP)阳性,癌胚抗原(CEA)阴性,雌激素受体(ER)阴性;特殊染色:ABPAS阳性(少许酸性黏液),未见肿瘤细胞(图5)。
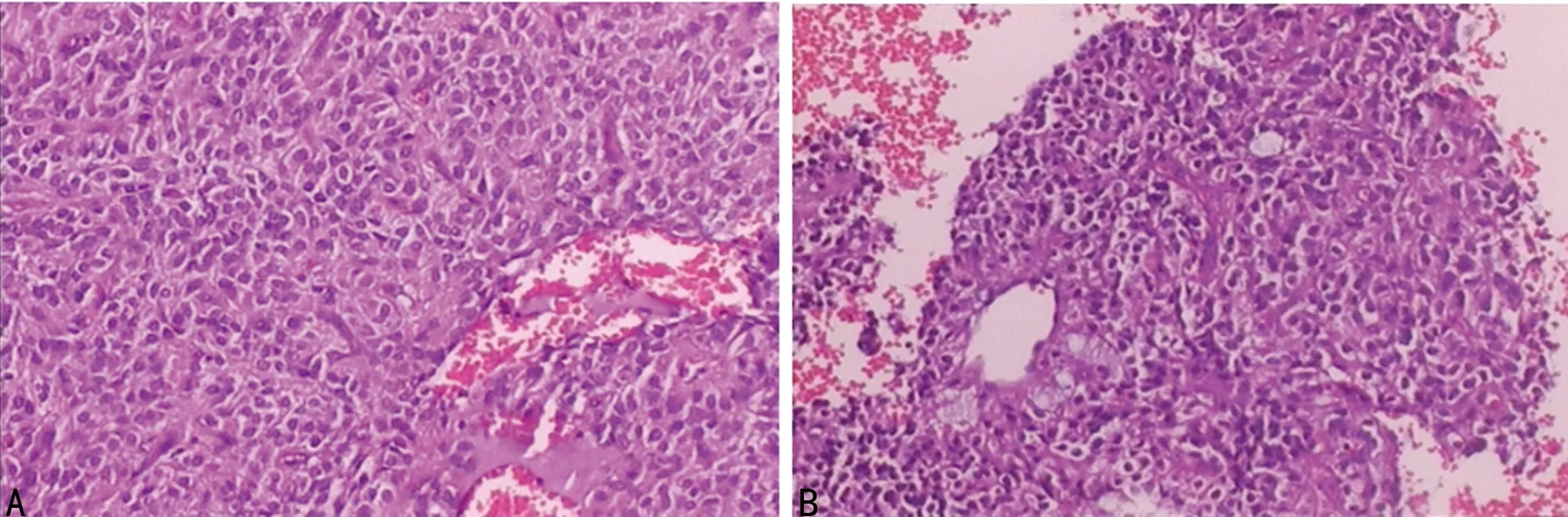
A:瘤体浅部组织;B:瘤体深部组织
图4 肿瘤组织HE染色(10×10)
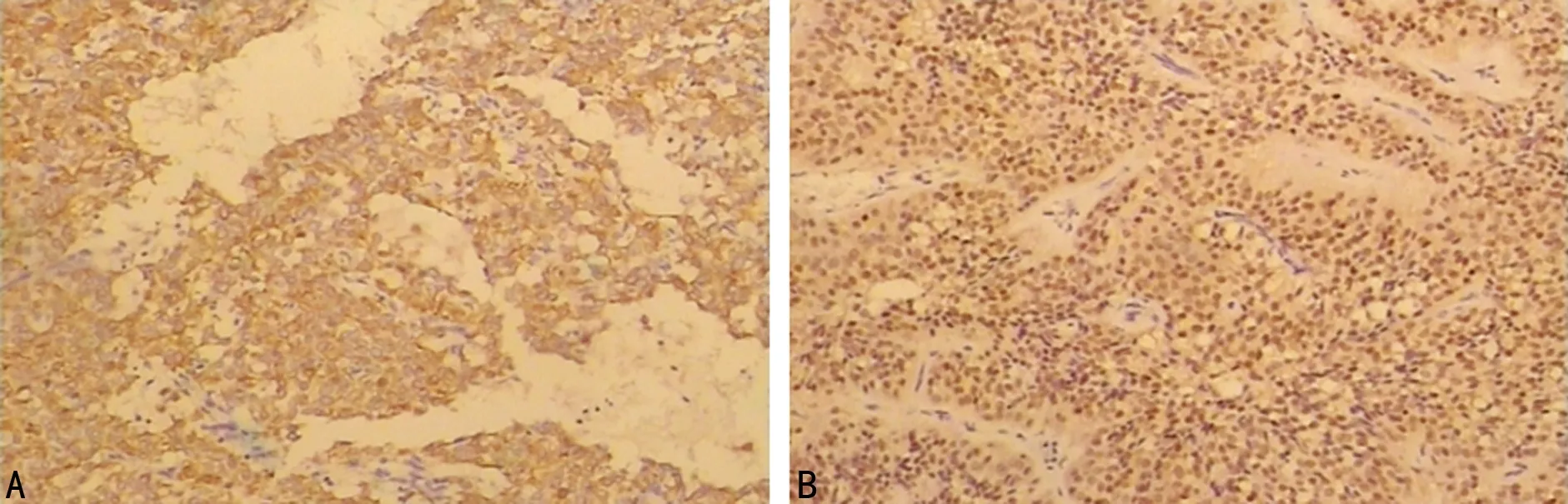
A:瘤体浅部组织;B:瘤体深部组织
图5 肿瘤组织免疫组织化学染色(×20)
术后前5 d经深静脉以全胃肠外营养(TPN)为主,同时予以生长抑素抑制胰酶分泌,监测血糖及血淀粉酶波动情况,患者术后第4天血淀粉酶基本控制在正常范围内,血糖波动在6~10 mmol/L。术后1周逐步减少TPN,增加肠内营养(EN)。患者胰腺头部手术区域引流液于术后6 d基本引流干净,拟拔出引流管,但于术后第8天突然引流出鲜红色血液约100 mL,怀疑因胰液腐蚀手术创面周围组织血管所致,立即经窦道行内镜检查,明确出血来源于胰头部创面一细小滋养血管渗血(图6),并于镜下顺利止血后经窦道填塞加压包扎,术后2周窦道完全闭合痊愈,期间患者未诉腹痛不适,复查血常规及血淀粉酶正常。患者于术后9 d进食后出现腹胀不适,伴反复呕吐,呕吐物系进食的食物残渣,行上消化道碘水造影提示轻中度胃潴留,遂进一步完善电子内镜见十二指肠球部及降段水肿并成角,内镜无法顺利进入十二指肠远端,遂在内镜下植入空肠营养管行全肠内营养(图7),术后2周间断夹闭空肠营养管,术后18 d再次行上消化道碘水造影未见明显胃潴留,造影剂顺利经十二指肠进入空肠,遂拔出空肠营养管嘱患者由流质饮食逐步恢复正常饮食,期间未再出现腹胀、呕吐等,并于术后3周康复出院。
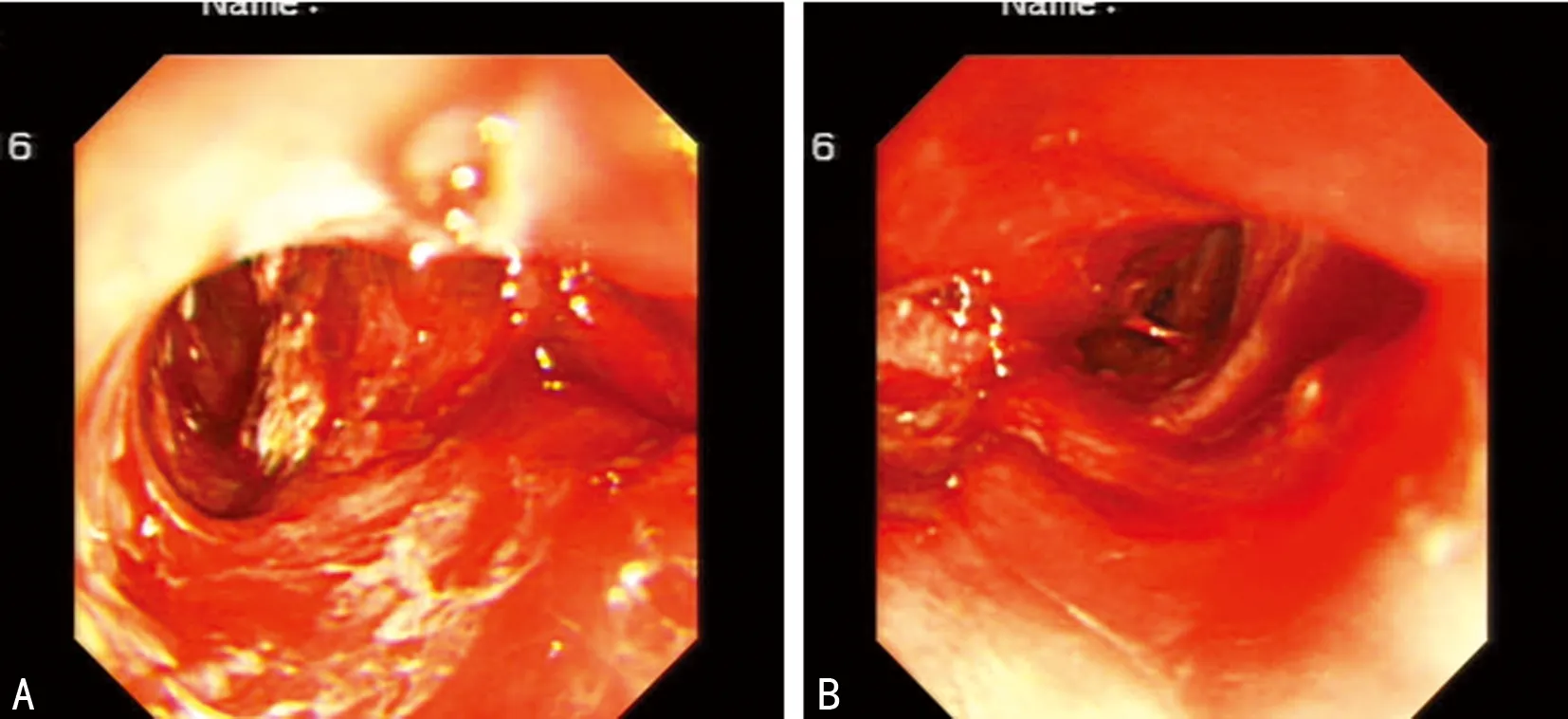
A:窦道内壁;B:窦道底胰头部渗血面
图6 经窦道行内镜检查
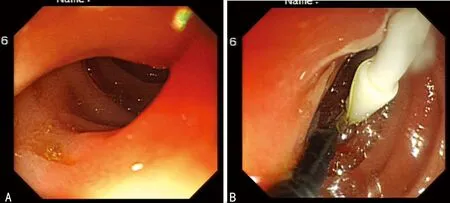
A:十二指肠降段内壁水肿;B:经十二指肠降段置空肠管
图7 内镜下植入空肠营养管行全肠内营养
2 讨 论
目前关于SPN的发病原因并不清楚,其组织学来源也存在很大争议,国外学者CAMPBELL等[2]指出SPN可能起源于胰腺干细胞;同样TIEN等[3]的研究也指出SPN可能来源于胰腺原始多能干细胞或胰腺的胚胎神经嵴细胞。虽然发病机制不明,但大多数学者认为该肿瘤多为良性病变,预后较好,且多发于青春期女性。
儿童SPN早期多无明显表现,部分患儿系体检中发现,其早期诊断主要依赖于多层螺旋CT(MSCT)检查,其影像学表现为肿瘤均呈囊实性,但比例不一,增强后肿瘤实性部分强化,且门静脉持续性强化,囊性部分均不强化[4]。与CT相比,MRI不是常规检查手段,但在显示SPN内部组织结构及肿瘤与周围组织关系方面,如有无囊内出血、周围组织及血管侵犯等,特别是儿童胰腺组织发育尚不健全且供血单一,术前行MRI对手术方式的选择具有重要意义[5]。
SPN有潜在恶变可能,据HUFFMAN等[6]研究表明,SPN行外科手术后5年存活率高达98%,而保守治疗5年存活率为40%,且预后与年龄、性别、有无转移等相关。国内研究也表明,儿童SPN中,女性明显多于男性,男女比约1∶2[7];同时年龄可作为判定儿童胰腺肿瘤恶性程度及预后的指标:年龄越小(≤6岁),患高度恶性肿瘤的概率越大,预后差;年龄越大(12~18岁),患低度恶性肿瘤的概率越大,预后好。
结合本病例,手术切除是治疗的唯一有效方法。胰头部的SPN因其位置特殊,位于胆道、胰腺及十二指肠三者交汇处,依据肿瘤的大小、侵犯范围及包膜是否完整等,手术方式可分为胰头肿块剜除术、保留十二指肠胰头切除术(DPRHP,又称Beger术)、保留幽门的胰十二指肠切除术(PPPD)。本病例中,患者肿瘤较小,包膜完整,且无明显周围组织侵犯,故采取局部剜除术,最大可能保留胆道及胃肠道的完整性,不但能减少手术创伤,改善远期生活质量,同时也符合当前手术切除SPN的主流原则[8]。但考虑到儿童依从性较差,各方面发育尚未健全,故术后并发症及恢复可能较成人复杂多变。
本病预后良好,是一种少见的低度恶性或具有潜在恶性的肿瘤,R0切除后5年存活率高,但仍建议短期随访,随访周期为1年,随访时间为3~5年[9]。但部分国内学者建议以下情况时则需长期随访:(1)非根治性切除;(2)巨大肿瘤;(3)年轻男性及儿童;(4)术中出现肿瘤破裂或术中探查存在周围神经、血管浸润,周围胰腺实质浸润[10]。



