刘晓洁,杨静薇,彭 红,叶 虹△
(1.重庆医科大学附属妇女儿童医院/重庆市妇幼保健院生殖医学中心,重庆 400013;2.重庆市生殖与遗传研究所,重庆 400013)
甲状腺功能减退(以下简称“甲减”)是由于甲状腺激素(TH)分泌缺乏或作用缺陷所导致的一种全身低代谢综合征,是目前最常见的甲状腺疾病,以女性多见。大量研究报道了妊娠期甲减对胎儿及新生儿均有不良影响,如死胎、流产、胎盘早剥、宫内发育迟缓、低出生体重儿及早产儿发生率增加,少数还可引起新生儿甲状腺功能亢进或减退,重者可危及生命或造成神经、心理、体格、智力发育异常[1-4]。2018年公布的中国育龄夫妇中不孕不育症的发病率为25%,借助辅助生殖手段帮助妊娠的育龄夫妇也在逐年增加[5]。女性的不孕不育又与生殖-内分泌轴息息相关,且已证实甲减与女性不孕不育相关,体现在生殖调节的各个阶段[6]。促甲状腺激素(TSH)在胎儿的生长和神经发育中起着至关重要的作用,这取决于从妊娠早期开始母体TH的充足供应[7]。故母体TH、抗甲状腺抗体水平对胎儿大脑及全身发育均有极大的影响。但针对甲减人群的新生儿TSH研究却鲜少有报道。本文研究患有甲减的不孕症女性在辅助生殖助孕中的助孕结局和新生儿TSH水平,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2016年6月至2022年12月在本院生殖医学中心行辅助生殖技术(assisted reproductive technology,ART)助孕,并在首个新鲜移植周期获得单胎活产的6 279例女性患者资料。纳入标准:(1)年龄20~45岁;(2)BMI 18~28 kg/m2;(3)无糖尿病、高血压等其他内分泌疾病病史。排除标准:(1)胚胎植入前遗传学检测(PGT)的不孕症患者;(2)促排卵采取微刺激/自然周期或黄体期促排卵方案者。共251例助孕女性患者在体外受精期间确诊甲减(诊断参照《成人甲状腺功能减退症诊治指南》),将其中在本院新生儿筛查中心完成新生儿TSH筛查的108例患者设为甲减组。通过倾向评分匹配(PSM)统计方法,按照上述纳入排除标准匹配同期ART助孕无甲减的患者设为对照组,共539例。本研究符合《赫尔辛基宣言》关于医学研究的基本原则,并获得本院生殖医学伦理委员会审批[伦审(研)2022-RGI-13号]。
1.2 方法
1.2.1治疗方法
1.2.1.1控制性促排卵
所有ART助孕患者由本中心高年资医师根据患者年龄、卵巢功能及BMI综合评估后个性化制订促排卵方案。方案主要包含:(1)促性腺激素释放激素(GnRH)激动剂方案。从黄体中期开始用GnRH-a(德国Ferring GmbH公司)0.1 mg/d或0.05 mg/d,14~21 d,垂体下调。降调节达标标准:孕酮(P)<0.9 ng/mL,雌二醇(E2)<30 pg/mL,黄体生成素(LH)<5 mIU/mL;然后通过皮下注射促性腺激素(Gn)诱导排卵,剂量为75~300 IU/d。(2)GnRH拮抗剂方案。从月经周期的第2~4天开始,当两个卵巢的窦卵泡直径小于0.5 cm,子宫内膜厚度小于0.5 cm时,注射75~300 IU Gn以启动促排,满足:①至少有1个卵泡大于14 mm;②血清雌激素水平>600 pg/mL;③血清LH水平>10 IU/L给予GnRH-ant(瑞士默克雪兰诺公司)0.25~0.50 mg/d直至扳机。所有患者都通过经阴道超声和血液标本观察卵泡生长情况。当2个或更多的优势卵泡直径达到18 mm时,注射250 μg重组人绒毛膜促性腺激素(rhCG,意大利默克雪兰诺公司)进行扳机。扳机后36~38 h进行经阴道排卵。
1.2.1.2胚胎培养及移植
所有胚胎均在Time Lapse时差培养箱中培养观察,自取卵后开始黄体支持,阴道用黄体酮凝胶90 mg/d或软胶囊0.2 g,每天3次,同时口服补充地屈孕酮片20 mg/d,取卵后第3天返院进行新鲜周期胚胎移植手术。
甲减组患者给予左旋甲状腺素片(商品名:优甲乐,德国默克公司),起始剂量25~50μg,根据每2~4周复测TSH及游离甲状腺素水平调整药物剂量,直至TSH达到正常水平,持续用药随访至分娩后。对照组常规孕检及产后随访。
1.2.2观察指标
主要观察指标:新生儿足跟血TSH水平;次要观察指标:获卵数、成熟卵数、2PN受精率、可移植胚胎数、孕周、分娩方式、新生儿性别、出生体重及身长。
1.3 统计学处理
2 结 果
2.1 两组一般资料比较
本研究共纳入647例单胎活产且有新生儿结局的ART助孕患者,其中甲减组108例,PSM配对同期单胎活产的ART助孕无甲减的患者539例(对照组)。研究对象纳入流程图,见图1。两组年龄、不孕年限、BMI、血清AMH、不孕类型、Gn总量及窦卵泡数无明显差异(P>0.05),见表1。
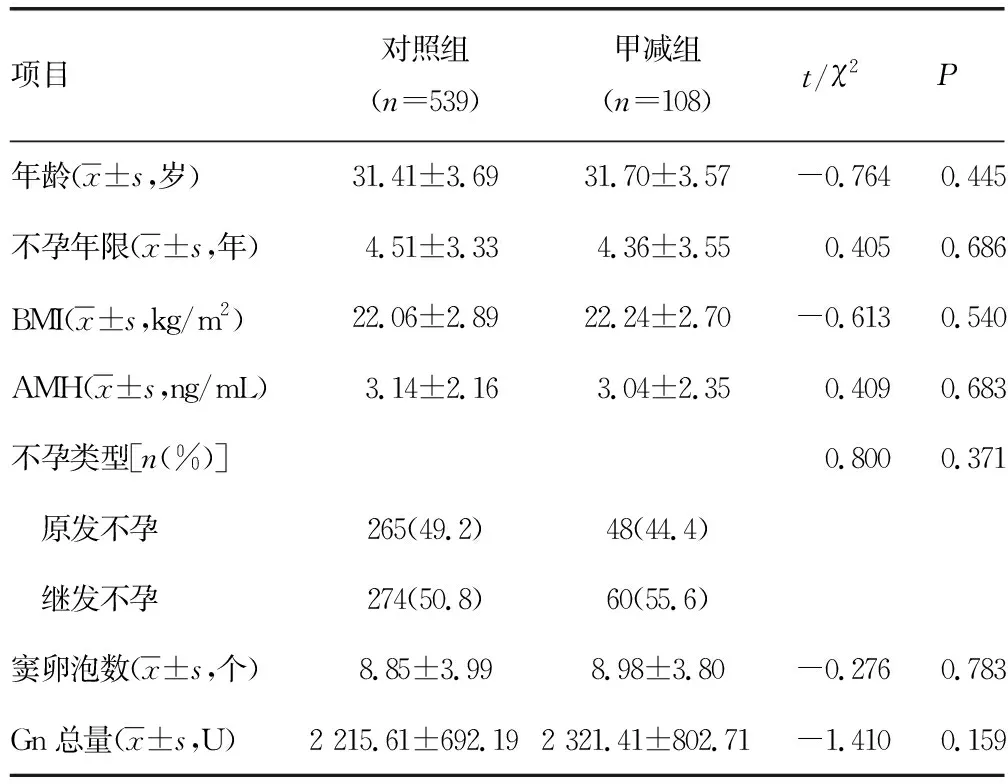
表1 两组患者一般资料比较

图1 研究对象纳入流程图
2.2 两组体外受精助孕结局比较
两组获卵数、成熟卵数、2PN受精率及可移植胚胎数比较,差异均无统计学意义(P>0.05),见表2。

表2 两组体外受精助孕结局比较
2.3 两组新生儿结局比较
甲减组孕周和新生儿出生体重均小于对照组,差异有统计学意义(P<0.05);两组分娩方式、新生儿性别、出生身长及新生儿TSH比较,差异均无统计意义(P>0.05),见表3。甲减组有2例新生儿发生甲减,对照组有6例新生儿发生甲减。
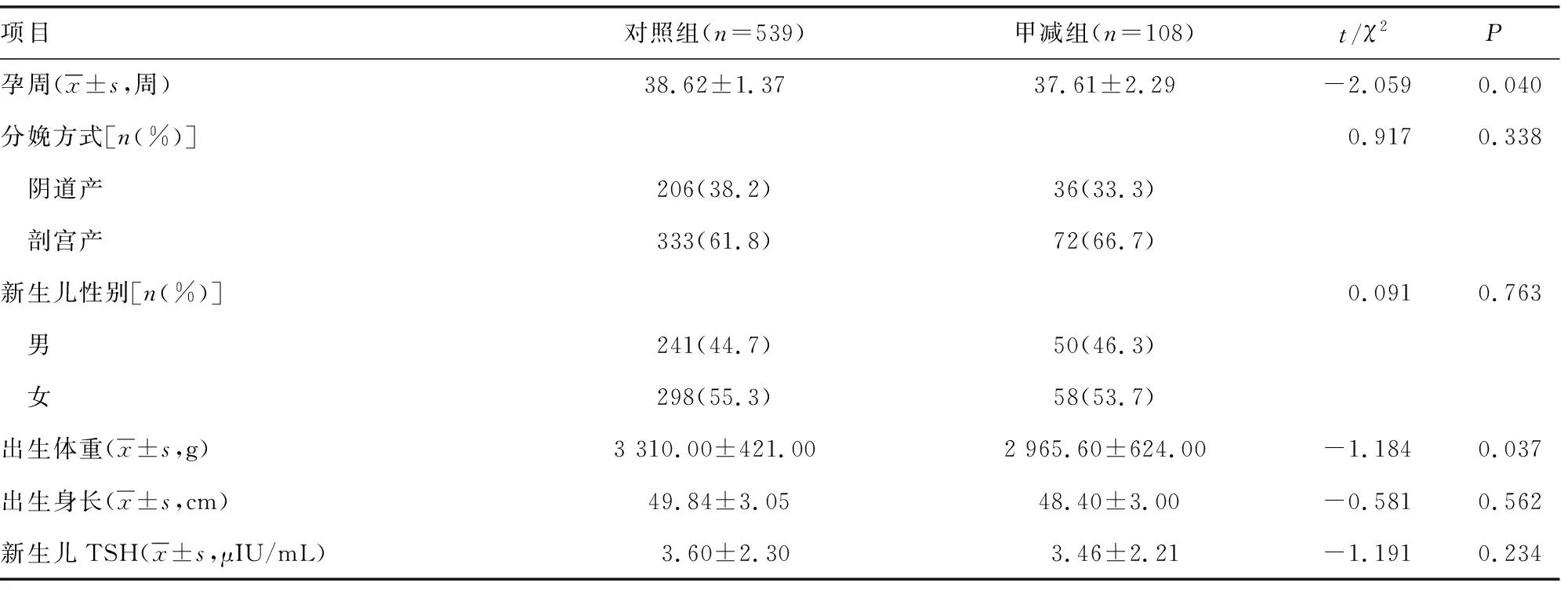
表3 两组新生儿结局比较
3 讨 论
甲状腺激素参与调节女性生殖的各个阶段,从卵泡发育成熟到卵子排出,再到授精、着床、继续妊娠直至足月分娩。甲状腺激素与卵泡刺激素(FSH)协同作用,对颗粒细胞的分化和功能产生刺激作用,从而参与了排卵和随后的黄体形成。近期有研究表明,孕前3个月的TSH水平与辅助生殖助孕的临床妊娠率无明显相关性[8]。一项病例对照研究纳入了137例接受左旋甲状腺素治疗的甲减妇女和274例年龄匹配的甲状腺功能正常对照,结果表明接受充分治疗的甲减与辅助生殖助孕后的着床率、临床妊娠率或活产率无关[9]。但也有证据表明,接受辅助生殖技术的亚临床性甲减女性可能受益于甲状腺素(TH)的补充治疗[10]。本研究经PSM匹配,排除了年龄、BMI、AMH、不孕类型等影响因素后,两组获卵数、成熟卵数、2PN受精率及可移植胚胎数无明显差异。这与之前报道一致,均说明通过充分有效的治疗,甲减女性具有同甲状腺功能正常女性一样的辅助生殖助孕结局。
胚胎甲状腺在妊娠10~11周产生少量TH,约在妊娠20周时,胎儿下丘脑-垂体-甲状腺轴功能成熟后,胎儿产生的TH才会增加。胎儿的甲状腺功能在孕12周才开始集中碘合成甲状腺素,故整个孕期胎儿的甲状腺素合成都依赖母体的甲状腺功能[1]。从妊娠早期开始,胚胎和胎儿的发育过程都需要TH,其在骨、骨骼肌及神经系统的发育中可促进蛋白质合成,参与胎儿及新生儿的生长发育。本研究发现,甲减组女性ART后代的孕周及出生体重较对照组低,但两组分娩方式、新生儿性别及出生身长无明显差异。既往研究报道,早产是甲减孕妇的妊娠并发症之一[11-13]。还有报道指出,孕妇甲减和亚临床性甲减与流产、早产和儿童认知能力评估评分较低有关[14]。而在一个横跨10年样本量8 413例的回顾性研究中发现,甲减患者TSH>4 mIU/L与低出生体重的相对危险度增加有关[15]。但也有研究报道,甲减孕妇与新生儿低体重无明显相关性[16]。本研究结果显示,甲减组孕妇的新生儿出生体重低于正常甲状腺功能孕妇,这也与孕周息息相关。2021年的一项meta分析报道,正常高值TSH组与正常低值TSH组对比,临床妊娠率、活产率、新生儿出生体重及胎龄相似[17],不过该meta分析的研究对象是正常甲状腺功能人群,分为TSH>2.5 mIU/L组和TSH≤2.5 mIU/L组,与本研究纳入人群并不一致。本文的新颖点在于探究甲状腺功能异常的孕妇对其新生儿甲状腺功能的影响。已有文献报道,孕妇TH在整个孕期可通过胎盘屏障,TSH受体抗体从妊娠中期通过胎盘屏障,这可能会引起胎儿或新生儿短暂性甲状腺功能亢进或减退[18]。但甲减孕妇中研究新生儿TSH的报道却很少。
一项来自中国15 615例新生儿的研究发现,新生儿先天性甲减的发生率与胎龄和出生体重有关[19]。另一项研究报道显示,胎龄及母亲妊娠合并甲减是早产儿发生高TSH血症的危险因素,且母亲妊娠合并甲减亦是足月儿发生高TSH血症的危险因素[20]。本研究收集了108例甲减女性患者的新生儿TSH,结果显示甲减组和对照组无明显差异。分析新生儿TSH未受到影响的可能的原因:(1)ART助孕中发现甲减的女性,孕前就开始服药,且多数能在孕期坚持随访甲状腺功能直至正常。而经治疗的甲减女性孕育的后代,发生低体重和神经智力发育异常的风险增加[21]。(2)由于胎盘脱碘酶的优势,人类胎盘对TH具有适度的渗透性,它可以使从母体到胎儿循环的大部分TH失活[22],从而使胎儿下丘脑-垂体-甲状腺轴的发育相对独立于母体的影响。有研究报道,在诊断为亚临床性甲减或低甲状腺素血症的孕妇中,新生儿TSH水平与孕母是否外源性补充甲状腺激素无明显相关性[23]。
尽管目前不支持甲减母亲生育甲状腺功能异常新生儿的研究比例升高,但仍需关注甲减母亲的新生儿尤其早产儿的甲状腺功能,并长期随访。因为,早产儿更容易出现迟发性的甲状腺功能障碍[24]。尤其对于辅助生殖助孕的婴儿,虽然其新生儿筛查试验TSH结果正常,但促甲状腺激素释放激素试验发现TSH反应存在持续性和延迟性[25]。虽然曾有国外研究报道对甲减孕妇分娩的新生儿行甲状腺功能复检,并未发现临床额外获益[26]。但是甲减孕妇其后代未来发生甲状腺功能疾病的风险仍值得进一步深入研究。
综上所述,本研究发现甲减女性即使通过孕前药物干预和孕期的充分治疗,仍可能出现早产风险增加和较低的新生儿出生体重。尽管如此,对于有明显甲减的女性,妊娠期间适当的TH替代治疗可将不良后果的风险降到最低[27]。笔者建议预防甲减女性的妊娠并发症,还应加强产科保健,平衡孕妇营养摄入,必要时补充益生菌,避免孕期体重过低,同时控制好甲状腺功能异常。



