汪贵香
(湖北省天门中学,湖北 天门 431700)
得失电子守恒,攻克氧化还原的金钥匙
汪贵香
(湖北省天门中学,湖北 天门 431700)
得失电子守恒在化学计算题中的应用非常广泛,它往往是解决化学难题的简便方法.其中得失电子法,在有关氧化还原的计算中应用很多,学生在解题过程中若能发现隐藏在题目中的守恒规律,将可以大大提高解题效率.
得失电子;守恒;氧化还原
应用得失电子法解决氧化还原难题,守恒法的重要解题规律.准确找出还原剂与氧化剂,并利用它们的得失电子数确定等量关系,是解决此类题型时的关键.本文主要从三个方面对得失电子法在氧化还原中的应用进行阐述.
1.确定元素化合价
确定元素的化合价,是氧化还原反应中有关电子守恒的考点.解决此类问题时需弄清楚氧化剂和还原剂中得失电子的元素,再根据已知的得到的电子数(失去的电子数)元素,确定未知的元素的化合价.
例1 现有12mL的Na2SO3溶液,其浓度为0.1mol/L,当它恰好与0.04mol/L的K2Cr2O7溶液反应时,消耗的K2Cr2O7的体积为10mL,试着计算铬元素在还原产物中的化合价.
分析Na2SO3溶液在K2Cr2O7溶液中发生氧化还原反应,且Na2SO3作为还原剂存在,当1mol的Na2SO3失去2mol电子时,K2Cr2O7得电子,由于同一反应中各物质的得失电子数相等,根据此定理可进行相关计算.
解假设Cr在还原产物中的化合价为x,由得失电子守恒定律可得:12×10-3L×0.1mol/L×(6-4)=10×10-3L×0.04mol/L×2×(6-x).经计算解得:x=+3价,因此,Cr在还原产物中的价态为+3价.
评注本题考查化学反应中的得失电子守恒规律,同一化学反应中,氧化物得到的电子数与还原剂失去的电子数相等.本题中可以根据S原子失去的电子数与Cr原子得到的电子数相等,根据二者的关系可求得Cr的化合价.
2.参与反应的氧化剂与还原剂的质量或物质的量
在某些氧化还原反应中,有些化学物质在作氧化剂或还原剂的同时,还体现出其他性质.因此在书写化学反应方程式或者计算氧化剂与还原剂之时,需要根据得失电子守恒的规律去做.用这种方法不但可以使得解题过程简单明了,而且可以大大提高准确率.
例2 稀HNO3与足量的Fe反应的化学方程式如下:

已知生成的NO的体积为11.2L,试计算参与反应的Fe的质量和被还原的HNO3的物质的量.
分析此反应中,Fe为还原剂,稀HNO3既作氧化剂又作还原剂.根据化学方程式可知被还原的硝酸变成2个NO,又知总的硝酸为8个,因此,参与还原的HNO3为2个.通过相关的计量关系可求得Fe的质量及HNO3的物质的量.
解假设参与反应的Fe的质量为m,被还原的HNO3物质的量为n,根据以2HNO3~2NO 下计量关系可知:
3Fe ~ 2HNO3(被还原) ~ 2NO
3×56g ~ 2mol ~ 2×22.4L
m~n~ 11.2L
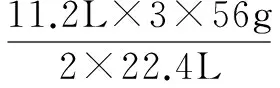
评注硝酸与金属的反应,是有关氧化还原反应计算题的典型例题.由于硝酸的可以还原为多种价态,且硝酸既具有氧化性又有酸性,因此,一般涉及到硝酸的计算题都比较复杂.计算这类计算题时,使用电子守恒法可大大简化计算过程,同时也可以大大提高解题效率.
3.确定化学反应的计量数
计算化学反应计量数,是化学反应方程式配平题型中的一种.计量数的确定,可以通过化学反应中得失的数目确定.尤其对于较复杂的化学反应,应用得失电子守恒法,不但可以缩短解题时间,而且可以大大提高解题的正确率.

A.2 B.4 C.6 D.9
分析此化学反应中M作为还原剂失去电子,O2作为氧化剂得到电子.又因为同一化学反应中,氧化剂得到的电子数与还原剂失去的电子数相等,因此可知,M失去的电子数与O2得到的电子数相等.
解本题由得失电子守恒可得:2×[0-(-2)]=x×(2-0),经计算可得x=2,因此本题中M2+前面得化学计量数x为2.
评注计算化学反应式中某元素前的计量数,是关于得失电子题型中的主要考查点.学生解决本题的关键是利用得失电子的数目,建立一个等量关系.确定好此等量关系后,这类题目便可迎刃而解.
综上所述,得失电子守恒规律,在高中化学学习的过程中应用极其广泛,得失电子守恒规律,往往是解决某些化学计算题的有效捷径.应用得失电子守恒法解题,在节约时间的同时还可以大大提高解题正确率.
[1]周素珍.浅析电子守恒原理在氧化还原反应中的应用[J].现代阅读(教育版),2013(10).
[2]郭以飞.例析得失电子守恒在解题中的应用[J].教育教学论坛,2010(29).
[责任编辑:季春阳]
G632
A
1008-0333(2017)25-0095-02
2017-07-01
汪贵香(1983.06-),女,湖北黄冈,中一,大学本科,从事高中化学教学.



