肖文武,方汉卿
1.湖北省十堰市竹溪县人民医院血液内科,湖北十堰 442300;2.华中科技大学同济医学院附属同济医院血液内科,湖北武汉 430000
急性淋巴细胞白血病是一种恶性增殖性疾病,其本质主要为骨髓超负荷产生异常原始、幼稚淋巴细胞,且在患者的外周血中释放,对患者的其他组织器官产生浸润[1]。急性淋巴细胞白血病主要好发于儿童群体,有大约2/3的急性淋巴细胞白血病患者都是儿童。有研究指出,每十万名儿童当中就有3~4名儿童患有急性淋巴细胞白血病,患病的高峰年龄为2~5岁,该疾病对患儿的生命健康产生了严重的威胁[2]。目前,针对急性淋巴细胞白血病的治疗方案主要为阿糖胞苷联合蒽环类抗菌药物,其治疗效果较为理想[3]。但是因为化疗药物存在一定的不良反应,且长时间用药会发生药物耐药性,导致高剂量的化疗药物在临床治疗中应用受限,且还有部分白血病患者因为难治及复发而发生死亡。利妥昔单抗属于人-鼠嵌合抗单克隆抗体(CD20),在对血液类疾病患者的治疗过程中被广泛应用。本研究旨在观察利妥昔单抗联合阿糖胞苷对急性淋巴细胞白血病患儿的临床疗效及不良反应发生的影响,现报道如下。
1 资料与方法
1.1一般资料 选取2016年5月至2017年5月华中科技大学同济医学院附属同济医院收治的90例急性淋巴细胞白血病患儿为研究对象。纳入标准:(1)符合急性淋巴细胞白血病的诊断标准[4]者;(2)年龄在2~5岁者;(3)临床资料齐全者;(4)完成随访者;(5)入组研究前未接受其他临床治疗及干预者。 排除标准:(1)患其他种类的白血病者;(2)合并感染者;(3)既往接受过造血干细胞移植及抗体治疗者;(4)合并自身免疫性溶血性贫血者;(5)晚期恶性肿瘤者;(6)合并免疫类疾病者;(7)合并严重的基础类疾病者,如高血压、心脏病等。纳入研究者依据治疗方式分成对照组和研究组,每组45例。对照组中,男29例,女16例;年龄2~5岁,平均(3.1±0.9)岁。研究组中,男28例,女17例;年龄2~5岁,平均(3.2±0.5)岁。两组的一般资料比较,差异无统计学意义(P>0.05),有可比性。本研究获取华中科技大学同济医学院附属同济医院医学伦理委员会许可。
1.2方法 对照组应用阿糖胞苷治疗。给予患儿静脉滴注,2.0 g/m2,2次/天,用法:每间隔1 d进行注射,每6次属于1个治疗疗程,给予患儿实施4个疗程的治疗。研究组在对照组的基础上联合应用利妥昔单抗。给予患儿连续静脉滴注4周,375 mg/m2,1次/周,每间隔28 d给予患儿1次重复给药。用法:在无菌环境下,抽取治疗所需要剂量的药物,在无致热源、无菌的输液袋(5%葡萄糖溶液或者0.9%生理盐水)中将其稀释至1 mg/mL。将注射袋颠倒,混合溶液的过程中避免出现泡沫。在经验丰富的血液科医生及肿瘤科医生的监督指导下实施临床治疗。在治疗过程中,若发生严重的呼吸困难、严重的低氧血症及严重的支气管痉挛,需要立即停止用药,同时还需要定时评估患儿在治疗过程中是否发生肿瘤溶解综合征。在整个治疗过程中必须严密、严格地监测两组患儿各项指征,对患儿实施常规的止吐、水化、保肝等相关干预治疗;指导患儿注意个人卫生,降低发生感染的风险;在治疗过程中,每2天对患儿进行1次血常规的检测,每7天对患儿进行1次肾功能及肝功能的检测。
1.3观察指标
1.3.1治疗有效率 疗效评估的依据为患儿的临床症状、血常规指标及骨髓细胞学检测指标。显效:经治疗后,患儿的相关临床症状全部消失。血常规指标方面:男性患儿外周血血红蛋白(Hb)水平≥100 g/L,女性患儿外周血Hb水平≥90 g/L,且没有出现任何的白血病细胞。骨髓细胞学检测指标方面:Ⅰ型原粒细胞+Ⅱ型原粒细胞总和≤5%,巨核细胞水平正常。有效:经治疗后,患儿的临床症状较治疗前发生明显改善。血常规指标方面:男性患儿外周血Hb水平<100 g/L,女性患儿外周血Hb水平<90 g/L。骨髓细胞学检测指标方面:Ⅰ型原粒细胞+Ⅱ型原粒细胞总和范围为5%~20%。无效:经治疗后,患儿的临床症状较治疗前未发生明显缓解,且经过血常规指标及骨髓细胞学检测指标检查结果提示,均未达到有效及显效标准[5]。有效率=(显效例数+有效例数)/总研究例数×100.0%。
1.3.2不良反应发生情况 比较两组治疗过程中的药物相关不良反应发生情况。
1.3.3无进展生存率及生存率 生存率从患儿接受治疗开始计算时间,直至本次研究的最终随访时间或者患儿死亡。无进展生存率从患儿接受治疗开始计算时间,直至本次研究的最终随访时间或者患儿的病情出现进展、恶化。本次研究的最终随访时间为2年。
2 结 果
2.1两组治疗有效率 研究组治疗有效率为88.9%,明显高于对照组的68.9%,差异有统计学意义(P<0.05),见表1。

表1 两组治疗有效率
2.2两组治疗过程中的药物相关不良反应发生情况 两组在整个治疗过程中并没发生严重的肝衰竭、肾衰竭、肿瘤溶解综合征等相关不良反应。两组在治疗过程中发生的药物相关不良反应主要为骨髓抑制,对照组的发生率为57.8%,研究组的发生率为60.0%,两组比较,差异无统计学意义(P>0.05)。非血液毒性不良反应主要为胃肠道反应,包括呕吐及恶心等,对照组的发生率为37.8%,研究组的发生率为40.0%,两组比较,差异无统计学意义(P>0.05)。两组在药物相关不良反应的发生情况方面比较,差异均无统计学意义(P>0.05),见表2。
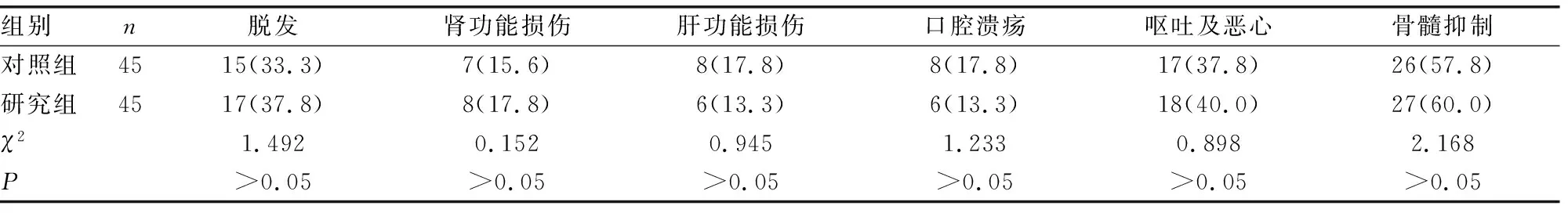
表2 两组治疗过程当中的药物相关不良反应发生情况[n(%)]
2.3两组无进展生存率及生存率比较 研究组1年无进展生存率、1年生存率、2年无进展生存率及2年生存率均高于对照组,差异有统计学意义(P<0.05),见表3。
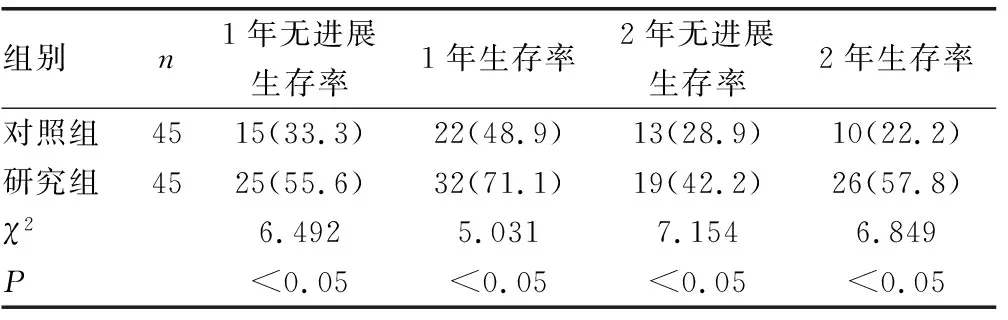
表3 两组无进展生存率及生存率比较[n(%)]
3 讨 论
阿糖胞苷属于嘧啶类的抗代谢药物,研究已经证实,阿糖胞苷在白血病细胞中具有明显细胞毒作用,因此成为治疗急性淋巴细胞白血病患者常用及首选药物之一[6]。阿糖胞苷进入机体后,能够在血液中迅速且大量地发生脱氨基,转变为没有活性的阿糖尿苷[7]。仅有少量的阿糖尿苷进入到细胞中,在磷酸酶的辅助催化作用下,形成三磷酸胞苷。三磷酸胞苷既能够对合成DNA多聚酶产生阻断作用,同时还能掺入DNA片段中,对肿瘤细胞生长产生抑制效果[8]。
利妥昔单抗属于IgG1免疫球蛋白(人鼠嵌合型),是通过在鼠细胞相应基因中转染后表达的一种基因产物,其包括1 328个氨基酸,其结构主要包括人IgG-Fc片段抗体及鼠抗CD20单克隆抗体可变区Fab[9]。其中,CD20抗原跟鼠源性Fab的可变区之间具有较高的亲和力。利妥昔单抗的特点主要包括以下几方面:不同效应细胞与人IgG-Fc片段抗体之间的亲和力较高,能够对正常宿主效应的功能产生介导作用。半衰期比单纯的鼠抗体更长[10]。能够抑制人抗鼠抗体的产生。在肿瘤B细胞及正常细胞中,人B淋巴细胞CD20抗原均出现高水平表达;主要在成熟B淋巴细胞及前B细胞中表达,但是在原浆细胞及多能干细胞当中并没有出现表达[11]。由此可知,利妥昔单抗与恶性B淋巴细胞及正常细胞中的CD20受体相互反应,但不会与任何其他非造血细胞组织,如干细胞、树突状细胞及单核细胞发生反应,特异度更高,针对性更强,从而使得其治疗疗效显着[12]。
本研究结果显示,研究组治疗有效率高于对照组,差异有统计学意义(P<0.05);研究组的1年及2年无进展生存率及生存率均高于对照组,差异有统计学意义(P<0.05);两组在药物相关不良反应的发生情况方面差异均无统计学意义(P>0.05)。提示联合利妥昔单抗及阿糖胞苷治疗急性淋巴细胞白血病患儿,可明显提高患儿的临床有效率及生存率,且不会额外增加患儿发生严重不良反应的风险。



