刘 艳,帅玉婷,涂娇子,刘 云,应志兰
南昌大学第二附属医院:1.心脏大血管外科ICU;2.耳鼻喉科;3.肾内科,江西南昌 330006
冠状动脉旁路移植(CABG)是心脏外科常见的治疗手段之一,而股动脉体外膜肺氧合(ECMO)辅助治疗作为一种过渡性的体外心肺功能支持手段,可代替心脏泵血,为CABG术后出现呼吸、循环衰竭的患者提供血液循环和呼吸循环支持,从而为患者心功能恢复或接受更高级别的后续治疗赢得抢救时间[1-3]。相关研究指出,虽然ECMO治疗拯救了大量心脏外科手术患者的生命,但采取ECMO治疗患者住院期间的病死率也非常高[4-5],这表明部分患者并未从ECMO治疗中获益。因此,为提高CABG术后患者预后,本研究探讨了CABG术后接受股动脉ECMO治疗患者的预后不良的危险因素。现将结果报道如下。
1 资料与方法
1.1一般资料 回顾性分析本院2020年1月至2022年10月接受股动脉ECMO治疗的200例CABG术后患者的临床资料。按照患者最终结局(顺利出院为观察终点)分为生存组(112例)和死亡组(88例)。纳入标准:符合CABG的手术指征且顺利完成手术治疗;接受股动脉ECMO辅助治疗;临床资料完整;CABG术后出现心脏骤停、多器官衰竭等。排除标准:股动脉ECMO治疗后24 h内死亡患者;因气道梗阻采取ECMO预防性治疗患者;存在不可逆的中枢神经损伤,终末期多器官衰竭患者;中途自动退出患者。
1.2方法
1.2.1序贯器官衰竭估计评分(SOFA)[6]该评分系统主要分为6个部分,分别是呼吸功能、凝血功能、肝脏功能、心血管系统、中枢神经系统和肾脏功能,单项评分为0~4分等,总分为0~24分,分数越高说明病情越重,预后越差。
1.2.2急性生理和慢性健康评分(APACHEⅡ评分)[7]该评分系统包括急性生理评分、年龄评分及慢性健康评分3个部分,总分为0~71分,分数越高说明病情越重,预后越差。
1.2.3ECMO治疗前后血乳酸水平检测 分别于ECMO治疗前6 h及ECMO治疗后24 h抽取患者动脉血4 mL,采用酶催化法对患者血液样本中的乳酸水平进行检测,检测仪器为德国EKF宜得孚便携式乳酸分析仪。
1.2.4临床资料统计 以顺利出院为观察终点,分析抢救成功患者与死亡患者的临床资料,对患者性别,年龄,体质量指数(BMI),ECMO治疗前心脏骤停时间(CA-ECMO),高血压、糖尿病及外周血管疾病等合并症,灌注插管型号(15Fr或17Fr),手术类型(体外循环或非体外循环),病变血管支数(<3支或≥3支),犯罪血管(右冠状动脉、左主干、左回旋支及左前降支),主动脉内球囊反搏(IABP)使用情况,吸烟史,ICU住院时间等资料进行记录和统计。
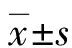
2 结 果
2.1生存组与死亡组临床资料比较 两组患者性别,BMI,高血压、糖尿病、外周血管疾病发生率,灌注插管型号,手术类型,犯罪血管,ECMO前6 h血乳酸水平,IABP使用情况及吸烟史比较,差异无统计学意义(P>0.05);两组患者年龄、APACHE Ⅱ评分、SOFA评分、CA-ECMO、病变血管支数、ECMO后24 h血乳酸水平、ICU住院时间比较,差异均有统计学意义(P<0.05)。见表1。
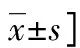
表1 生存组与死亡组临床资料比较[n(%)或M(P25,P75)或
2.2CABG术后接受股动脉ECMO治疗患者预后不良的多因素Logistic回归分析 将CABG术后接受股动脉ECMO治疗患者的预后情况作为因变量(死亡=1,生存=0),将表1中差异有统计学意义的指标[年龄(≥60岁=1,<60岁=0),APACHE Ⅱ评分(≥30分=1,<30分=0),SOFA评分(≥10分=1,<10分=0),CA-ECMO(≥33 h=1,<33 h=0),病变血管支数(≥3支=1,<3支=0),ECMO后24 h血乳酸水平(≥10.00 mmol/L=1,<10.00 mmol/L=0),ICU住院时间(≥14 d=1,<14 d=0)]作为自变量进行多因素Logistic回归分析。多因素Logistic回归分析结果显示,年龄≥60岁、APACHE Ⅱ评分≥30分、SOFA评分≥10分、CA-ECMO≥33 h、病变血管支数≥3支、ECMO后24 h血乳酸水平≥10.00 mmol/L、ICU住院时间≥14 d为CABG术后接受股动脉ECMO治疗患者预后不良的危险因素(P<0.05)。见表2。
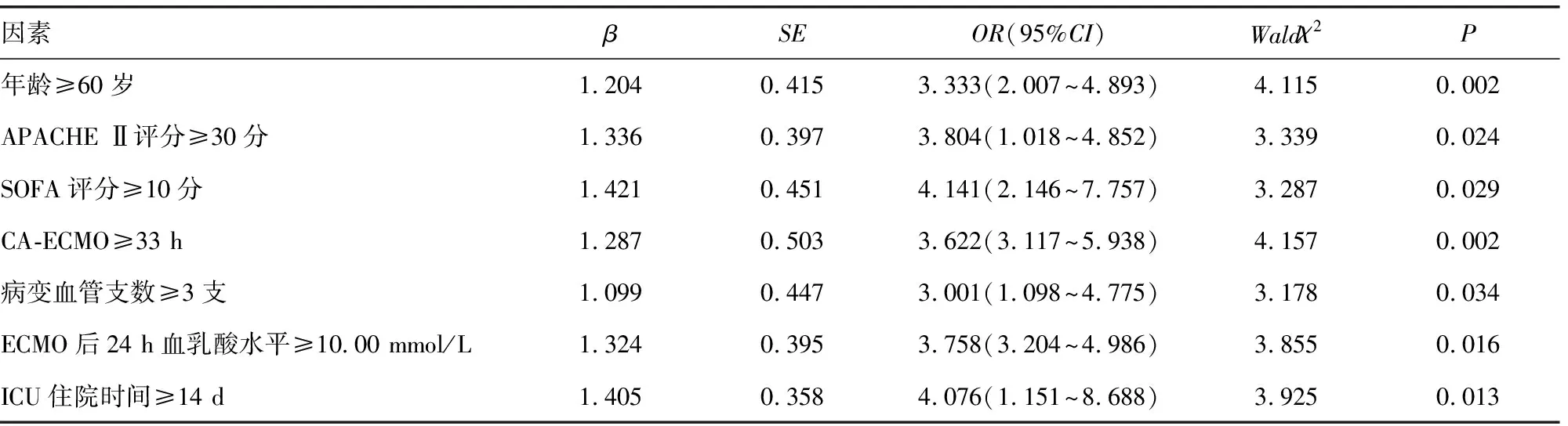
表2 CABG术后接受股动脉ECMO治疗患者预后不良的多因素Logistic回归分析
3 讨 论
ECMO的核心由膜肺(人工肺)和血泵(人工心脏)组成,其运行原理是利用人工血泵替代心脏功能,维持机体血流动力学稳定,减轻心脏负担,使得衰竭的心脏得到足够的休息时间,以利于其恢复。此外,ECMO还能有效减轻肺动脉与右心室压力,通过对体外循环中的血液进行氧合,从而有效改善机体组织器官缺氧、缺血状态[8-9]。相较于传统的心肺复苏中大剂量血管活性药物的使用,ECMO明显降低了患者心律失常、心肌耗氧增加等风险[10]。因此,对于CABG术后出现心脏骤停或多器官衰竭患者,应用ECMO进行辅助治疗,可实现呼吸和循环的双重支持作用,从而为抢救患者赢得宝贵时间,提高患者存活率。
ECMO能够提高心脏手术后心脏骤停患者的抢救成功率。本研究对200例CABG术后接受股动脉ECMO辅助治疗患者的生存结局进行了统计,结果显示,200例患者中,住院期间死亡88例,抢救成功112例,同GRANDIN等[11]相关报道结果一致。邵程程等[12]和ZHA等[13]报道器官衰竭状态、重急性或慢性疾病等都是影响心脏大手术患者术后ECMO治疗结局的危险因素,对于治疗前APACHE Ⅱ、SOFA评分越高的ECMO患者,预后抢救成功的概率越低。另外,年龄也是ECMO患者预后不良的重要因素,年龄通常与各种并发症、慢性疾病等有关,年龄越大,身体功能越差,发生各种并发症、慢性病风险越高,从而对ECMO治疗患者的预后造成不良影响[14]。有研究表明,ECMO应用时机也与ECMO治疗结局有关,临床中,对于符合ECMO 指征,且无禁忌证的危重症患者,ECMO 上机时机越早,患者预后不良事件的发生率越低[15]。另有研究表明,血乳酸水平升高可引起血管性并发症,在远端组织灌注不足、循环不稳定等患者中,血乳酸水平越高,CABG术后接受股动脉ECMO治疗患者预后不良风险越高[16]。因此,应密切观察ECMO上机后患者的血乳酸水平,改善不良预后。蒋玉兰等[17]报道指出,冠状动脉血管病变支数越多,术后不良风险越高。ICU住院时间通常代表患者病情的严重程度,有报道指出,心脏手术患者ICU住院时间越长,患者预后不良概率越高[18-20]。本研究中,年龄≥60岁、APACHE Ⅱ评分≥30分、SOFA评分≥10分、CA-ECMO≥33 h、病变血管支数≥3支、ECMO后24 h血乳酸水平≥10.00 mmol/L、ICU住院时间≥14 d为CABG术后接受股动脉ECMO治疗患者预后不良的危险因素(P<0.05),同上述相关报道结果基本一致。
综上所述,年龄≥60岁、APACHE Ⅱ评分≥30分、SOFA评分≥10分、CA-ECMO≥33 h、病变血管支数≥3支、ECMO后24 h血乳酸水平≥10.00 mmol/L、ICU住院时间≥14 d为CABG术后接受股动脉ECMO治疗患者预后不良的危险因素。在临床治疗中,需对上述因素加以重视和筛查,并采取积极的针对性措施,降低患者不良预后风险。本研究的局限性在于单中心回顾性研究,样本量相对较少,且患者随访时间也相对较短,未能明确对CABG术后远期预后的影响。因此,还需在今后的研究中对研究样本及研究时间做进一步完善,提高参考价值。



