喻燕波,王志剑,赵 勇,邱觅真,俞志强
(南昌大学第一附属医院疼痛科,江西 南昌 330006)
青少年腰椎间盘突出症(adolescent lumbar disc herniation,ALDH)目前定义为21岁及以下的腰椎间盘突出症患者[1],其发病率呈逐年上升趋势。据报道[2,3],ALDH 占同期住院腰椎间盘突出症患者的0.6%~6.8%,而患有下腰痛的青少年有3%为腰椎间盘突出症。传统的牵引、按摩及中草药等保守治疗效果不佳[4,5]。近年来,腰椎间盘微创治疗技术在临床迅速发展,并取得显着治疗效果。本研究主要比较射频热凝术联合胶原酶化学溶解术与传统椎板减压术治疗ALDH 的效果,现报道如下。
1 资料与方法
1.1 一般资料 选取2019年6 月-2020年6 月南昌大学第一附属医院收治的ALDH 患者65例作为研究对象,纳入标准:单侧或双侧下肢痛、体格检查阳性体征明确,与CT、MRI 影像表现相一致,且均为单间隙椎间盘突出,经保守治疗无效者。排除标准:合并其它脏器疾病、突出物钙化、凝血功能障碍、椎体滑脱或椎管先天性骨性狭窄者。根据治疗方式不同分为A组33例和B组32例。A组男25例,女8例;年龄14~21岁,平均年龄(19.21±2.40)岁。B组男26例,女6例;年龄15~21岁,平均年龄(20.45±1.86)岁。两组性别、年龄比较,差异无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会审批通过,患者家属知情同意并签署知情同意书。
1.2 方法
1.2.1 A组 予以射频热凝术联合胶原酶化学溶解术治疗:患者取俯卧位于DSA 手术室C 臂床上,海绵软垫置于腹部,减小腰椎生理曲度,以患者舒适为度。根据术中定位片,结合患者CT、MRI 影像资料与突出物形态来设计适宜的穿刺路径,包括小关节内缘入路、椎间孔安全三角区入路。选取5 mm 裸端穿刺套管针,常规消毒铺巾,使用利多卡因行皮肤穿刺点及部分肌层麻醉,在影像引导下进行穿刺,侧位片提示穿刺针位置至椎间盘后1/3(即近椎间盘髓核部),并行造影证实盘内及突出物均显影[2]。根据造影剂弥散情况,先行注射胶原酶120 U/0.3 ml,置入射频电极后测定电阻抗值,再行感觉诱发(50 Hz、0.5~1.0 mA)及运动诱发(2 Hz、1.0~2.0 mA)检测,不诱发出疼痛与下肢肌肉收缩则表明电极与神经根保持安全距离。另外,设定初始工作参数为70 ℃、30 s进行连续射频热凝,并渐次提高到80 ℃、90 s,90 ℃、90 s,无电击样麻木或疼痛后遂将工作参数设置为95 ℃、90 s,工作2个周期完成髓核内部分胶原酶灭活及髓核热凝成型术。在手术过程中,与患者沟通交流,观察下肢运动、感觉功能。射频热凝术结束后拔除电极,再行突出物外层面胶原酶化学溶解术(胶原酶600 U/2.0 ml)。
1.2.2 B组 予以常规椎板后路开窗减压术治疗:连续硬膜外神经阻滞麻醉后,患者取俯卧位,胸部、双侧季肋部及双侧髂部垫枕,腹部悬空。取病变节段处腰部后正中切口,切开皮肤、皮下组织,单侧连续和间断开窗剥离患侧骶棘肌,交叉开窗剥离双侧骶棘肌,显露椎板间隙,不切断棘上韧带、不咬除棘突,用椎板咬骨钳咬去上位椎板下缘,切除部分黄韧带,神经剥离器轻轻深入分离椎板与硬膜之间粘连,扩大骨窗,部分咬除上下椎板,显露神经根。见椎间盘突出行髓核摘除,扩大神经根通道。温生理盐水冲洗椎管,覆盖游离薄层脂肪片。术毕,创口内放硅胶引流管常规留置负压引流24 h。术后第7 天,在腰围保护下起床,3个月内禁止体力劳动。
1.3 观察指标 比较两组疼痛程度、腰椎功能恢复情况及围手术期指标(手术时间、术中失血量、术后下床时间、住院时间、住院费用)。采用视觉模拟评分法(VAS)评估患者疼痛程度,评分范围0~10 分,其中0 分为无痛,10 分为最剧烈疼痛。采用日本骨科协会评估治疗分数(JOA)评估患者腰椎功能恢复情况,评分范围0~29 分,患者腰椎功能的恢复程度与评分呈正相关。
1.4 统计学方法 采用SPSS 24.0 统计软件包进行数据分析,计量资料以()表示,采用t检验;计数资料以[n(%)]表示,采用χ2检验。以P<0.05 表示差异有统计学意义。
2 结果
2.1 两组VAS 评分比较 两组术后1周、3个月VAS评分低于术前,且A组术后3个月VAS 评分低于B组,差异有统计学意义(P<0.05),见表1。
表1 两组VAS 评分比较(,分)
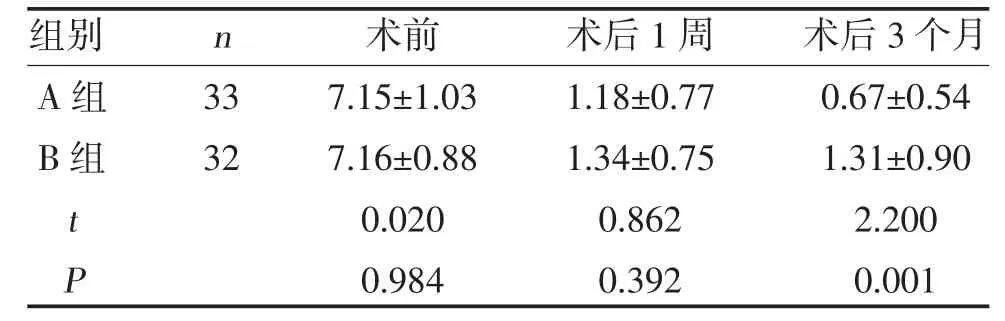
表1 两组VAS 评分比较(,分)
2.2 两组JOA 评分比较 两组术后1周、3个月JOA评分高于术前,且A组术后3个月JOA 评分高于B组,差异有统计学意义(P<0.05),见表2。
表2 两组JOA 评分比较(,分)
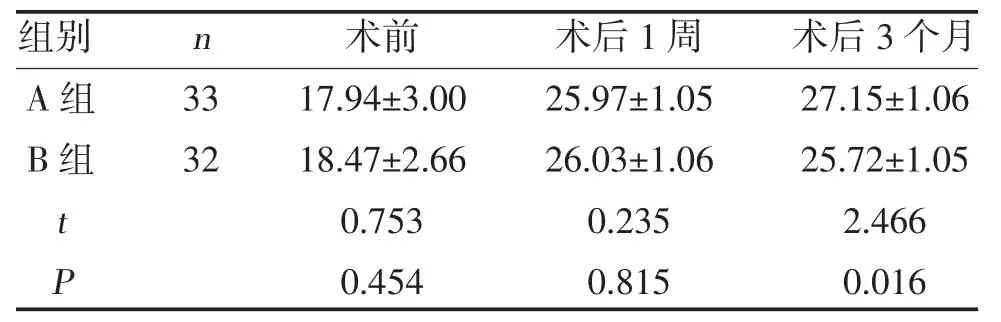
表2 两组JOA 评分比较(,分)
2.3 两组围手术期指标比较 A组手术时间、术中失血量、住院时间及住院费用优于B组,差异有统计学意义(P<0.05);两组术后下床时间比较,差异无统计学意义(P>0.05),见表3。
表3 两组围手术期指标比较()
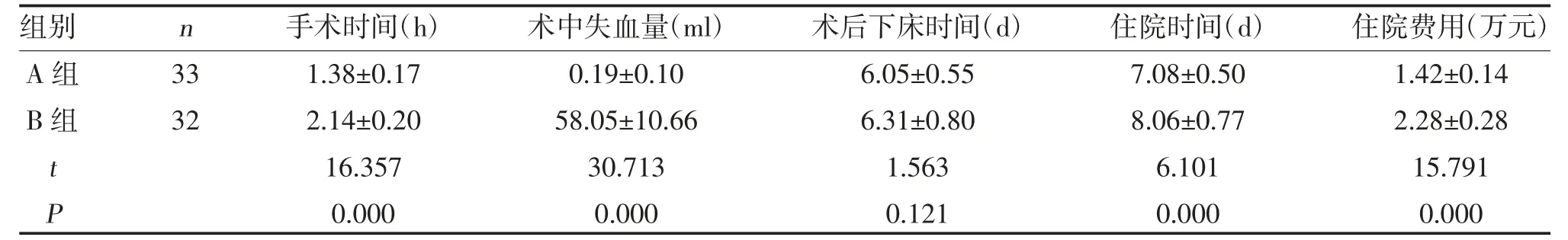
表3 两组围手术期指标比较()
3 讨论
ALDH 致病原因较多,目前尚不明确,一般认为与创伤、遗传、发育异常及体重等相关[6]。青少年时期椎间盘与成年后生理特性有明显区别,其髓核为水化良好的胶冻状,纤维环有优良的弹性,且基质中富含蛋白多糖、胶原和水份,具有抗压、缓和冲击的作用[7]。青少年造成椎间盘突出主要原因是软骨终板破裂、髓核突出或脱出,其中软骨板损伤后,可能导致椎间盘的营养通路受阻,营养供给减少,代谢终产物集积聚,乳酸浓度升高,使椎间盘内的金属蛋白酶等激活,导致基质破坏,细胞代谢异常甚至凋亡;髓核内的蛋白多糖类物质渗出,对神经根及周围组织产生刺激,引起无菌性炎症或自身免疫应激反应,如再受到外力挤压,纤维环和髓核组织突入椎管,或游离出来,造成椎管狭窄,压迫神经根,引发临床常见的腰腿痛[8]。
由于青少年脊柱生长发育阶段,其椎间盘尚未发育成熟,有学者认为ALDH 应先行保守治疗,经充分保守治疗4~6周症状无好转,方可考虑手术[9,10]。常用的保守治疗包括卧床、牵引、药物及椎管内神经阻滞治疗等,可一定程度缓解腰腿痛,但其确切疗效还有待进一步研究。有研究认为[11,12],ALDH 患者保守治疗效果不及成年人。戴锋等[13]对71例LDH 合并纤维环破裂者进行5年随访,结果显示保守治疗后JOA 评分优良率可达73.2%,其中24例髓核明显吸收,推测可能与激活内源性胶原酶有关。胶原酶化学溶解术的应用可以追溯到1969年,Sussman BJ等[14,15]使用胶原酶对椎间盘组织进行体外溶解试验及动物实验,证实了胶原酶是具有专一水解胶原蛋白的特异性溶解酶,提出可用特异性胶原酶来治疗腰椎间盘突出症。胶原酶化学溶解术的主要机制是当外源性胶原酶以酶原的形式接触到髓核组织,包括椎间盘内或突出物中的被激活而水解胶原分子,使之易解链变性,降解为脯氨酸等氨基酸及水,被人体吸收[16,17]。本研究结果显示,A组术后3个月VAS评分低于B组,JOA 评分高于B组,差异有统计学意义(P<0.05);A组术中失血量、手术时间、住院时间及住院费用优于B组,差异有统计学意义(P<0.05),而两组术后下床时间比较,差异无统计学意义(P>0.05),考虑原因为胶原酶这种特殊蛋白酶具有高度特异性,主要是水解突出的髓核组织中胶原蛋白,使突出物缩小,甚至消失,达到减轻或消除突出物对神经根的压迫,同时其具有抑制炎性介质的作用,能够缓解神经根炎症,减轻水肿,改善临床症状。此外,联合射频热凝技术,利用电极周围产生的热能可使髓核固缩,修复纤维环或损毁纤维环的内增生移行的神经末稍,达到降低椎间盘内压并抑制疼痛的目的[18-20],二者结合起来可使腰椎间盘突出症的机械压迫问题及椎间盘热凝成型同时得到解决。
综上所述,腰椎间盘胶原酶溶解联合射频热凝术治疗ALDH 效果确切,具有术后恢复快、手术及住院时间短、术中出血量少、住院费用低等优点。但本研究纳入病例数量及随访时间有限,有待在临床实践中进一步研究。



