杨会杰 杜洁 赵倩 朱超霞
(郑州市第七人民医院 郑州 450000)
我国帕金森病患者超过300 万,约占全球发病的30%(全球近1 000 万例)[1]。帕金森病是一种常见的中枢神经系统退行性疾病,临床主要病理特征表现为中脑黑质致密部多巴胺能神经元变性缺失,同时伴有5-羟色胺(5-HT)能神经元减少[2]。帕金森病的发病原因尚未完全明确,但多巴胺能系统和非多巴胺能系统受损无疑在其中发挥着重要的作用。研究表明,帕金森病患者中脑黑质多巴胺能神经元变性坏死超过50%,纹状体多巴胺含量减少超过80%[3]。多巴胺合成减少可刺激乙酰胆碱功能亢进,也就是说,多巴胺与乙酰胆碱之间失衡是诱导帕金森病发生的重要原因[4]。因此,增强多巴胺效应、维持多巴胺与乙酰胆碱的平衡,是治疗帕金森病的关键。多巴丝肼片为治疗帕金森病的首选用药,其可竞争性抑制多巴脱羧酶活性,维护乙酰胆碱与多巴胺间平衡[5]。吡贝地尔缓释片属于一种非麦角类多巴胺受体激动剂,具有半衰期长、血药浓度稳定的特点,能提高多巴胺受体兴奋性,修复受损神经元细胞[6]。吡贝地尔联合多巴丝肼片治疗能迅速改善帕金森病患者临床症状,但是否通过调节脑神经递质发挥治疗作用目前尚缺乏足够的证据。本研究主要分析吡贝地尔联合多巴丝肼片治疗帕金森病临床疗效及对脑神经递质的影响。
1 资料与方法
1.1 资料
选择2018 年4 月—2020 年10 月收治的早期帕金森病患者86 例为研究对象,男54 例,女32 例,年龄52 ~68 岁,病程1 ~7 年,H-Y 分级Ⅰ~Ⅲ级[7]。采用随机数字表法分为试验组44 例、对照组42 例,两组患者性别等基础数据比较差异无统计学意义(P>0.05,表1)。
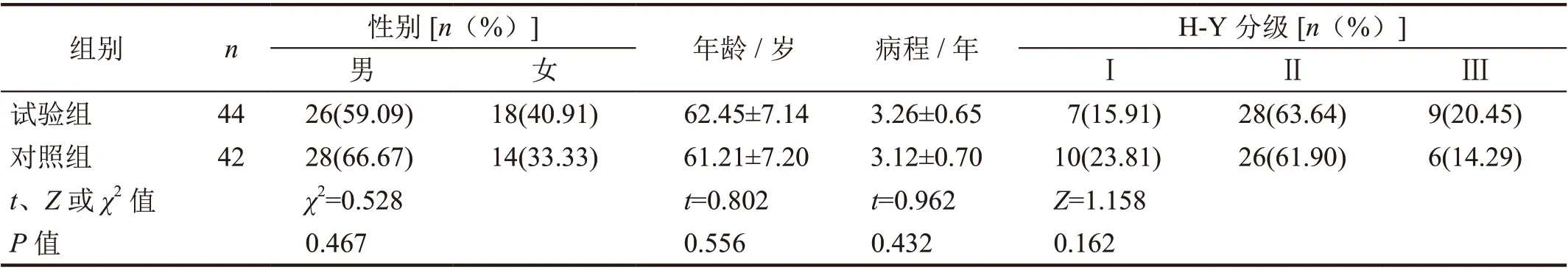
表1 患者一般资料比较
1.2 纳入与排除标准
纳入标准:①均符合中华医学会神经病学分会《中国帕金森病治疗指南(2016 版)》诊断标准[8];②H-Y分级Ⅰ~Ⅲ级[4];③意识清晰,有正常交流能力;④入组前未接受抗帕金森病药物治疗;⑤经医院伦理委员会批准,患者或家属知情同意。
排除标准:①合并严重心、肺、肝、肾等脏器功能障碍者;②伴有认知功能障碍及精神异常者;③对本次研究药物过敏者;④中途退出者。
1.3 治疗方法
对照组给予多巴丝肼片(上海罗氏制药,国药准字H10930198,规格0.25 g/片)治疗,初始剂量62.5 mg/次,2 次/d,逐渐调整至有效剂量125 mg/次,2 次/d。试验组给予吡贝地尔缓释片[施维雅(天津)制药,国药准字J20140064,规格50 mg/片]联合多巴丝肼片治疗,多巴丝肼片用法用量同对照组,吡贝地尔缓释片初始剂量25 mg/次,2 次/d,逐渐调整至有效剂量为50 mg/次,3 次/d。两组均连续治疗6 个月。
1.4 观察指标
1)临床疗效 采用改良Webster 症状评分量表评估[9],包括面部表情、上肢姿式、步态、语言、起坐障碍等10 个症状,每个症状采用0 ~3 分4 级评分法,分值越高,症状越严重。量表Cronbach’s α=0.915。以Webster 评分减少率为疗效判断标准,分为显效(Webster评分减少率>50%)、有效(Webster 评分减少率20%~50%)、无效(Webster 评分减少率<20%)。减少率=(治疗前评分-治疗后评分)/治疗前评分×100%;有效率=(显效+有效)/总例数×100%。
2)运动相关功能 治疗前后,采用帕金森综合评估量表(UPDRS)测评[10],包括精神行为和情绪(4 条目)、运动功能(14 条目)、日常活动(13 条目)等3 维度共31 个条目,每个条目采用0 ~4 分评分,分值越高,相关功能越差。量表Cronbach’s α=0.875。
3)神经递质 治疗前后,采用ML2001 型脑电超慢涨落分析仪(北京同仁光电技术公司)检测,包括S1谱系γ-氨基丁酸(GABA)、S4 谱系5-HT、S11 谱系多巴胺(DA)等。4)不良反应 统计两组恶心呕吐、失眠、便秘、体位性低血压等并发症发生率。
1.5 统计学方法
2 结果
2.1 临床疗效
试验组治疗有效率高于对照组(93.18%vs76.19%,P<0.05,表2)。
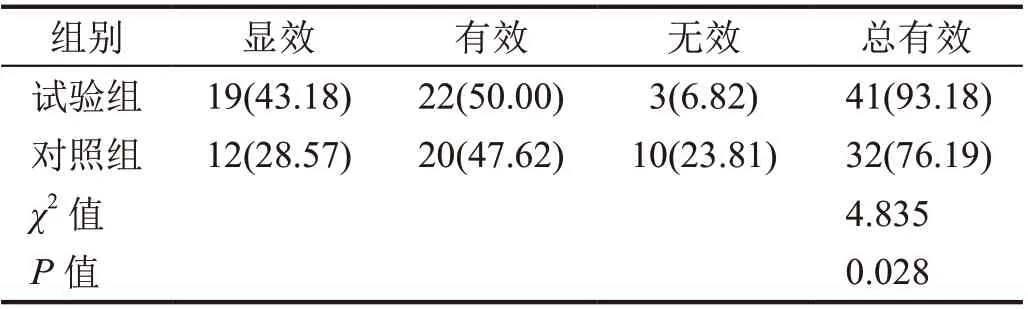
表2 临床疗效比较[n(%)]
2.2 运动相关功能
与同组治疗前比较,两组帕金森病患者精神行为和情绪等评分均降低(P<0.05);治疗6 个月,试验组帕金森病患者精神行为和情绪、运动功能、日常活动、UPDRS 总分低于对照组(P<0.05,表3)。
表3 治疗前后UPDRS评分比较(±s)
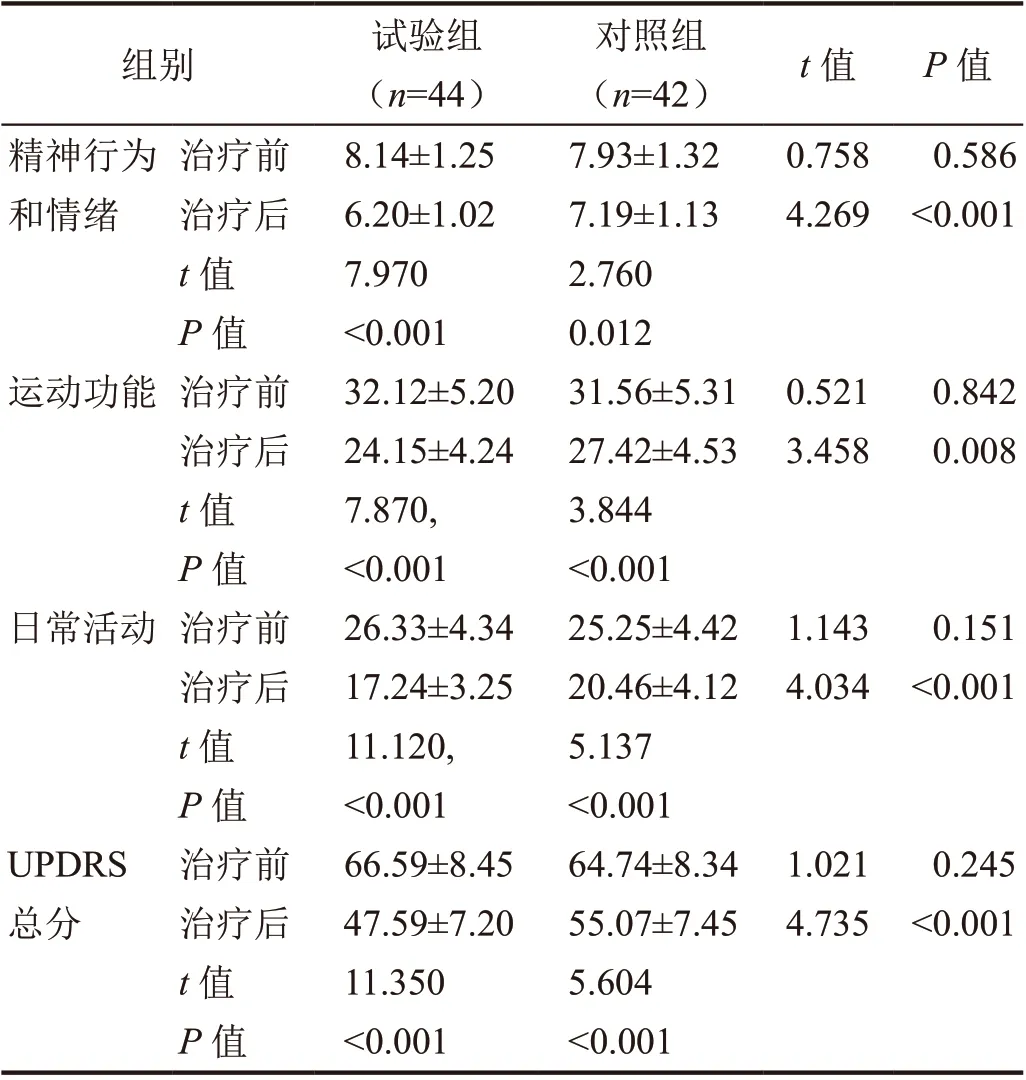
表3 治疗前后UPDRS评分比较(±s)
组别试验组(n=44)对照组(n=42)t 值P 值治疗前 8.14±1.257.93±1.320.7580.586治疗后 6.20±1.027.19±1.134.269 <0.001 t 值7.9702.760 P 值<0.0010.012运动功能治疗前 32.12±5.20 31.56±5.31 0.5210.842治疗后 24.15±4.24 27.42±4.53 3.4580.008 t 值7.870,3.844 P 值<0.001<0.001日常活动治疗前 26.33±4.34 25.25±4.42 1.1430.151治疗后 17.24±3.25 20.46±4.12 4.034 <0.001 t 值11.120,5.137 P 值<0.001<0.001 UPDRS总分精神行为和情绪治疗前 66.59±8.45 64.74±8.34 1.0210.245治疗后 47.59±7.20 55.07±7.45 4.735 <0.001 t 值11.3505.604 P 值<0.001<0.001
2.3 脑神经递质
与同组治疗前比较,两组患者脑GABA 降低,5-HT、DA 升高(P<0.05);治疗6 个月,试验组脑GABA 低于对照组,但5-HT、DA 高于对照组(P<0.05,表4)。
表4 治疗前后脑神经递质比较(±s, ng·mL-1)

表4 治疗前后脑神经递质比较(±s, ng·mL-1)
组别GABA5-HTDA治疗前治疗后t 值P 值治疗前治疗后t 值P 值治疗前治疗后t 值P 值试验组 7.54±1.12 5.74±0.72 8.967 <0.001 16.15±3.20 22.54±4.12 8.125 <0.001 38.21±7.00 73.52±11.21 16.574 <0.001对照组 7.38±1.05 6.62±0.81 3.714 0.003 16.54±3.34 19.43±4.21 3.4850.007 40.13±8.21 54.31±8.62 7.445 <0.001 t 值0.6835.3310.5533.4621.1577.822 P 值0.656<0.0010.7840.0070.146<0.001
2.4 不良反应
两组恶心呕吐等不良反应比较差异无统计学意义(P>0.05,表5)。
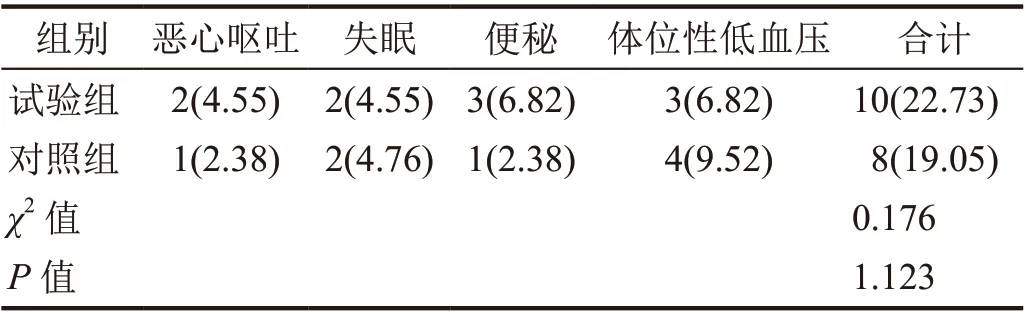
表5 不良反应比较[n(%)]
3 讨论
多巴丝肼片由苄丝肼与左旋多巴复合而成,苄丝肼属于一种脱羧酶抑制剂,能够抑制机体外周多巴脱羧酶,诱导多巴进入脑部转化为多巴胺;左旋多巴是目前治疗帕金森病最有效的一种药物,能够调节多巴胺与乙酰胆碱的平衡。但长期应用左旋多巴易诱发“开关现象”,即药物疗效难以预料[11-12]。吡贝地尔是一种缓释型多巴胺受体激动剂,可通过刺激中脑-边缘叶通路(D2、D3受体)、大脑黑质纹状体D2受体,增强多巴胺效应,诱导多巴胺与多巴胺受体结合。因其作用缓慢,半衰期长,血药浓度稳定,能避免纹状体突触后膜多巴胺受体的脉冲样刺激。同时吡贝地尔属于非麦角碱药物,主要作用部位在新边缘叶、脑部黑质细胞,且作用机制与多巴胺脱羧酶无关,能减轻四肢震颤与“开关现象”的发生[13]。也有文献报道,吡贝地尔能够增强多巴丝肼片中左旋多巴的功能,发挥协同作用[14]。本研究中,试验组患者精神行为和情绪、运动功能、日常活动、UPDRS 总分低于对照组,有效率高于对照组,与刘红[15]报道基本相似,说明吡贝地尔联合多巴丝肼片能改善帕金森病患者运动相关功能,提高临床疗效。
本研究结果表明,吡贝地尔缓释片联合多巴丝肼片应用于早期帕金森病患者治疗中,能够改善患者精神行为和情绪、运动功能、日常活动状态,提高临床疗效,且不增加不良反应,可能与调节患者脑内GABA、DA、5-HT 等神经递质有关。需要指出的是,本研究仅仅分析了吡贝地尔联合多巴丝肼片对脑神经递质影响的现象,吡贝地尔联合多巴丝肼片通过何种路径影响脑神经递质,仍需要更多的基础研究和临床研究去求证。



