史子柯 马霄云 张雁山 金雪玲 寇海瑞 吴嘉明
(甘肃省武威肿瘤医院重离子中心放射物理室,甘肃 武威 733000)
肝癌是我国常见的恶性肿瘤之一,其发病率和死亡率分别位居我国恶性肿瘤的第4位和第2位。全世界每年新发病例约26万人,其中我国占42%~45%[1-2]。放射治疗技术被越来越多地用于肝癌的治疗[3]。容积旋转调强放射治疗(VAMT)利用动态多叶光栅(MLC)、可变剂量率和可变的机架转速[4-5],通过优化的弧形照射来实现旋转治疗,理论上可以获得更优的靶区剂量分布,减少正常组织的受量[6-7]。无均整过滤器(FFF)模式移除了均整器,机头散射因子和准直器散射因子降低,离轴比剂量分布变小,照射野周围的剂量更低,提高了剂量率,其射野的剂量分布与有均整过滤器(FF)模式下有较大差别[8-10]。本研究针对肝癌患者分别制定FFF和FF下两种VMAT计划,比较分析两种计划的靶区以及危及器官(OAR)的剂量学差异,探究FFF-VMAT计划用于肝癌临床放疗的优势。
1 对象和方法
1.1 对象
选择2020年8月—2021年4月在甘肃省武威肿瘤医院重离子中心确诊为肝癌并放疗的患者10例(靶区体积35~200 cm3),年龄52~81岁。
1.2 设备
Vital beam直线加速器(美国瓦里安公司)、definition AS 64排大孔径CT定位机(德国西门子)、真空负压袋加热塑膜固定装置。
1.3 方法
1.3.1靶区勾画及处方剂量 患者行CT增强扫描,范围为第5胸椎至第4腰椎,层厚3 mm,扫描所得CT图像以DICOM格式传输至治疗计划系统进行三维重建。由我中心放疗医生勾画出计划靶区(PTV)和OAR。靶区处方剂量50 Gy/25次[1,5],OAR的限量设定分别为:胃Dmax≤4 500 cGy,双肾Dmean≤1 500 cGy,十二指肠Dmax≤5 000 cGy,脊髓Dmax≤4 500 cGy,双肺Dmean≤1 500 cGy,以及肝脏Dmean≤2 500 cGy。
1.3.2两种治疗计划的设计 采用Eclipse 15.5治疗计划系统针对每例患者分别制定FFF模式和FF模式两种VMAT治疗计划。FFF模式计划需采用6MV-FFF能量射线,最大剂量率1 400 MU/min;FF模式计划采用6 MV能量射线,最大剂量率为600 MU/min[11]。两种治疗计划均采用VMAT技术,为使靶区有更好的剂量均匀性,并更好地保护正常肝组织,所有计划均采用3个小半弧设计(准直器角度5°~20°)[12-13]。同时为减少对比误差,两组治疗计划的照射角度和优化条件相同,归一方式均为95%的PTV满足处方剂量,处方剂量110%所包绕的体积不得超过靶区体积的1%。
1.3.3两种治疗计划的评估指标及其标准 对FFF模式和FF模式两种治疗计划的剂量分布云图进行对比分析,评估指标包括靶区适形度(CI)和剂量均匀性(HI)(CI的值越接近于1,说明靶区的适形度越好,HI的值越接近于0,说明靶区的剂量均匀性越好)[14-15],以及正常的肝组织受量和OAR受量、加速器总跳数和出束时间。其中CI=(PTV95/VPTV)×(PTV95/V95),PTV95为PTV被95%的处方剂量线所包绕的体积,VPTV为PTV的体积,V95为95%的处方剂量线所包绕的所有区域的总体积;HI=(D2%-D98%)/D50%。OAR受量评估指标包括Dmean、Dmax、V5、V10、V15、V20、V25、V30、V35、V40。记录两种放疗计划的加速器总跳数和出束时间。
1.4 统计学处理
2 结 果
2.1 两种治疗计划的剂量分布云图比较
FF-VMAT和FFF-VMAT计划均能满足临床处方要求,剂量分布云图(包含横断面、冠状面、矢状面)显示,FF-VMAT和FFF-VMAT计划处方剂量均能较好包围靶区,剂量分布类似,靶外无剂量热点,靶内无剂量冷点,且未见超出处方剂量110%的区域(图1)。
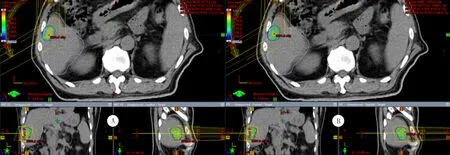
A:FF-VMAT计划,B:FFF-VMAT计划
2.2 两种治疗计划的靶区剂量分布比较
两种治疗计划靶区CI和HI比较,差异无统计学意义(P>0.05)。两种计划靶区剂量分布都能满足临床处方剂量的要求。见表1、2。
2.3 两种治疗计划的正常肝组织和OAR受量分布比较
两种治疗计划的正常肝组织和OAR受量各项参数比较,差异均无统计学意义(P>0.05)。见表3、4。两种模式下的正常肝组织和OAR受量情况均能满足限制要求。
2.4 两种治疗计划的加速器总跳数以及出束时间比较
FF-VMAT计划以及FFF-VMAT计划的加速器总跳数分别为(348.630±41.747)、(379.800±48.007)MU,出束时间分别为(0.592±0.066)、(0.271±0.034)min,FF-VMAT计划以及FFF-VMAT计划的加速器总跳数比较,差异无统计学意义(P>0.05),出束时间比较,差异具有统计学意义(t=13.611,P<0.05)。
3 讨 论
本研究采用的VAMT技术是一种较新的放疗技术,其最大的优势是显着提高了治疗效率[4]。近年来临床放疗中越来越广泛地采用VMAT技术联合FFF模式,因其具有适形高效的特点,可提高肿瘤治疗增益比。FFF与FF模式的演变反映了放疗医生和放射物理师对初始射线剂量均匀性与最终靶区内部理想剂量分布因果关系的认识变化。FF模式以降低光子通量为代价,也即降低射线的剂量率来满足射线质均整性。FFF模式移除了均整器,射线质软化,平均能量变低,光子注量增加,剂量率提高,射线均匀性变差,半影变小,使小野靶区更容易产生较高的表面剂量,大野靶区产生相当的或较低的表面剂量,但配合动态MLC调制,靶区也可以获得较好的CI和HI。
本研究结果显示,FF-VMAT和FFF-VMAT计划均能满足临床处方剂量要求,靶区CI和HI无明显差异。张基永等[16]对直肠癌放疗相关剂量学研究显示,FF模式较FFF模式能更优地实现靶区剂量分布和均匀性,而FFF模式更利于保护射野周边组织。REGGIORI等[17]对肝癌的研究表明,靶体积在100~300 cm3之间FFF模式的CI高于FF模式,靶体积小于100 cm3和大于300 cm3时FF模式CI更高。而吴思华等[18]的研究表明,靶区体积并没有对两种模式下靶区CI和HI产生出明显的影响。
本研究中FFF模式下的靶区外剂量跌落更快,大部分正常肝组织和OAR的受量更低。靶区外剂量分布受到肿瘤形状、大小、位置、剂量调制程度及射线能量高低和射线离轴比的影响[19],射野外的组织受到的射线离轴比变大,射线平均能量比FF模式更低,剂量跌落较快。相关的研究也表明,FFF模式可以很好地保护靶外正常组织和OAR[20-22]。
本研究中FFF模式下的正常肝组织在3 000、3 500 cGy处的受照体积比FF模式下略高,右肾受照的平均剂量也略高,可能是因为FFF模式下射线质的异质性大于FF模式,离轴较远处的平均能量比FF低,更易于被散射。而本研究的肝癌病灶位于右上腹,水等效深度大,这样容易使较多的散射剂量沉积在正常肝组织和邻近的右肾中,从而导致其受到略高的低剂量照射[22]。
本研究中FFF模式剂量率是常规FF模式的2.33倍,出束时间仅为FF模式的一半。FU等[23]研究显示,FFF和FF模式下治疗时间的差别和分割剂量有关。分割剂量越大,在FFF模式下治疗时间缩减越多。在脑部立体定向放射治疗(SBRT)、肺癌SBRT、前列腺癌立体定向消融放疗(SABR)等单次照射剂量较高的放疗中,其时间效率优势可得到充分发挥[18]。由于单次照射剂量大,FFF模式下的高剂量率可有效缩短出束时间,以此来减少器官运动带来的影响,提高患者舒适度。但周鹏等[24]认为,FFF模式下的高剂量率在提高治疗增益的同时也带来了治疗风险。因此,采用FFF模式治疗前可采用呼吸门控、图像引导及光学表面摆位等技术来确保靶区位置精确。
综上,对肝癌患者的放疗,采用FF-VMAT以及FFF-VMAT模式均能满足临床治疗需要,其靶区CI和HI无明显差异,但FFF-VMAT模式下的靶区外剂量跌落更快,正常肝组织和OAR的受量更低。另外,由于本研究采用的剂量分割为常规分割,FFF-VMAT模式的优势没有得到充分发挥。



