姚克林 陈仁彪 王亮 高绍 刘陈汉 赵添
肺动静脉瘘(pulmonarv arteriovenous fistula,PAVF)是一种罕见的先天性肺血管畸形,表现为肺动脉与肺静脉之间发生异常交通,由CHURTON在1897年首次发现,称之为多发性肺动脉瘤,其中60%~90%的PAVF为遗传性出血性毛细血管扩张症[1-2]。PAVF的临床诊断依靠劳累后呼吸困难、紫绀、血氧分压下降、杵状指和红细胞增多等典型症状体征以及实验室检查,主要还是依赖于影像学检查,其中CT肺动脉造影(CT pulmonary angiography,CTPA)和数字减影血管造影技术(digital subtraction angiography,DSA)的诊断价值较高[2-3]。既往PAVF的治疗以传统外科手术为主,但由于损伤大且并发症多,已经逐渐将被微创、可重复、近期疗效确切的介入栓塞治疗所取代。笔者回顾性分析4例采用Amplatzer血管封堵器(Amplatzet vascular plug,AVP)联合弹簧圈栓塞治疗多发性PAVF的疗效,现报道如下。
1 资料与方法
1.1 临床资料 回顾性分析2018年9月至2019年9月在浙江大学附属邵逸夫医院联合AVP与弹簧圈介入栓塞治疗多发性PAVF的患者4例。其中,1例分2次手术完成;男1例,女3例;年龄28~61岁,中位年龄为43岁;主要症状为胸闷、呼吸困难,4例均有紫绀、血氧分压下降表现,3例红细胞增多、血红蛋白增高,2例杵状指改变,1例年轻男性患者有近期脑梗死病史,1例女性患者有急性乳腺炎病史。
1.2 图像分析 所有患者术前均完善CTPA,使用64排CT扫描仪(GE LightSpeed VCT,or Siemens CT SOMATOM Definition)。初步评估主要供血血管大小、数目以及流入、流出道。所有获取的影像图像评估分析由两位介入科副主任医师完成。
1.3 治疗方法 术前均排除手术禁忌证,所有患者均签署知情同意书。依据术前CTPA选择性行肺动脉主干及相关肺叶、肺段造影,在Philips Allura xper FD20 DSA或者GE Innova 4100-IQ血管造影系统下操作,当发现异常支气管动脉或非支气管性体动脉参与供血时,尽量使用微导管超选栓塞(2.9-Fr,Microcatheter;Merit Maestro,USA;或2.7-Fr Progreat;Terumo,Japan)。术中给予吸氧、心电图及血氧饱和度监护。核对患者信息无误后给予2%利多卡因局麻,麻醉完成后采用改良Seldinger法,使用18 G穿刺针经右侧股静脉穿刺,置入6 F长导管鞘(70 cm),用5 F Pig导管行肺动脉造影,常规肺动脉造影设置高压注射器流速20 mL/s,流量30 mL,每秒6帧曝光,亚段肺动脉造影依据畸形血管位置情况而适当调整参数,了解两肺多发性PAVF位置、数目及病灶大小、供血动脉管径。根据病变所在的部位分别使用单弯导管、SIM导管进行左肺动脉或右肺动脉造影,发现病变后置微导管分别超选择于病变血管近端再次造影,观察病变血管的部位和所属供血动脉,之后行局部放大造影或旋转一定角度造影,详细判断瘘口的大小、数量、供血动脉的管径。
1.4 评估指标 (1)临床成功:定义为紫绀、血氧饱和度的改善。(2)技术成功:定义为对所有探测到的异常肺血管畸形,并进行插管和随后的栓塞。(3)临床失败:介入后复发或临床症状继续存在。(4)技术失败:造影发现异常血管未能成功超选并栓塞。对于血管畸形数目较多,或累及双肺时,为了降低对肺功能影响,则可以考虑行分次介入手术。(5)并发症评估:术后并发症通过病历系统获取,延迟并发症通过门急诊随访,包括有无缺血所致的肺梗死等并发症。
2 结果
2.1 造影及栓塞表现 4例患者,肺动脉DSA造影共发现21个PAVF病灶,其中位于左侧9个,右侧12个。所有患者通过选择性肺动脉DSA造影观察病变的部位、数目、供血动脉和引流静脉。超选择至责任血管;栓塞后造影确认PAVF病灶不再显示,并确认放置的AVP定位精准,展开良好,无脱落移位;放置的弹簧圈无脱落、游走,无异位栓塞发生。其中1例患者术后造影两肺尖部仍可见2个微小PAVF灶,但供血血管小于2 mm,未予处理,图1A。
2.2 治疗效果 临床成功率、技术成功率均100%,4例多发性肺动静脉瘘均获得成功栓塞(图1-4),其中1例分两次介入手术完成,对供血动脉最大径≥5 mm的选用AVP栓塞,对供血动脉最大径<5 mm的采用弹簧圈栓塞,总计放置AVP 8个,弹簧圈25枚。4例患者手术未见严重并发症,紫绀和低氧血症的临床症状均明显改善,见表1。术后复查无再发。
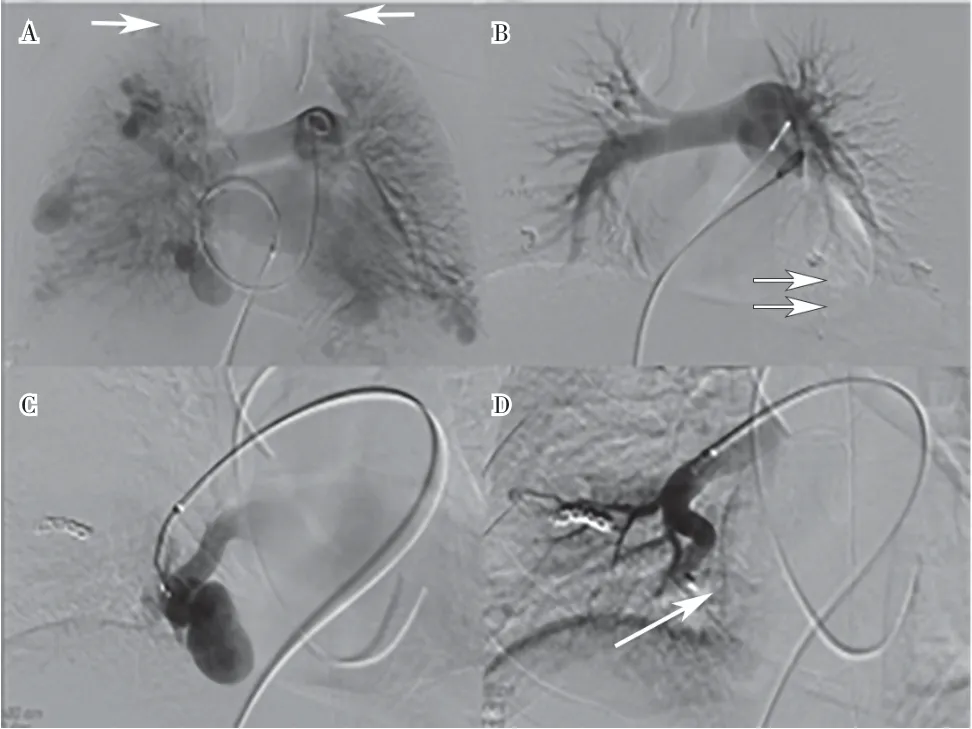
图1 A-B. 两肺多发PAVF栓塞前后造影;B.左肺下叶AVM病灶供血动脉(箭头标记处)串联放置多个AVP栓塞;C-D.右肺下叶PAVF病灶供血动脉(箭头标记处)放置AVP栓塞,两肺尖仍见小PAVF病灶(箭头标记处)
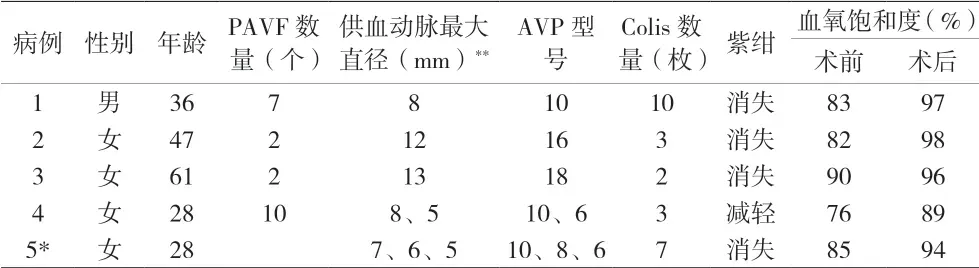
表1 Amplatzer vascular plug 联合弹簧圈栓塞多发性肺动静脉瘘的治疗结果
2.3 并发症情况 4例患者PAVF栓塞治疗后均无明显并发症发生。放置的AVP定位精准,展开形态良好,无脱落移位,无卡压邻近血管引起异常症状。放置的弹簧圈无脱落、游走,无异位栓塞发生。
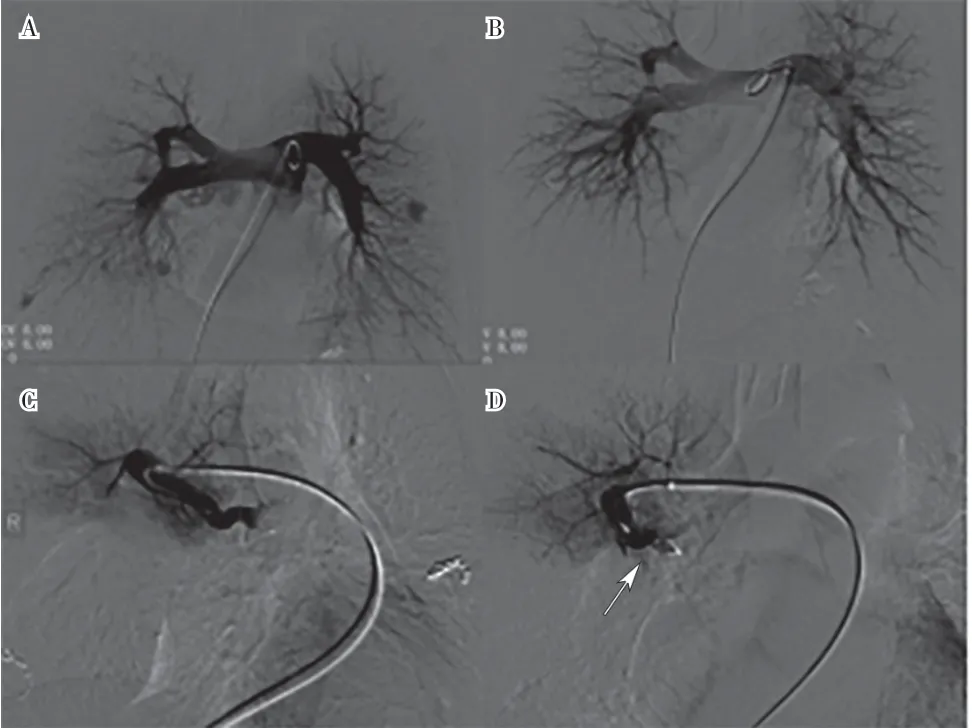
图2 A-B.两肺多发PAVF栓塞前后造影;C. 先放置一枚弹簧圈填塞;D. (箭头标记处)放置AVP,栓塞后远端血管未显示
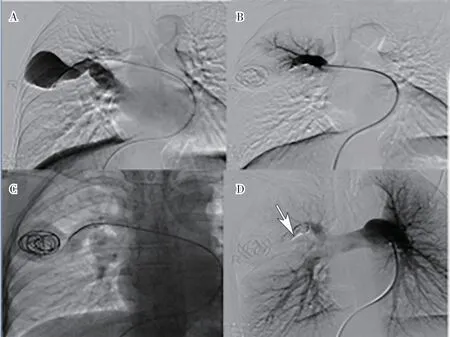
图3 A-B. 右肺较大PAVF病灶栓塞前后造影;C-D. 先行瘤体内填充弹簧圈,然后供血动脉主干AVP完全栓塞(箭头标记处)
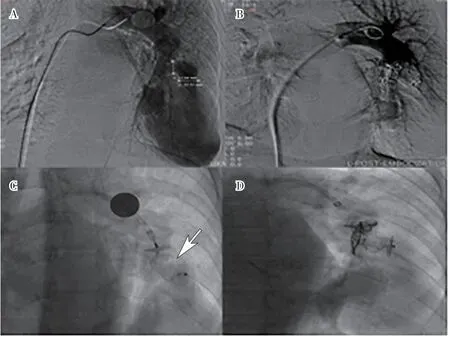
图4 A-B. 左肺较大PAVF病灶栓塞前后造影;C-D. 先行供血动脉主干AVP完全栓塞(箭头标记处),然后补充弹簧圈填塞
3 讨论
PAVF是指肺动脉与肺静脉异常交通引起的血流短路,分为先天性和获得性两种。获得性PAVF可由炎症和外伤引起,先天性肺动静脉短路可能由肺毛细血管壁发育障碍异常扩张或缺如所致。该病的临床症状取决于血流右往左分流量的大小,分流量小一般无症状,分流量大则可出现紫绀、杵状指、呼吸困难、心悸等症状。也有文献报道由于PAVF血液粘稠度高而导致脑梗死和脑脓肿的案例[3-4]。本组有1例年轻男性患者发生新近脑梗死,推测可能与PAVF相关。
PAVF的治疗传统上可采用手术切除肺叶或肺段,但手术创伤大、恢复慢,一定程度上降低了患者的呼吸储备功能,如遇双侧多发且伴有肺动脉高压的PAVF则手术受到严重限制。随着介入治疗技术的发展,栓塞治疗已成为PAVF的首选治疗方法,并且可以多次分期治疗,疗效可靠,创伤小,风险低,手术成功率高达80%~100%[5]。目前,常用的栓塞材料有金属弹簧圈、可脱式球囊、Amplatzer血管封堵器、国产双伞型封堵器等。1977年,PORSTMANN[6]首次报道使用弹簧圈进行肺动静脉瘘的栓塞治疗。弹簧圈作为肺动静脉瘘的常用栓塞材料,具有栓塞技术成熟、价格便宜等优点,对于供血动脉直径介于3~5 mm者尤为合适,术后完全栓塞率可达93%[7]。但若供血动脉直径大于5 mm,往往需多枚弹簧圈才能封堵彻底,而且弹簧圈移位、脱落、异位栓塞等并发症与残余分流的发生可能性会明显增加。Amplatzer血管封堵器最初设计是用于先天性心脏病的封堵治疗,鉴于其自膨胀及可回收的性能,术中还可相应调整封堵器的位置并可更换封堵器,具有定位可靠、栓塞技术简单等优点,现已应用于供血动脉粗大的PAVF封堵治疗[8]。但AVP的缺点是裸的镍钛金属丝网篮装置释放后不能立即形成血栓,通常需要8~35 min才能达到彻底封堵,在此过程中可能有一些小的纤维素栓子脱落造成体循环栓塞的并发症,尤其是对肺或脑循环系统[2]。国内报道不同的栓塞材料治疗PAVF均有满意疗效[6-9],也有文献报道对复杂型病例采用封堵器联合弹簧圈行栓塞治疗取得了较好效果[10]。
笔者使用AVP联合弹簧圈血管内栓塞治疗多发性PAVF的初步体会:首先,通过超选择性肺动脉造影评估供血动脉直径,以便选择合适的栓塞材料。对于供血动脉直径<5 mm的PAVF可试用弹簧圈封堵,但是放置的第1枚弹簧圈直径最好要大于供血动脉直径的50%~60%,不仅有利于固定及血栓形成,还能有效降低异位体循环栓塞的发生率。对于供血动脉直径≥5 mm的PAVF,则可首选AVP进行封堵,不仅能够一次栓塞成功,还减少了手术曝光时间。同时,在目前实施疾病诊断相关分类(diagnosis related groups,DRGs)支付背景下,这种选择较释放多个弹簧圈栓塞治疗更经济高效。而复杂多发的PAVF,建议联合使用AVP和弹簧圈栓塞治疗。一般认为栓塞成功的标准是:(1)术后动脉血气稳定改善;观察1年以上瘤体消失。PAVF术后随访应包括询问症状、体格检查、指尖无创氧饱和度测定、超声心动图检查、胸部CT增强检查、栓塞后4~6周及1年时复查动脉血气,每3~5年评估小动静脉瘘的增长情况。
综上所述,经导管封堵PAVF是一种创伤性小、安全性高和近期疗效确切的介入治疗方法。PAVF治疗的目的是减少右向左分流,改善缺氧症状,预防严重并发症,故应该坚持适度原则,仅对供血动脉直径超过2 mm的PAVF进行栓塞治疗,对于供血动脉直径<5 mm的PAVF可试用弹簧圈封堵,对于供血动脉直径≥5 mm的PAVF则可首选AVP进行封堵,复杂多发的PAVF建议联合使用AVP和弹簧圈进行栓塞治疗。



