丁 浩 张吉翔
人着色性干皮病基因D(xeroderma pigmentosum D,XPD)是转录因子ⅡH(transcription factorⅡH,TFⅡH)的一个重要组分[1]。已有的研究显示,XPD除在TFⅡH介导的核苷酸切除修复和转录过程中发挥作用外,还参与细胞的增殖、凋亡及肿瘤的发生[2]。有研究表明,乙肝病毒X蛋白(Hepatitis B virus X protein,HBx)能通过P53的介导抑制XPD的表达[3],但XPD是否能通过P53的介导来影响HBx的表达目前鲜见相关报道。本研究将人XPD质粒转染人肝癌细胞HepG2.2.15,并给予P53抑制剂Pifithrin-α处理,探讨XPD与P53两者对肝癌细胞增殖以及HBx、Bcl-2和Bax表达的影响。
1 材料与方法
1.1 材料 人肝癌细胞HepG2.2.15由复旦大学附属华山医院感染科张轶俊博士惠赠。培养基DMEM购自Hyclone公司。胎牛血清购自Gibco公司。重组质粒pEGFP-N2/XPD和空载质粒pEGFP-N2由本实验室构建并保存,pEGFP-N2/XPD已通过PCR反应、酶切及基因测序三重鉴定[4]。LipofectamineTM2000和Trizol购自Invitrogen公司。Pifithrin-α购自Sigma公司。G418和MTT购自Solarbio。DMSO购自Amresco。逆转录试剂盒购自Fermentas公司。引物由Generay Biotech合成。2×Taq PCR MasterMix购自天根生物技术有限公司。总蛋白提取试剂盒购自北京普利莱基因技术有限公司。一抗XPD、HBx、Bcl-2、Bax和β-actin购自Santa Cruz公司。二抗辣根过氧化物酶IgG购自北京中杉金桥公司。
1.2 细胞培养、质粒的转染和Pifithrin-α的处理 将HepG2.2.15置于含10%胎牛血清、双抗(100 U/mL的青霉素和100 mg/L的链霉素)和400 mg/L G418的DMEM培养基的培养瓶中,37℃、饱和空气湿度和5%的CO2孵箱内培养。以1×105/孔的密度将细胞铺于6孔板内,24 h后细胞融合率约为90%。用脂质体转染法将重组质粒pEGFP-N2/XPD和空载质粒pEGFP-N2转染细胞,质粒每孔4.0 μg,脂质体每孔10 μL介导转染。转染后第2天给予20 μmol/L的Pifithrin-α孵育24 h。根据处理因素的不同分为5组,1组:空白对照组;2组:转染空载质粒pEGFP-N2;3组:转染重组质粒pEGFP-N2/XPD;4组:pEGFP-N2/XPD+Pifithrin-α;5组:Pifithrin-α。孵育结束后收获细胞。
1.3 RT-PCR检测mRNA表达水平 细胞总RNA抽提和逆转录参照试剂说明书进行操作。各基因引物序列和产物大小,见表1。PCR反应体系如下:cDNA 500 ng,上下游引物各1 μL,2×Taq PCR MasterMix 12.5 μL,补去离子水至终体积 25 μL。按下列条件进行扩增:预变性,1个循环,94℃5 min;PCR反应,35个循环,94℃ 40 s,56 ℃ 40 s,72℃ 55 s;延伸,72℃7 min。取5 μL PCR产物进行1.5%琼脂糖凝胶电泳,用暗箱式紫外透射仪观察电泳结果并拍照。结果用BANDLEAD 3.00软件,以目的条带/β-actin的光密度值进行分析。

Table 1 Gene primer sequence and product size表1 各基因引物序列和产物大小
1.4 Western blotting检测蛋白表达水平 用RIPA法取总蛋白,BCA法测定蛋白质浓度,取100 μg进行SDS-PAGE电泳分离蛋白。蛋白转印到硝酸纤维素膜上,脱脂奶粉溶液4℃封闭过夜。膜分别用按相应比例稀释的XPD、HBx、Bcl-2、Bax和β-actin的一抗孵育,4℃过夜,二抗孵育2 h,DAB显色照相。结果用Quantity One 4.62软件,以目的条带/β-actin的灰度值进行分析。
1.5 MTT检测细胞存活率 将细胞种植在96孔板中,空白调零孔只加不含细胞的培养基。实验处理后,每孔加入5 g/L MTT溶液20 μL,继续培养4 h,弃上清,加入150 μL DMSO,振荡15 min,酶标仪(Labststems,芬兰)测定492 nm处各孔吸光度(A)值。
1.6 流式细胞仪检测细胞周期 实验处理后,用胰酶消化收集上述各组细胞。采用碘化丙啶单染法,应用FACSCalibar流式细胞仪(Beckton Dickinson公司,USA)分析细胞周期,得出细胞各周期的百分率。
1.7 统计学处理 应用统计学软件SPSS 13.0进行统计分析,数据采用均数±标准差(±s)表示,多组间比较采用单因素方差分析,两两比较采用LSD-t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 各组mRNA表达水平比较 与空白对照组和pEGFP-N2组相比,pEGFP-N2/XPD的转染明显增加了XPD mRNA的表达;与空白对照组和pEGFP-N2组相比,pEGFP-N2/XPD组的HBx和Bcl-2 mRNA的表达明显减少,Bax mRNA的表达明显增多;与空白对照组相比,Pifithrin-α组的HBx和Bcl-2 mRNA的表达明显增多,Bax mRNA的表达明显减少;与pEGFP-N2/XPD组相比,pEGFP-N2/XPD+Pifithrin-α组的HBx和Bcl-2 mRNA的表达明显增多,Bax mRNA的表达明显减少;而空白对照组与pEGFP-N2组之间相比,差异无统计学意义,见图1、表2。
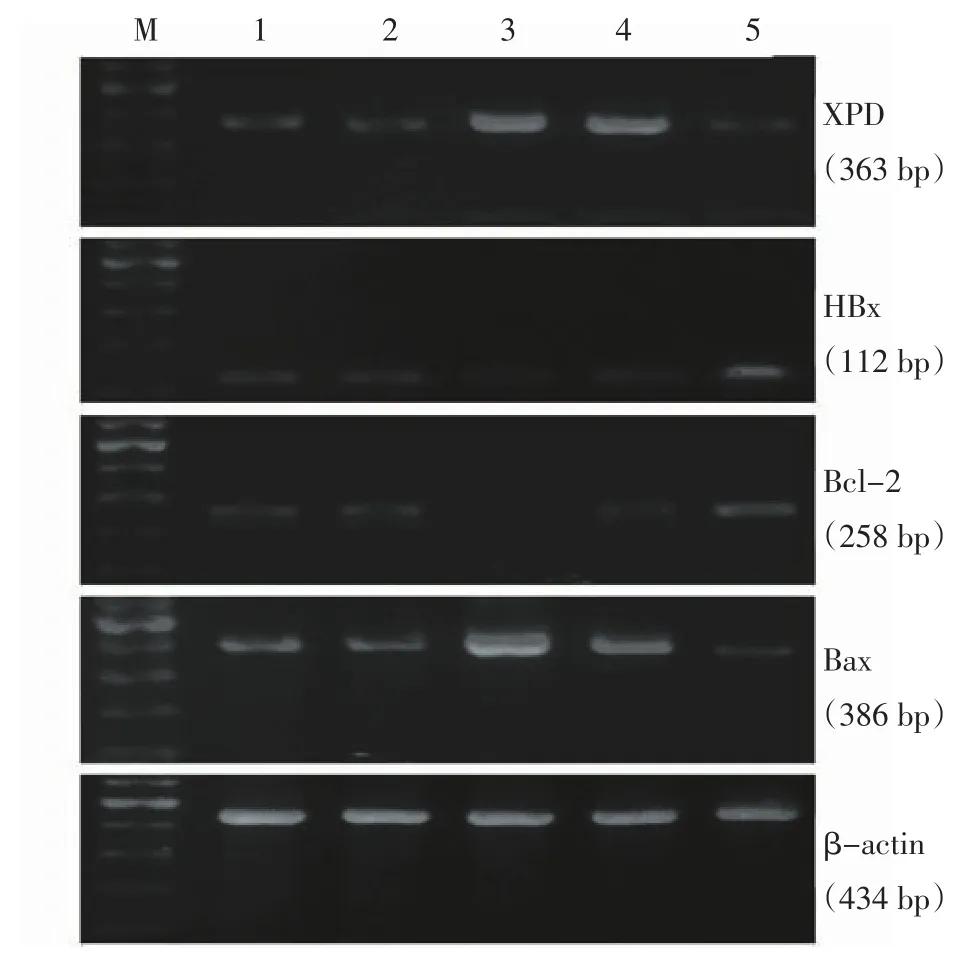
Figure 1 Electrophoresis of PCR图1 PCR电泳图
Table 2 Comparison of mRNA Expressions between gene groups表2 各组基因mRNA表达的比较 (±s,n=6)
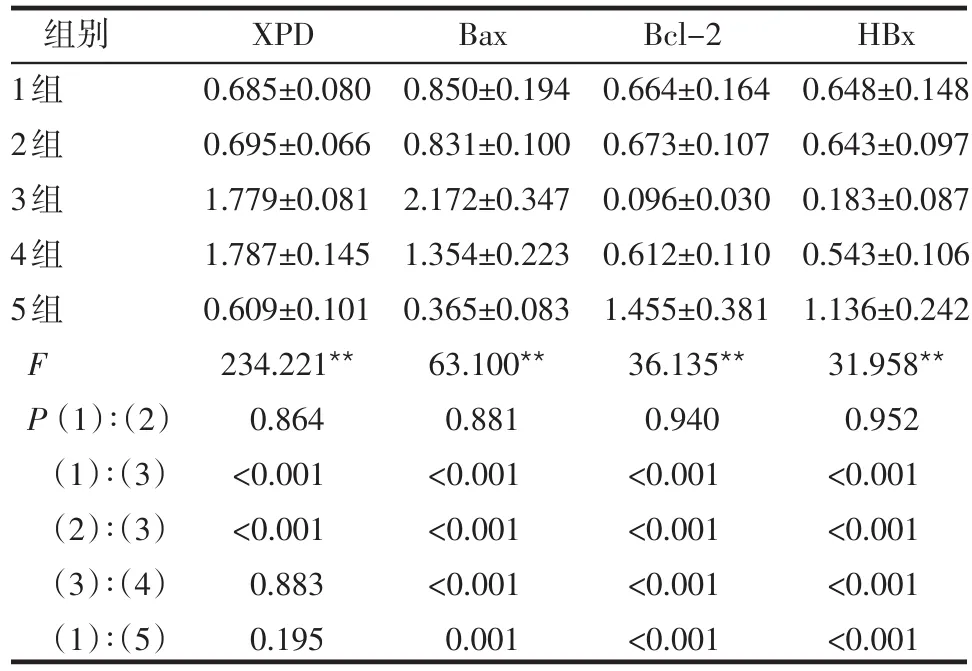
Table 2 Comparison of mRNA Expressions between gene groups表2 各组基因mRNA表达的比较 (±s,n=6)
**P<0.001
组别1组2组3组4组5组F P(1)∶(2)(1)∶(3)(2)∶(3)(3)∶(4)(1)∶(5)XPD 0.685±0.080 0.695±0.066 1.779±0.081 1.787±0.145 0.609±0.101 234.221**0.864<0.001<0.001 0.883 0.195 Bax 0.850±0.194 0.831±0.100 2.172±0.347 1.354±0.223 0.365±0.083 63.100**0.881<0.001<0.001<0.001 0.001 Bcl-2 0.664±0.164 0.673±0.107 0.096±0.030 0.612±0.110 1.455±0.381 36.135**0.940<0.001<0.001<0.001<0.001 HBx 0.648±0.148 0.643±0.097 0.183±0.087 0.543±0.106 1.136±0.242 31.958**0.952<0.001<0.001<0.001<0.001
2.2 各组蛋白表达水平比较 与空白对照组和pEGFP-N2组相比,pEGFP-N2/XPD组的转染明显增加了XPD蛋白的表达,HBx和Bcl-2蛋白的表达明显减少,Bax蛋白的表达明显增多;与空白对照组相比,Pifithrin-α组的HBx和Bcl-2蛋白的表达明显增多,Bax蛋白的表达明显减少;与pEGFP-N2/XPD组相比,pEGFP-N2/XPD+Pifithrin-α组的HBx和Bcl-2蛋白的表达明显增多,Bax蛋白的表达明显减少;而空白对照组与pEGFP-N2组之间相比,差异无统计学意义,见图2、表3。
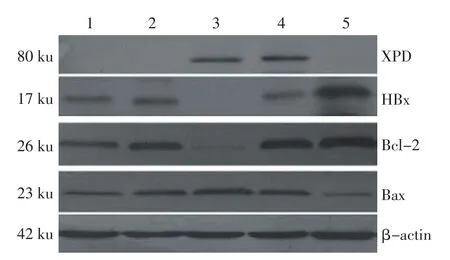
Figure 2 Electrophoresis of protein SDS-PAGE图2 蛋白SDS-PAGE电泳图
Table 3 Comparison of protein expression between gene groups表3 各基因蛋白表达的比较 (±s,n=6)
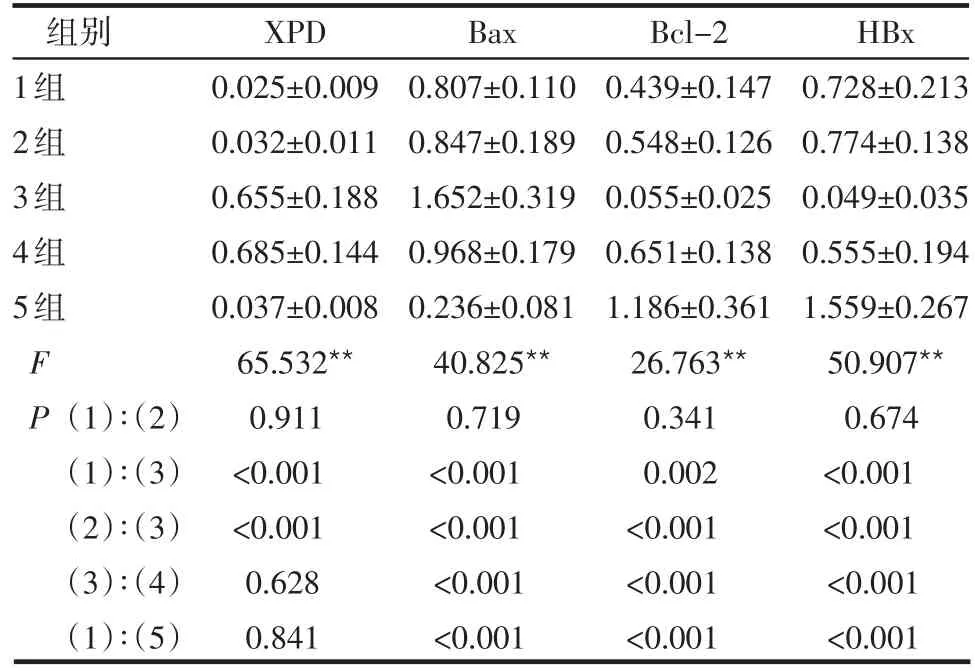
Table 3 Comparison of protein expression between gene groups表3 各基因蛋白表达的比较 (±s,n=6)
**P<0.001
组别1组2组3组4组5组F P (1)∶(2)(1)∶(3)(2)∶(3)(3)∶(4)(1)∶(5)XPD 0.025±0.009 0.032±0.011 0.655±0.188 0.685±0.144 0.037±0.008 65.532**0.911<0.001<0.001 0.628 0.841 Bax 0.807±0.110 0.847±0.189 1.652±0.319 0.968±0.179 0.236±0.081 40.825**0.719<0.001<0.001<0.001<0.001 Bcl-2 0.439±0.147 0.548±0.126 0.055±0.025 0.651±0.138 1.186±0.361 26.763**0.341 0.002<0.001<0.001<0.001 HBx 0.728±0.213 0.774±0.138 0.049±0.035 0.555±0.194 1.559±0.267 50.907**0.674<0.001<0.001<0.001<0.001
2.3 细胞增殖活力的变化 pEGFP-N2/XPD组的A值明显低于空白对照组和pEGFP-N2组;Pifithrin-α组的A值明显高于空白对照组;pEGFP-N2/XPD+Pifithrin-α组的A值明显高于pEGFP-N2/XPD组;而空白对照组与pEGFP-N2组之间相比,差异无统计学意义,见表4。
2.4 细胞周期的变化 与空白对照组和pEGFP-N2组相比,pEGFP-N2/XPD组的G1期细胞明显增多,S期细胞明显减少;与空白对照组相比,Pifithrin-α组的G1期细胞明显减少,S期细胞明显增多;与pEGFP-N2/XPD组相比,pEGFP-N2/XPD+Pifithrin-α组的G1期细胞明显减少,S期细胞明显增多;而空白对照组与pEGFP-N2组之间相比,G1期细胞和S期细胞差异均无统计学意义,见表4。
Table 4 Comparison of the cell proliferation and periodic variation between cell groups表4 各组细胞增殖活力和细胞周期变化比较(±s,n=6)
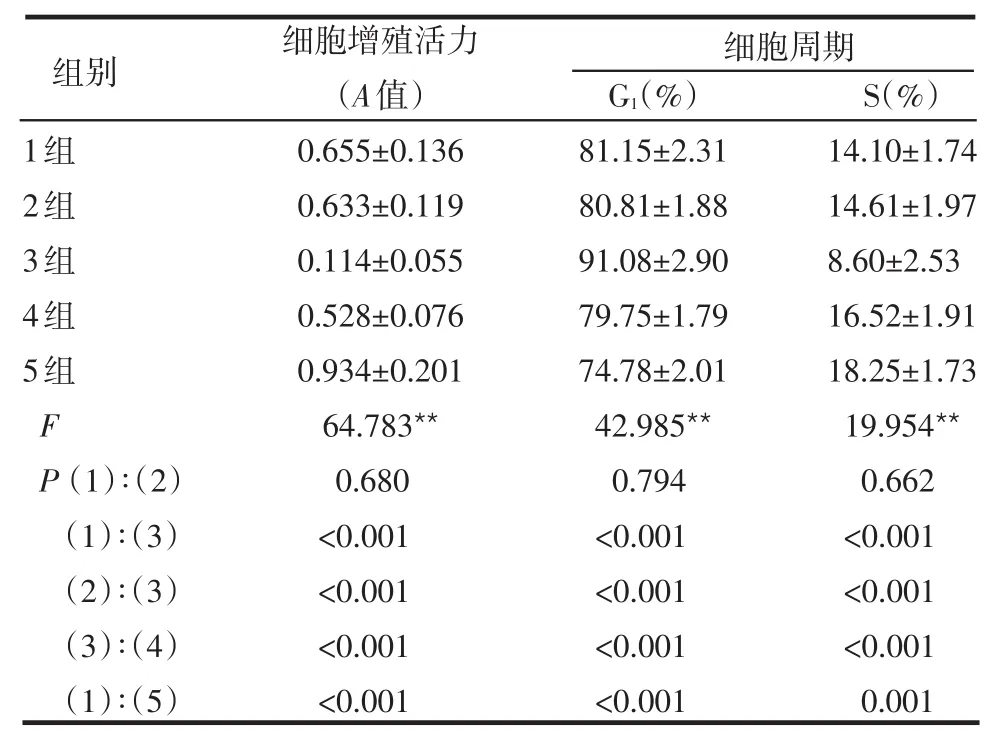
Table 4 Comparison of the cell proliferation and periodic variation between cell groups表4 各组细胞增殖活力和细胞周期变化比较(±s,n=6)
**P<0.001
组别 细胞周期1组2组3组4组5组F P(1)∶(2)(1)∶(3)(2)∶(3)(3)∶(4)(1)∶(5)细胞增殖活力(A值)0.655±0.136 0.633±0.119 0.114±0.055 0.528±0.076 0.934±0.201 64.783**0.680<0.001<0.001<0.001<0.001 G1(%)81.15±2.31 80.81±1.88 91.08±2.90 79.75±1.79 74.78±2.01 42.985**0.794<0.001<0.001<0.001<0.001 S(%)14.10±1.74 14.61±1.97 8.60±2.53 16.52±1.91 18.25±1.73 19.954**0.662<0.001<0.001<0.001 0.001
3 讨论
TFⅡH是一个由9个亚基(XPB,XPD,P62,P52,P44,P34,cdk7,cyclinHT和MATl)组成的多酶复合物,XPD作为一个支架,介导着复合物内部的连接[5]。XPD具有单链DNA解旋酶活性,参与了核酸剪切修复,其功能缺陷可导致突变的基因不能得到有效的修复,同时也会影响一些癌基因和抑癌基因的功能,从而促使肿瘤的发生[6]。而且笔者既往的研究显示,XPD基因能抑制肝癌细胞生长,促进肝癌细胞凋亡[7]。
p53基因有野生型和突变型,野生型是公认的抑癌基因。野生型p53是某些细胞内DNA损伤无法修复时导致细胞凋亡发生的重要调控基因,在维持细胞正常生长、抑制恶性增殖过程中起着重要作用,其缺失和变异与多数肿瘤的发生发展密切相关[8]。既往的研究发现,XPD能与P53结合并作用于P53,从而参与了P53诱导的凋亡过程[9]。而P53是否也参与了XPD诱导的凋亡过程尚有待于证实。原癌基因HBx能通过P53使得肝细胞的XPD表达下调[3]。
为此,本研究将重组质粒pEGFP-N2/XPD转染人肝癌细胞HepG2.2.15使得XPD表达增高,并给予Pifithrin-α抑制P53,然后检测细胞增殖以及HBx、Bcl-2和Bax表达的变化。本研究所用的细胞株HepG2.2.15是整合了HBV DNA的人肝癌细胞,能表达较高水平的HBx[10]。Pifithrin-α能可逆性地抑制P53依赖的基因转录激活,如Bax,也可增高Bcl-2的表达,还能抑制P53介导的细胞凋亡[11]。
本研究显示,重组质粒pEGFP-N2/XPD的转染能降低HepG2.2.15的增殖活力,使得停滞在G1期的细胞增多,S期细胞减少,说明XPD能抑制肝癌细胞生长,与笔者既往研究结果一致[7]。而XPD抑制生长的作用能被Pifithrin-α阻断,即XPD抑制肝癌细胞生长的作用是通过P53途径实现的。这证实,不仅XPD参与了P53诱导的凋亡过程[9],反过来,P53也参与了XPD诱导的凋亡过程,XPD与P53之间能相互调节。
本研究证实了XPD可下调HBx和Bcl-2的表达,上调Bax的表达。Bax和Bcl-2同属于Bcl-2基因家族,但前者是抑癌基因,后者是公认的癌基因。P53可直接下调Bcl-2的表达,激活Bax的表达[12]。在本研究中,XPD能下调Bcl-2的表达,上调Bax的表达,这进一步证实了XPD的抑癌作用。HBx蛋白是乙型肝炎病毒HBV合成的蛋白质,而且是HBV致肝癌的重要因素之一[13]。HBx能通过P53使得XPD表达下调[3]。而本研究显示,XPD也能下调HBx的表达,即XPD与HBx之间亦能相互调节。本研究结果显示,XPD下调HBx和Bcl-2表达以及上调Bax表达的作用能被Pifithrin-α阻断,表明XPD影响上述基因的表达是通过P53途径实现的。
本研究还发现,与空白对照相比,Pifithrin-α不仅能下调Bax的表达及上调Bcl-2的表达,而且能上调HBx的表达。而已有研究表明,HBx可抑制P53的活性或使其突变[14]。这表明P53与HBx之间亦能相互调节。
综上所述,XPD是通过P53途径抑制肝癌细胞增殖的;XPD能通过P53途径下调HBx和Bcl-2的表达以及上调Bax的表达;XPD、P53和HBx三者之间能相互作用、相互影响,共同调节肝癌的发生与发展。
[1]Coin F,Proietti De Santis L,Nardo T,et al.p8/TTD-A as a repair-specific TFIIH subunit[J].Mol Cell,2006,21(2):215-226.
[2]Laine JP,Mocquet V,Bonfanti M,et al.Common XPD(ERCC2)polymorphisms have no measurable effect on nucleotide excision repair and basal transcription[J].DNA Repair(Amst),2007,6(9):1264-1270.
[3]Jaitovich-Groisman I,Benlimame N,Slagle BL,et al.Transcription alregulation of the TFIIH transcription repair components XPB and XPD by the hepatitis B virus x protein in liver cells and transgenic liver tissue[J].J Biol Chem,2001,276(17):14124-14132.
[4]汤蕾,张吉翔,熊瑛.人着色性干皮病D组基因的克隆及其真核表达[J].生物医学工程学杂志,2008,25(3):668-672.
[5]Rudolf J,Rouillon C,Schwarz-Linek U,et al.The helicase XPD unwinds bubble structures and is not stalled by DNA lesions removed by the nucleotide excision repair pathway[J].Nucleic Acids Res,2010,38(3):931-941.
[6]Uhring M,Poterszman A.DNA helicases and human diseases[J].Med Sci(Paris),2006,22(12):1087-1094.
[7]Wang HY,Xiong GF,Zhang JX,et al.The role of XPD in cell apoptosis and viability and its relationship with p53 and cdk2 in hepatoma cells[J].Med Oncol,2011 Jan 25.[Epub ahead of print]
[8]Goldstein I,Marcel V,Olivier M,et al.Understanding wild-type and mutant p53 activities in human cancer:new landmarks on the way to targeted therapies[J].Cancer Gene Ther,2011,18(1):2-11.
[9]Robles AI,Wang XW,Harris CC.Drug-induced apoptosis is delayed and reduced in XPD lymphoblastoid cell lines:possible role of TFIIH in p53-mediated apoptotic cell death[J].Oncogene,1999,18(33):4681-4688.
[10]Wu KL,Zhang X,Zhang J,et al.Inhibition of Hepatitis B virus gene expression by single and dual small interfering RNA treatment[J].Virus Res,2005,112(1-2):100-107.
[11]Javelaud D,Besancon F.Inactivation of p21WAF1 sensitizes cells to apoptosis via an increase of both p14ARF and p53 levels and an alteration of the Bax/Bcl-2 ratio[J].J Biol Chem,2002,277(40):37949-37954.
[12]Pratheeshkumar P,Kuttan G.Vernolide-A,a sesquiterpene lactone from Vernonia cinerea,induces apoptosis in B16F-10 melanoma cells by modulating p53 and caspase-3 gene expressions and regulating NF-κB-mediated bcl-2 activation[J].Drug Chem Toxicol,2011,34(3):261-270.
[13]De Mitri MS,Cassini R,Bernardi M.Hepatitis B virus-related hepatocarcinogenesis:molecular oncogenic potential of clear or occult infections[J].Eur J Cancer,2010,46(12):2178-2186.
[14]Gouas DA,Shi H,Hautefeuille AH,et al.Effects of the TP53 p.R249S mutant on proliferation and clonogenic properties in human hepatocellular carcinoma cell lines:interaction with hepatitis B virus X protein[J].Carcinogenesis,2010,31(8):1475-1482.



