张卉,王道清,程留慧,黄方方


摘要目的:研究人工智能(AI)应用于冠状动脉电子计算机断层扫描(CT)血管成像对冠状动脉狭窄的诊断效能及临床意义。方法:以2018年1月—2022年9月我院收治的168例行冠状动脉CT血管成像检查病人为研究对象,所有病人均进行冠状动脉造影确诊,分别采用后处理软件Syngo.via(人工组)和联影AI冠状动脉智能辅助诊断系统软件(AI组)对冠状动脉CT血管成像进行图像后处理,比较两种方法评价冠状动脉CT血管成像图像质量、冠状动脉狭窄的检出情况及诊断效能。结果:AI组和人工组图像质量评价优、良、差病人分布及图像缺陷原因占比差异均无统计学意义(P>0.05)。168例病人共发生冠状动脉狭窄89例,其中人工检出83例,AI检出71例;无冠状动脉狭窄79例,其中人工检出60例,AI检出70例。AI诊断冠状动脉狭窄的敏感度低于人工组,但特异度高于人工组(P<0.05),同时两者曲线下面积(AUC)比较差异无统计学意义(P>0.05)。结论:AI应用于冠状动脉CT血管成像的图像后处理,其图像质量评价及对冠状动脉狭窄的诊断效能与人工相当,可用于临床辅助影像医师进行冠状动脉狭窄的诊断。
关键词冠状动脉狭窄;人工智能;电子计算机断层扫描;血管成像;诊断效能
doi:10.12102/j.issn.1672-1349.2024.08.005
冠心病是临床常见心血管疾病,评估冠状动脉狭窄情况是诊断冠心病的重要步骤,冠状动脉造影(CAG)是临床诊断冠状动脉狭窄的金标准,但其费用昂贵,且属于有创检查[1-2]。近年来,随着冠状动脉电子计算机断层扫描(CT)血管成像的广泛应用,其已经成为临床筛查冠状动脉狭窄的首选无创检查方法,但影像医师对图像后处理和结果判读过程所用时间较长,影响工作效率的同时影响判读结果,增加误诊、漏诊的风险[3]。近年来,人工智能(AI)技术在医疗行业的应用越来越广泛,其借助计算机视觉、深度学习、大数据平台等技术使得临床诊疗服务更加的便捷和精确,在提高影像医师工作效率、缓解医师工作压力和强度方面起着积极作用[4],而目前关于AI在冠状动脉CT血管成像中的应用情况尚未完全明确,基于此,本研究将AI应用于冠状动脉CT血管成像,分析其对冠状动脉狭窄的诊断效能及临床意义。
1资料与方法
1.1一般资料
选取2018年1月—2022年9月河南中医药大学第一附属医院收治的168例行冠状动脉CT血管成像检查病人为研究对象,男89例,女79例;年龄27~85(57.41±3.72)岁;心率51~104(75.94±4.88)次/min。
1.2纳入、排除、脱落与剔除标准
纳入标准:参照相关文献[5]进行冠状动脉狭窄的诊断;无精神障碍、语言障碍、听力障碍,能配合医师指令完成相关检查者;冠状动脉CT血管成像图像血管伪影少,不影响结果判断者;与CAG检查时间间隔短于2周者;AI软件能自动计算完成者等。排除标准:冠状动脉开口异常者;行心脏搭桥术或冠状动脉支架置入术者等。脱落与剔除标准:相关数据丢失者。
1.3检查方法
1)冠状动脉CT血管成像:使用一代双源CT行冠状动脉CT血管成像检查,先进行气管分叉处下1.0~1.5 cm至心脏膈面头足方向的心电门控扫描序列扫描,无硝酸甘油禁忌病人扫描前舌下含服0.5 mg硝酸甘油,后进行增强扫描,参数设定管电流为实时动态曝光剂量调剂自动曝光,管电压120 kV,开启实时动态曝光剂量调剂自动曝光,旋转时间为每周0.28 s,层间距0.5 mm,重建图像层厚0.75 mm,重建算法采用B 26 fmedi·umsmoothAsA,注射对比剂后运用对比剂追踪触发技术进行检查。2)图像后处理:扫描完成后选择图像数据传输至西门子工作站,利用后处理软件Syngo.via(人工组)和联影AI冠状动脉智能辅助诊断系统软件(AI组)进行图像后处理。人工组主要由影像科技师完成后处理,AI组由AI冠状动脉软件自动进行。
1.4观察指标
1.4.1人工和AI对冠状动脉CT血管成像图像质量评价
所有图像均经3位专业影像医师进行图像质量评价,图像质量评定包括优、良、差[6];统计良和差图像缺陷原因,包括血管遮挡、组织、静脉干扰或杂质污染、血管缺如或误添加。
1.4.2人工和AI对冠状动脉狭窄的检出情况
根据图像后处理结果统计人工组和AI组冠状动脉狭窄的检出情况。
1.4.3人工和AI对冠状动脉狭窄的诊断效能
采用受试者工作特征曲线(ROC)分析人工和AI对冠状动脉狭窄的诊断效能。
1.5统计学处理
数据分析使用SPSS 21.0统计软件进行,定性资料采用例数、百分比(%)表示,比较采用χ2检验;绘制ROC曲线,获取曲线下面积(AUC)分析人工和AI对冠状动脉狭窄的诊断效能。以P<0.05为差异有统计学意义。
2结果
2.1人工和AI对冠状动脉CT血管成像图像质量评价比较
AI组和人工组图像质量评价优、良、差病人分布及图像缺陷原因分布差异均无统计学意义(P>0.05)。详见表1。
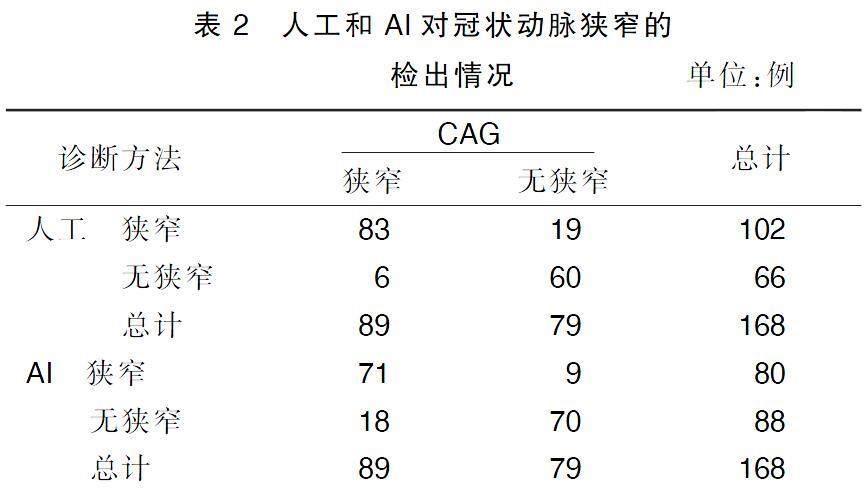
2.2人工和AI对冠状动脉狭窄的检出情况比较
168例病人共发生冠状动脉狭窄89例,其中人工检出83例,AI检出71例;无冠状动脉狭窄79例,其中人工检出60例,AI检出70例。详见表2。
2.3人工和AI对冠状动脉狭窄的诊断效能比较
AI诊断冠状动脉狭窄的敏感度低于人工组,但特异度高于人工组(P<0.05),同时两者AUC值比较差异无统计学意义(P>0.05)。详见表3及图1。
2.4典型病例影像资料
典型病例[1],男,45岁,Sigovia工作站冠状动脉软件后处理图见图2。典型病例[2]AI自动识别和分割后处理图见图3。
3讨论
冠状动脉狭窄是冠心病的主要病因,近年来,随着人们生活方式的改变,冠状动脉狭窄发病率逐年升高,冠状动脉CT血管成像对冠状动脉狭窄进行准确、快速的诊断,为临床治疗提供了参考和依据,但其图像后处理工作量较大,使得影像医师日常工作强度较大,工作效率较低,难以满足现代医院的需求[7-8]。AI作为计算机科学延伸的一门新兴技术,在医学影像大数据时代,将其应用于心血管影像中有利于减轻影像医师的工作量,提高其工作效率及诊断准确率[9-10]。
在应用AI进行冠状动脉CT血管成像图像后处理过程中发现,AI冠状动脉智能辅助诊断系统软件在进行图像重建的过程中会删除部分冠状动脉CT血管成像图像重建步骤而缩短图像后处理用时,但其在图像着色和渲染方面的视觉感观强于人工重建[11]。本研究中AI组和人工组图像质量评价优、良、差病人分布及图像缺陷原因分布差异均无统计学意义,但AI组图像质量优秀率高于人工组,原因在于,容积再现图像中冠状动脉贴合紧密,且容易受静脉血管的干扰,在人工重建过程中很难去除[12-13],而AI在图像局部细节的色彩渲染十分优秀,可有效识别并去除静脉血管,但在AI处理过程中也同样存在组织、静脉干扰或杂质污染及血管缺如或误添加等因素对图像质量产生影响,这些因素的产生一方面可能与病人心率过快、心律不齐、体重过大等因素有关[14],另一方面可能与曝光剂量、重建算法等扫描参数有关[15],结合AI冠状动脉智能辅助诊断系统软件功能分析,当软件和仪器在学习的初级阶段获取诸如以上原因造成的非优质数据没得到足够的训练时,使得图像后处理质量降低[16-17]。
在现今大数据时代,AI应用于影像学疾病的诊断已经成为不可逆转的潮流趋势,对于心血管疾病病人,其对冠状动脉狭窄的诊断效能与其是否能在冠心病辅助诊断中广泛应用密切相关。本研究结果显示,AI诊断冠状动脉狭窄的敏感度、特异度及AUC值分别为79.78%、88.61%、0.842,其中敏感度低于人工,但特异度高于人工,而两者AUC值比较差异无统计学意义,说明AI对冠状动脉狭窄的诊断效能良好,可辅助影像医师进行冠状动脉狭窄的诊断。但在临床实际应用过程中,发现AI在辅助诊断冠状动脉狭窄的过程中也存在较多不足之处:1)对于受心率或呼吸运动影响使得图像有明显错层及冠状动脉起源异常、搭桥术后病人等变量结果较多,但缺乏大样本数据训练时,AI的程序算法会受到较大的限制,病人血管走行表现较多,导致AI解读困难,因此,这类病人在进行冠状动脉CT血管成像时应避免使用AI进行图像后处理,以免影响结果的判读及浪费医疗资源[18-19]。2)AI在血管命名准确率方面也存在着一定的误差,如对于冠状动脉左旋支中远段、钝缘支等血管标示命名可能出现错误[20]。3)冠状动脉钙化情况、狭窄程度等也会对AI判断结果产生影响[21]。因此,AI在冠状动脉狭窄诊断中应用的有效性和安全性还需要临床优质大样本数据的支撑和质量控制的介入。
AI应用于冠状动脉CT血管成像的图像后处理,其图像质量评价及对冠状动脉狭窄的诊断效能与人工相当,可用于临床辅助影像医师进行冠状动脉狭窄的诊断。本研究为小样本、单中心研究,仅对病人是否出现冠状动脉狭窄进行统计,而未具体到血管及相关节段,且未对血管钙化情况进行区分,可能使得研究结果存在偏倚,因此,有待后续研究进一步扩大样本量,联合其他医院的学者进行多中心研究,分析AI应用于冠状动脉CT血管成像对冠状动脉狭窄的诊断效能。
参考文献:
[1]KAWASHIMA H,KOGAME N,ONO M,et al.Diagnostic concordance and discordance between angiography-based quantitative flow ratio and fractional flow reserve derived from computed tomography in complex coronary artery disease[J].J Cardiovasc Comput Tomogr,2022,16(4):336-342.
[2]廖付军,鲍海龙,谢登海,等.冠心病患者胆红素血脂综合指数与冠状动脉狭窄程度的相关性[J].贵州医科大学学报,2021,46(8):925-930.
[3]SUN B,CHEN Z Y,DUAN Q,et al.A direct comparison of 3T contrast-enhanced whole-heart coronary cardiovascular magnetic resonance angiography to dual-source computed tomography angiography for detection of coronary artery stenosis:a single-center experience[J].Journal of Cardiovascular Magnetic Resonance,2020,22(1):40.
[4]李浚利,韩丹,段慧,等.AI在CCTA诊断冠状动脉狭窄中的准确性及应用价值[J].中国医学计算机成像杂志,2020,26(2):120-124.
[5]赵勇,吕宜凤.现代心血管病学[M].天津:天津科学技术出版社,2011:55-58.
[6]冯涛,田力.产前超声诊断右冠状动脉右房瘘1例[J].中国超声医学杂志,2022,38(10):1152.
[7]BAO W R,CHEN C H,YANG M,et al.A preliminary coronary computed tomography angiography-based study of perivascular fat attenuation index:relation with epicardial adipose tissue and its distribution over the entire coronary vasculature[J].European Radiology,2022,32(9):6028-6036.
[8]王曼,王怡宁,于敏,等.人工智能成像优化技术在冠状动脉CT血管成像的初步应用研究[J].中华放射学杂志,2020,54(5):460-466.
[9]刘佩君,王怡宁,于敏,等.人工智能优化算法对提高大体型患者低剂量扫描冠状动脉图像质量的价值[J].放射学实践,2019,34(7):760-766.
[10]黄增发,王翔.人工智能冠状动脉CT血管成像在冠心病诊断中的应用[J].放射学实践,2018,33(10):1017-1021.
[11]杨阳,刁楠,黄增发,等.CAD-RADS在冠心病诊断中的应用:人工智能与人工方法的对照研究[J].放射学实践,2022,37(4):413-418.
[12]赵润涛,窦冠华,王凡,等.基于人工智能动态CT心肌灌注成像分析技术的临床应用研究[J].国际医学放射学杂志,2021,44(5): 529-534.
[13]王宪凯,贾学燕,程祥科,等.人工智能在冠状动脉CTA图像后处理及狭窄评估中的应用价值[J].医学影像学杂志,2022,32(4):588-590.
[14]韦佳,鲍海华,王雪燕,等.基于人工智能的CT-FFR与冠状动脉狭窄的相关性分析[J].中国动脉硬化杂志,2022,30(9):787-792.
[15]李浚利,黄益龙,韩丹,等.冠状动脉CT血管成像中人工智能诊断冠心病的准确性[J].中国医学影像技术,2021,37(1):59-62.
[16]张晓浩,刘军波,范丽娟.人工智能技术应用于冠状动脉CTA图像后处理的可行性[J].放射学实践,2021,36(8):994-999.
[17]孙会利,陈杰,张焕,等.基于人工智能技术的非门控胸部CT平扫对冠状动脉钙化积分的准确性评价[J].CT理论与应用研究,2021,30(1):106-113.
[18]刘春雨,谢媛,苏晓芹,等.基于人工智能的冠状动脉CT血管成像检测阻塞性冠状动脉狭窄效能的研究[J].国际医学放射学杂志,2021,44(5):516-522.
[19]张明多,南楠,兰宏志,等.基于人工智能优化与计算流体力学的无创血流储备分数对冠状动脉狭窄缺血的诊断价值[J].心肺血管病杂志,2022,41(3):243-247.
[20]王平,陈亮,胡磊.人工智能+结构化报告赋能冠脉CT血管成像临床一体化[J].中国数字医学,2021,16(11):50-54.
[21]尹伟,王敏杰,徐瑞敏,等.基于人工智能的辅助运动校正算法对CCTA图像质量的影响[J].放射学实践,2022,37(8):1035-1041.
(收稿日期:2023-01-06)
(本文编辑王雅洁)



