于明良 刘丽 彭晓红 杨文超
(1.华中科技大学同济医学院附属武汉普爱医院麻醉科,湖北 武汉 430022; 2.武汉大学人民医院重症医学科,湖北 武汉 430022)
氯胺酮联合可乐定对神经病理性痛大鼠疼痛感觉分辨和情绪体验的影响
于明良1刘丽2△彭晓红1杨文超1
(1.华中科技大学同济医学院附属武汉普爱医院麻醉科,湖北 武汉 430022; 2.武汉大学人民医院重症医学科,湖北 武汉 430022)
目的 对神经病理性痛大鼠在联合使用氯胺酮(KET)与可乐定条件下其疼痛分辨和情绪体验受影响的情况进行观察。方法 雄性SD大鼠30只,分为假手术组(S组)、坐骨神经结扎模型组(C组)、氯胺酮组(K组)、可乐定组(CL组)、氯胺酮+可乐定组(KC组)。C组、K组、CL组和KC组采用坐骨神经慢性压迫法(CCI)制备大鼠神经病理性痛模型,S组仅暴露坐骨神经,不结扎。术后3~10d,每天给予K组氯胺酮(0.3 mg/kg)、CL组可乐定(1 μg/kg)、KC组氯胺酮(0.3 mg/kg) +可乐定(1 μg/kg)鞘内注射,S组和C组鞘内注射等容量生理盐水。各组分别于术前、术后3、7、10 d测定机械痛阈和热痛阈,各组于术后第10天行反映痛情绪的大鼠位置逃避实验(PEAP)。结果 与S组比较,C组、K组、CL组、KC组术后机械痛阈和热痛阈降低(P<0.05),其在白室所待时间延长(P<0.05);与C组比较,K组、CL组、KC组术后机械痛阈和热痛阈升高(P<0.05),其在白室所待时间缩短(P<0.05);与K组、CL组比较,KC组术后机械痛阈和热痛阈升高(P<0.05),其在白室所待时间明显缩短(P<0.05),减少了其位置逃避行为。结论 在联合应用氯胺酮及可乐定的情况下,神经病理性疼痛大鼠所存在的热痛和机械痛过敏现象能够得到有效的抑制,而且CCI大鼠的痛行为和痛相关负性情绪也会得到较大的改善。
神经病理性疼痛; 痛相关负性情绪; 氯胺酮; 可乐定
神经病理性疼痛是因为神经系统功能紊乱或者是最初的损伤而造成的疼痛,它是一种慢性状态,不但包括外周或者中枢神经系统的功能紊乱,还包括损伤和疾病。研究表明作为非竞争性N-甲基-D-天冬氨酸受体(NMDA)拮抗剂的氯胺酮(KET),在神经病理性疼痛的治疗中发挥了重要作用[1]。而可乐定是一种α2受体激动剂,也具有一定的治疗疼痛的作用。D.H.Roh[2]等发现,鞘内注射可乐定可抑制由注射NMDA引起的大鼠疼痛反应及磷酸化NR1的表达。本研究拟通过将氯胺酮和可乐定向鞘内注射的方法,观察对其所产生的镇痛作用效果以及影响慢性病理性痛大鼠的情绪体验及疼痛感觉分辨的情况进行初步的观察与探究。
1 材料与方法
1.1 实验动物 实验共选取了30只SD大鼠,分为五组,每组6只,分别为假手术组(S组)、坐骨神经结扎组(C组)、氯胺酮组(K组)、可乐定组(CL组)及氯胺酮+可乐定组(KC组)。
1.2 模型制备 参照文献[3]的方法,麻醉大鼠后,游离大鼠坐骨神经,用4-0丝线在坐骨神经干位置扎四道,每道间隔约1 mm,结扎的松紧程度以不对血运造成影响为宜。其中S组并不结扎,仅将坐骨神经暴露,其余各组均制作坐骨神经结扎模型。术后3~10 d,每天给予K组氯胺酮(0.3 mg/kg)、CL组可乐定(1 μg/kg)、KC组氯胺酮(0.3 mg/kg) +可乐定(1 μg/kg)鞘内注射,S组和C组鞘内注射等容量生理盐水。
1.3 药品、试剂和仪器情况 盐酸氯胺酮注射液(福建古田药业有限公司,批号:KH140309);可乐定(湖北随州天丰化工科技有限公司,批号:201405200411);PL-200热辐射仪(成都泰盟科技有限公司);位置逃避实验箱(自制)。
1.4 行为学测定 各组大鼠分别在术前、术后3、7、10 d时测定机械痛阈(MWT)和热痛阈(TWL)。(1)机械痛阈:采用up-down法计算对大鼠的机械痛阈进行测定[4]。把大鼠放置在箱子中适应30 min以上,箱子为30 cm×40 cm×60 cm的有机玻璃箱,底部为1 cm× 1 cm的铁丝网,采用von Frey纤维丝测定机械缩足反射阈值(PWT)。(2)热痛阈(TWL):参照Hargreaves等[5]的方法测定热痛阈,热辐光源通过3 mm厚的玻璃板对大鼠右后肢足底的中部进行照射,并对其缩足反应出现的时间予以记录,且每隔5 min测定一次,连测3次,取其平均值作为热痛阈。(3)位置逃避实验:术后第10天进行位置逃避实验,参考C.J.LaBuda等[6]方法。将动物放于安静、独立的环境中,使其适应环境至少1 h,测试箱为有机玻璃箱(60 cm × 30 cm × 30 cm),其一半为暗室,另一半明室环境。在测试开始的30 min内允许大鼠在测试箱中自由活动。测试时将其放入测试箱中央,每隔15 s 用60 g Von Frey纤毛刺激大鼠后足底中部,当大鼠停留在暗室时刺激其患侧足,在明室时刺激其健侧足。每隔5 min记录大鼠在明室和暗室分别所待时间。
2 结 果
2.1 大鼠机械痛阈和热痛阈变化情况 各组大鼠在术前1 d的机械痛阈和热痛阈比较差异无统计学,P>0.05。较之术前以及S组,K组、CL组和KC组大鼠机械痛阈和热痛阈明显降低,P<0.05;较之C组,K组、CL组和KC组大鼠在术后的3、7、10 d都出现了机械痛阈和热痛阈明显升高,P<0.05;较之K组、CL组,KC组术后机械痛阈和热痛阈升高,P<0.05。见表1,表2。
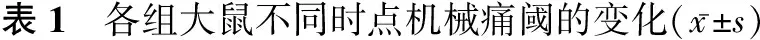

组别n术前术后不同时段3d7d10dS621.7±2.321.5±3.122.6±3.323.2±2.8C623.1±3.211.9±3.3#△6.8±2.1#△9.3±1.6#△K622.6±1.913.7±2.2#△▲14.2±3.1#△▲14.9±2.4#△▲CL623.1±2.613.1±2.9#△▲13.6±2.8#△▲14.8±2.8#△▲KC622.4±1.915.2±2.1#△▲16.4±2.4#△▲★☆17.6±2.4#△▲★☆
注:与S组比较,#P<0.05;与术前比较,△P<0.05;与C组比较,▲P<0.05;与K组比较,★P<0.05;与CL组比较,☆P<0.05。
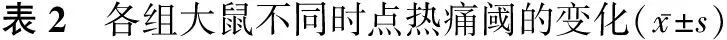

组别n术前术后不同时段3d7d10dS611.4±0.811.4±0.311.5±0.9 11.5±0.8C611.5±0.47.2±0.8#△8.01±0.8#△ 8.2±0.8#△K611.2±0.47.8±0.4#△▲8.23±0.2#△▲9.2±0.7#△▲CL611.3±0.47.7±0.4#△▲8.25±0.3#△▲8.6±1.2#△▲KC611.6±0.59.4±1.3#△▲ 9.9±1.5#△▲★☆ 10.2±1.1△▲★☆
注:与S组比较,#P<0.05;与术前比较,△P<0.05;与C组比较,▲P<0.05;与K组比较,★P<0.05;与CL组比较,☆P<0.05。
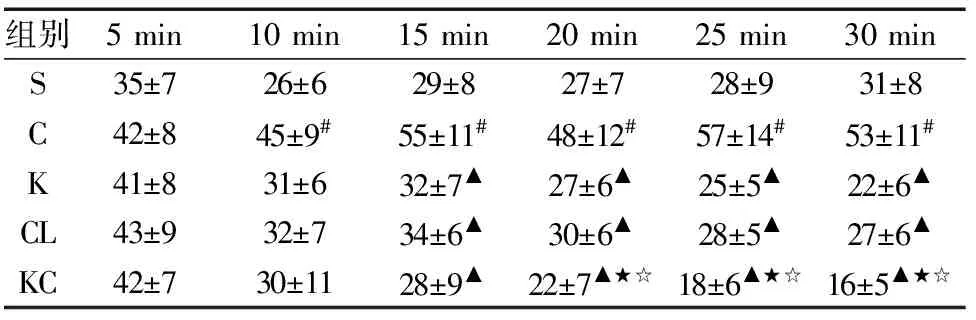
2.3 鞘内注射氯胺酮和可乐定对CCI大鼠位置逃避行为的影响 C组与S组相比,其在白室所待时间明显增加(P<0.05),提示CCI大鼠表现出明显的痛厌恶情绪。鞘内注射氯胺酮和可乐定组0.5 h后,K组、CL组和KC组与C组相比,其在白室所待时间明显缩短(P<0.05);与K组和CL组相比,KC组在白室所待时间均明显缩短(P<0.05),位置逃避行为减少,此作用在实验开始后20 min具有统计学意义(P<0.05) ,见表3。
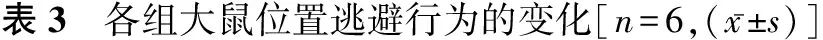
组别5min10min15min20min25min30minS35±726±629±827±728±931±8C42±845±9#55±11#48±12#57±14#53±11#K41±831±632±7▲27±6▲25±5▲22±6▲CL43±932±734±6▲30±6▲28±5▲27±6▲KC42±730±1128±9▲22±7▲★☆18±6▲★☆16±5▲★☆
注:与S组相比,#P<0.05;与C组比较,▲P<0.05;与K组比较,★P<0.05;与CL组比较,☆P<0.05。
3 讨 论
目前临床上神经病理性疼痛的发病率呈现快速增长,疼痛及负性情绪给患者的身心造成了严重的损害。T.T.Li等[7]研究发现周围炎性痛可导致前扣带皮层(ACC)内NMDA的NR2A和NR2B两种受体亚基表达上调,易化其突触传递过程,增强ACC内神经元兴奋性,提示NMDA受体的NR2A、NR2B亚基参与痛相关厌恶情绪的形成。相关研究表明神经病理性疼痛发展过程中激活NMDA受体,导致钙离子内流,内流的Ca2+与CaM结合,进而磷酸化激活CaMKII,p-CaMKII又可以磷酸化激活NR2B,导致痛相关负性情绪的形成,因此推测抑制NMDA受体的激活,就可以有效抑制痛相关负性情绪的形成。
氯胺酮和可乐定单独使用都可以用于神经病理性疼痛的治疗。氯胺酮通过阻断NMDA受体,直接抑制PKC的活性,减少GAP-43的生成。还可以通过降低Ca2+浓度抑制GaM与GAP-43的解离,使GAP-43释放减少,通过这两条途径使脊髓的中枢敏化减轻,缓解痛觉过敏[8]。但氯胺酮对交感神经和循环有兴奋作用,会导致血压升高、心率增快、眼内压和颅内压升高,兴奋边缘系统,出现恶梦幻觉等不良反应[9]。
研究[10]表明中枢性α2受体参与氯胺酮镇痛作用,作为α2受体激动剂的可乐定可能通过抑制谷氨酸的释放,加强氯胺酮的镇痛作用。而可乐定亦可以通过调节Ca2+的浓度使GAP-43的表达下调而减轻疼痛。并且可乐定可以降低高血压、减慢心率、镇静和一定的镇痛作用,从药理作用上可以拮抗氯胺酮的副作用,两者合用具有协同互补的作用。
本实验观察发现氯胺酮和可乐定联合使用对坐骨神经结扎大鼠的热痛阈及机械痛阈在术后3、7、10 d都有明显的提升。在坐骨神经结扎术后10 d,氯胺酮联合可乐定组大鼠位置逃避行为减少,提示氯胺酮联合可乐定鞘内给药的镇痛效果优于氯胺酮或者可乐定单独使用,且未发现单独使用氯胺酮所出现的易激惹、烦躁等不良反应。综上所述,氯胺酮联合可乐定使用通过不同的作用机制发挥协同镇痛的作用,不仅可以减少副作用,还具有更理想的镇痛效果,对于神经病理性疼痛的治疗提供了新的思路。
[1] Poyhia R,Vainio A.Topically administered ketamine reduces caps-aicin-evoked mechanical hyperalgesia[J].Clin J Pain,2006,22:32-36.
[2] Roh DH,Seo HS,Yoon SY,et al.Activation of spinal alpha-2 adrenoc-eptors,but not mu-0pioid receptors,reduces the intrathecal N-methyl-D-aspartate-induced increase in spinal NR1 subunit phosphorylation and nociceptive behaviors in the rat J[J].Anesth Analg,2010,110(2):622-629.
[3] Bennett GJ,Xie YK.A peripheral mononeuropathy in rat that produces disorders of pain sensation like those seen in man[J].Pain,1988,33 :87-107.
[4] Chaplan SR,Bach FW,Pogrel JW,et a1.Quantitative assessment of tactile allodynia in the rat paw[J].J Neurosci Methods,1994,53 :55-63.
[5] Kubota T,Hirota K,Yoshida H,et a1.Inhibitory effect of clonidine on ketamine-induced norepinephrine release from the medial prefronta1 cortex in rats[J].Br J Anaesth,1999,83 :945-947.
[6] LaBuda CJ,Fuchs PN.A behavioral test paradigm to measure the aver-Sive qulity of inflammatory and neuropathic pain in rats[J].Exp Neurol,2000,163:490-494.
[7] Li TT,Ren WH,Xiao X,et al.NMDA NR2A and NR2B receptors in the Rostral anerior cingulate cortex contribute to pain-related aversion in male rate[J].Pain,2009,146:183-193.
[8] 赖逾鹏,魏绪红,刘先国.N-甲基-D-天门冬氨酸受体在神经病理性疼痛中的作用[J].中山大学学报(医学科学版),2009,30(4s):280-282.
[9] 李俊毅,李建红,李克勤.氯胺酮麻醉并发症和不良反应初探[J].贵州医药,2013,37(5):432-433.
[10] 邢艳红,冷玉芳,王殊秀,等.可乐定与右美托咪定对慢性神经病理性痛大鼠背根神经节生长相关蛋白-43 mRNA表达的影响[J].中华医学杂志,2012,92(7):444-447.
武汉市卫计委科研基金(编号:WX14C63)
R614.R-332
B
1000-744X(2016)03-0251-03
2015-09-08)
△通信作者



