周 蓓,陶少平,杭 宇
(皖南医学院附属第二医院内分泌科,安徽芜湖241000)
2型糖尿病(T2DM)常并发大血管病变。近年来研究发现慢性炎症与T2DM及其大血管病变密切相关[1]。罗格列酮能改善胰岛素抵抗和降低血糖,其降糖以外的效应越来越受到重视。本研究通过检测T2DM患者高敏C反应蛋白(hsCRP)变化,探讨慢性炎症反应与T2DM大血管病变的关系,并分析罗格列酮的抗炎作用及其对大血管的保护机制。
1 临床资料
1.1 一般资料 T2DM 组68例(男39例,女29例)均为本院门诊或住院患者,符合1997年糖尿病诊断标准,平均年龄(51±9)岁,排除合并严重感染、肝肾功能异常、其他内分泌疾病、糖尿病酮症酸中毒者。根据是否合并大血管病变,分为大血管病变组(A组)36例和无大血管病变组(B组)32例。对照组(C组)30例(男 16例,女14例)为健康体检者,平均年龄(50±8)岁。
1.2 研究方法
1.2.1 生化检测 晨起采集空腹静脉血检测空腹血糖(FBG)、糖化血红蛋白(HbA1c)、hsCRP、血脂等。
1.2.2 大血管病变判断依据 存在下列情况之一者:高血压、冠心病(或缺血性心脏病)、脑血管病及下肢缺血性病变等。A组在服用原降糖药基础上给予口服罗格列酮钠(太极集团涪陵制药厂生产)4mg,疗程8周。8周后重复检测上述指标。A、B组原使用的降脂药、阿司匹林等维持不变。
2 结 果
2.1 各组一般资料及生化指标比较 A组血清hsCRP水平明显高于B、C组,差异均有统计学意义(P<0.01)。B组与C组血清hsCRP水平也有明显差异(P<0.05),见表1。
表1 各组一般资料比较
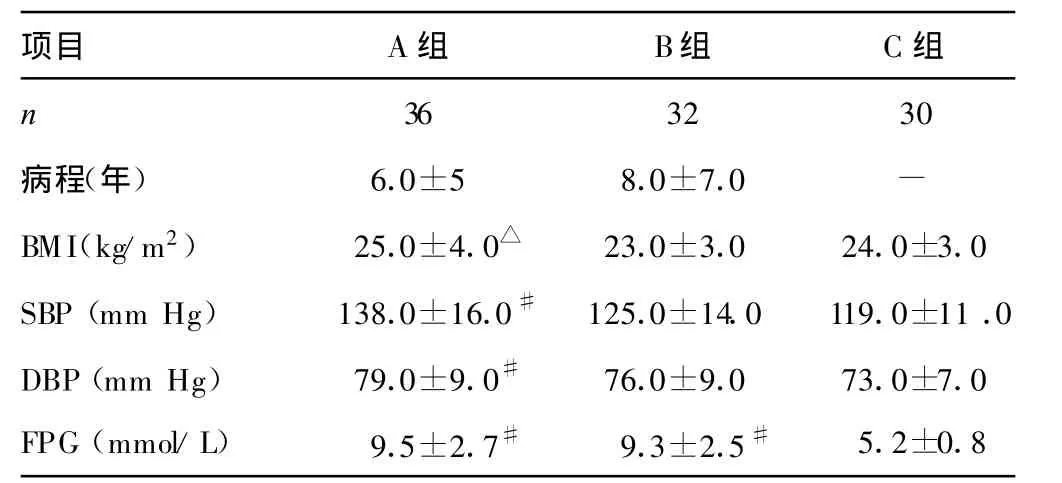
表1 各组一般资料比较
与 C组比较,*:P<0.05,#:P<0.01;与 B组比较,△:P<0.05,☆:P<0.01;-:表示无数据。
项目 A组 B组 C组n 36 32 30病程(年)6.0±5 8.0±7.0 -BMI(kg/m2)25.0±4.0△ 23.0±3.0 24.0±3.0 SBP(mm Hg)138.0±16.0# 125.0±14.0 119.0±11.0 DBP(mm Hg)79.0±9.0# 76.0±9.0 73.0±7.0 FPG(mmol/L)9.5±2.7# 9.3±2.5# 5.2±0.8
续表1 各组一般资料比较

续表1 各组一般资料比较
与C组比较,*:P<0.05,#:P<0.01;与 B组比较,△:P<0.05,☆:P<0.01;-:表示无数据。
项目 A组 B组 C组HbA1c(%)8.1±1.8* 8.0 ±2.1* 6.2±1.7 TG(mmol/L)2.2±1.1# 1.7±1.2* 1.1±0.5 TC(mmol/L)5.2±1.2* 5.0±1.0 4.6±0.8 HDL-C(mmol/L)1.1±0.4# 1.2±0.2 1.4±0.3 LDL-C(mmol/L)3.7±1.7 3.5±1.4 3.1±0.7 hsCRP(mg/L)3.9(2.5~6.7)#☆ 2.7(1.3~ 4.6)*1.9(1.6~3.8)
2.2 A组罗格列酮治疗前后血清hsCRP等指标变化 部分患者出现下肢浮肿,轻度者未予处理,稍重者给予小剂量利尿剂双氢氯噻嗪(25mg/d)治疗,见表2。
表2 A组治疗前后各指标比较
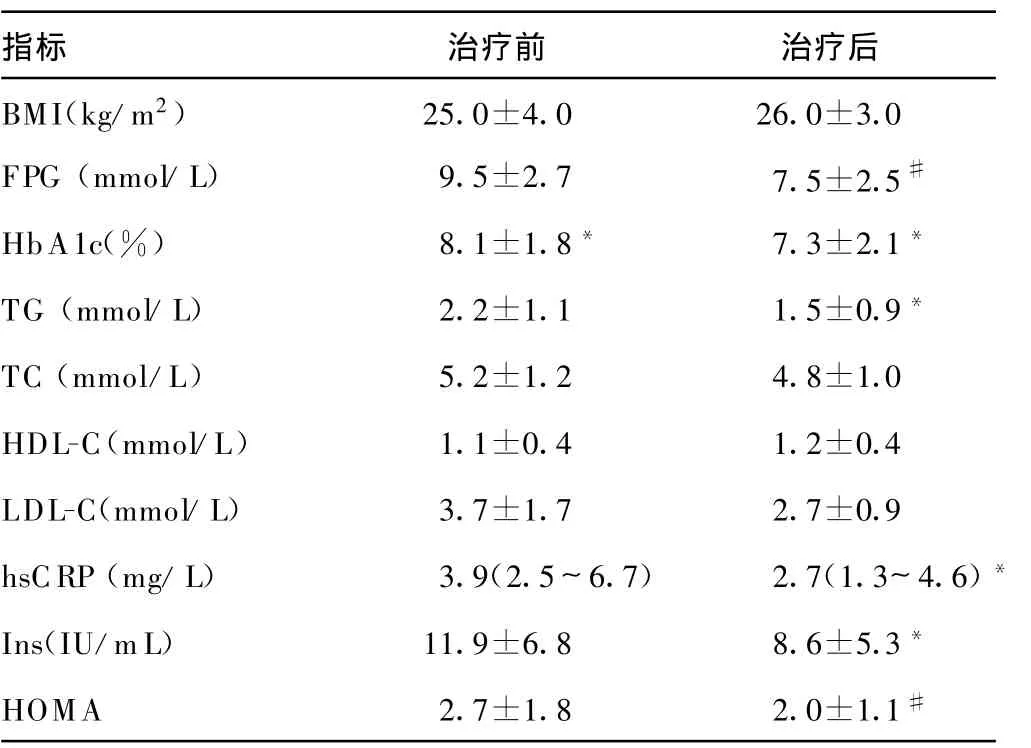
表2 A组治疗前后各指标比较
与治疗前比较,*:P<0.05,#:P<0.01。
指标 治疗前 治疗后BMI(kg/m2)25.0±4.0 26.0±3.0 FPG(mmol/L)9.5±2.7 7.5±2.5#HbA1c(%)8.1±1.8* 7.3±2.1*TG(mmol/L)2.2±1.1 1.5±0.9*TC(mmol/L)5.2±1.2 4.8±1.0 HDL-C(mmol/L)1.1±0.4 1.2±0.4 LDL-C(mmol/L)3.7±1.7 2.7±0.9 hsCRP(mg/L)3.9(2.5~ 6.7)2.7(1.3~ 4.6)*Ins(IU/mL)11.9±6.8 8.6±5.3*HOMA 2.7±1.8 2.0±1.1#
2.3 ΔhsCRP与血脂等指标的关系 分别作ΔhsCRP与BMI、SBP、DBP、FBG、HDL-C、TG、TC、LDL-C 等指标治疗前后差值的多元线性回归分析,未发现ΔhsCRP与上述指标治疗前后变化值有相关性(P>0.05)。
3 讨 论
T2DM大血管病变主要指动脉粥样硬化,涉及血管有主动脉、冠状动脉、脑动脉、肾动脉、髂股动脉等弹性动脉和肌性动脉,临床常见疾病为冠心病、脑卒中和下肢动脉硬化、坏疽等。T2DM合并大血管病变为一般人群的2~4倍。C反应蛋白(CRP)是一种敏感的非特异性炎症标志物,越来越多证据表明,炎症反应参与了动脉硬化的形成[2]。
本研究结果显示,T2DM合并大血管病变者血清hsCRP明显高于无大血管病变者,此结果支持糖尿病大血管发病炎症学说[1]。CRP在T2DM大血管病变中增高的可能机制是胰岛素抵抗时肿瘤坏死因子-α(TNF-α)表达合成增高,作用于肝脏导致CRP增加,并可通过抑制胰岛素受体酪氨酸激酶活性而加重胰岛素抵抗,进一步促进前炎性细胞因子的产生。而且胰岛素抵抗时,TNF-α、IL-1、IL-6等分泌增加,这些因子使平滑肌细胞增生和内皮细胞通透性增加,进一步分泌IL-1和TNF-α作用于肝脏,使CRP增加[3]。
罗格列酮是过氧化物酶体增殖物激活受体-γ(PPAR-γ)激动剂,本品激活 PPA R-γ核受体,可对参与葡萄糖生成、转运和利用的胰岛素反应基因转录进行调控[4]。其抗糖尿病作用是通过提高肝脏、肌肉和脂肪组织对胰岛素敏感性而实现的,并且在脂肪组织中使胰岛素调控的葡萄糖转运因子GLUT-4的基因表达增加[5]。本研究结果显示,罗格列酮同样能降低糖尿病患者CRP水平,并且与其血糖改善无关。说明这一作用机制可能与其降糖之外的作用有关,包括改善内皮细胞功能、减轻内皮细胞损伤、减少炎性细胞、抑制泡沫细胞和平滑肌细胞产生的金属蛋白酶、减轻内膜炎症及稳定斑块等[6]。因此对于糖尿病患者尤其是有大血管病变者,使用罗格列酮类药物对于防止心脑血管并发症具有重要意义。
[1]Dandona P,Aljada A,Chaudhuri A,et al.The potential influence of inflammation and insulin resistance on the pathogenesis and treatmentofatherosclerosis-related complications in type 2 diabetes[J].J Clin Endocrinol Metab,2003,88:2422.
[2]Danesh J,Wheeler JG,Hirschfield GM,et al.C-reactive protein and other circulating markers of inflammation in the prediction of coronary heart disease[J].N Engl J Med,2004,350:1387.
[3]Winkler G,Lakatos P,Salamon F,et al.Elevated serum TNF-levels as a link between endothelial dysfunction and insulin resistance in normotensive obese subjects[J].Diabet Med,1999,16:207.
[4]闫春玲,弓向荣,吴铭辉.罗格列酮治疗2型糖尿病肥胖患者的疗效观察[J].医药论坛杂志,2007,28(4):69.
[5]Haffner SM,Greenberg AS,Weston WM,et al.Effect of rosiglitazone treatment on nontraditional markers of cardiovascular disease in patients with type 2 diabetes mellitus[J].Circulation,2002,106:679.
[6]Ilhan T,Berrin C,Erdem T,et al.Effect of rosiglitazone on insulin resistance,C-reactive protein and endothelial function in on-obese young women with polycystic ovary syndrome[J].European Journal of Endocrinology,2005,153:115.



