赵丽凤 赵明明 马艳玲 苏会霞 周莹君
(河北省石家庄以岭药业股份有限公司,石家庄050035)
通便灵胶囊为番泻叶、当归和肉苁蓉加工制成的胶囊剂。功能与主治:泻热导滞、润肠通便。用于热结便秘,长期卧床便秘,一时性腹胀便秘。采用加速试验和长期试验方法,考察不同批号的样品,测试不同试验条件下样品的外观、性状、鉴别、水分、崩解时限、含量等的变化,获得药品稳定性试验数据。
1 仪器与试药
1.1 仪器 Agilient1200高效液相色谱仪,紫外检测器:G1314B。
1.2 试药 阿魏酸对照品(中国药品生物制品检定所,批号:110773-200611,药品:通便灵胶囊,市售包装(石家庄以岭药业股份有限公司,批号100201、100202、100701、071101、080201、081201,规格:0.25g/粒);甲醇,色谱纯,冰醋酸。
2 方法和结果
2.1 含量测定方法考察
2.1.1 色谱条件 色谱柱:C18,5μm,4.6×150mm;流动相:甲醇-1%的冰醋酸(28:72);检测波长为322nm。理论板数按阿魏酸峰计算应不低于3000。
2.1.2 对照品溶液的制备 精密称取阿魏酸对照品适量,置棕色容量瓶中,加甲醇配制成对照品原液,冰箱保存,临用时加40%的甲醇稀释成每毫升含5微克的溶液,作为对照品溶液。
2.1.3 供试品溶液的制备 取装量差异项下的本品内容物,研细,取约0.6g,精密称定,置具塞三角瓶中,精密加70%甲醇25ml,称定重量,回流提取40min,放凉,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液5ml,置蒸发皿中,水浴浓缩至约1ml,浓缩液用盐酸-水(1:30)溶液25 ml,分次转移至分液漏斗中,蒸发皿再用20 ml乙醚,分次洗涤,洗涤液并入漏斗中,振摇萃取三次,每次20ml,合并乙醚液,于40℃的水浴上,挥至近干,残留物先用甲醇1 ml分次溶解,移至5ml的容量瓶中,再用40%的甲醇洗涤蒸发容器,并入容量瓶中,并至刻度,用微孔滤膜(0.45μm)滤过,滤液作为供试品溶液。
2.1.4 对照品和供试品溶液测定 分别精密吸取对照品溶液与供试品溶液各20μl,注入液相色谱仪,测定,即得。本品每粒含当归以阿魏酸(C10H10O4)计,不得少于0.036 mg。
2.1.5 精密度试验 进样20μl,连续6次,测定峰面积,RSD=0.84%,取同一供试品数份,按含量测定项下方法平行测定,RSD=1.31%(n=6)。
2.1.6 稳定性试验 取供试品溶解,按以上色谱条件测定峰面积,每隔2h进样测定1次,每次进样20μl,共测定6次,结果RSD为1.3%,显示供试品溶液至少在10h内稳定。
2.2 制剂稳定性考察
2.2.1 各项检验项目的标准规定 见表1。

表1 各项检验项目的标准规定
2.2.2 加速稳定性试验 将本品置温度(40±2)℃,相对湿度(75±5)%的条件下放置6个月,根据国家药品标准(试行YBZ05942004)检验。三批加速试验中,外观、性状、鉴别、平均装量均符合规定,水分、崩解时限、含量(mg/粒)定期测定结果如表2。
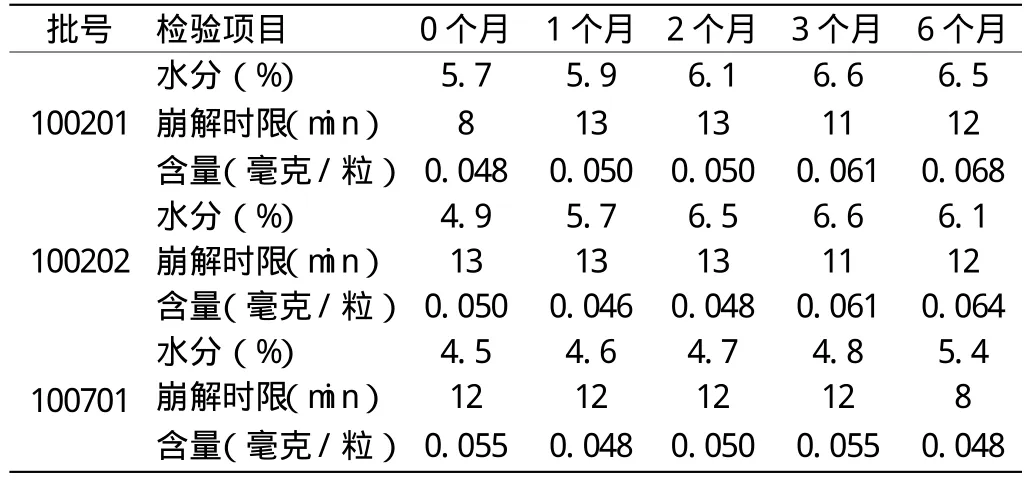
表2 各批号水分、崩解时限、含量定期测定
2.2.3 长期稳定性试验 将本品在市售包装条件下,置温度(25±2)℃,相对湿度(60±10)%的条件下,放置24个月,分别于0个月、3个月、6个月、9个月、12个月、18个月、24个月各取样1次,检测指标、标准规定同上。三批通便灵胶囊长期稳定性试验中,外观、性状、鉴别、平均装量、崩解时限和微生物限度均符合规定,水分和含量测定略有波动,检测结果如下:批号:100201水分为2.6%~4.0%,含量为0.039~0.065毫克/粒;批号:100202 水分为3.5%~5.6%,含量为0.052~0.062毫克/粒;批号:100701 水分为3.9%~4.8%,含量为0.054~0.068毫克/粒。
3 结论
本实验采用加速试验方法对通便灵胶囊的稳定性进行考察,方法可行,采用高效液相色谱法对不同加速试验期间的通便灵胶囊的含量进行测定比较,对其外观、性状、水分、崩解时限进行比较,不同批号的质量存在一定差异,总体看稳定性较好。本品经过24个月试验,其外观、性状、鉴别、水分、崩解时限、含量及微生物限度检查等项目均无明显变化,符合质量标准规定,故认为本品制剂稳定。



