戴万生,赵声兰,张鹏慧,曹冠华,许兆熙,朱智芸
云南中医学院,云南 昆明 650500
滇黄精3种炮制方法的比较研究*
戴万生,赵声兰,张鹏慧,曹冠华,许兆熙,朱智芸
云南中医学院,云南 昆明 650500
目的:优选滇黄精炮制方法。方法:采用紫外分光光度法测定3种不同方法炮制滇黄精品中还原糖、小分子总糖、多糖和总皂苷的含量,并按药典方法测定其浸出物含量,以此综合评判优选。结果:6个指标综合评判Y值为:方法一Y=0.6833,方法二Y=-5.0375,方法三Y=4.2812。结论:滇黄精直接蒸制(法三)优于煮后蒸制(法一和法二)。
滇黄精;炮制方法;综合指标
滇黄精(Polygonatum kingianum CoIL et Hemsl),味甘,性平,归脾、肺、肾经,具有养阴润肺,补脾益气,滋肾填精的功能。通过炮制,可消除黄精的麻味,减轻对咽喉的刺激,增强其补脾润肺益肾的功效。黄精炮制方法较多,历代以来有:九蒸九曝法、蔓荆子水蒸法、酒熬法、焙制法、黑豆煮法、酒蒸法、乳浸晒法等20多种;《中国药典》(2010版)收载的炮制方法为酒蒸法,各省、市、自治区又有自己的炮制规范,方法不统一[1-2]。云南使用的黄精以滇黄精为主,民间应用和地方法规收载的滇黄精炮制方法有3种,但它们在炮制方法和工艺上存在一定的差异,且缺乏客观的技术参数。本实验对云南常用的3种滇黄精的炮制方法进行比较研究,分别测定其水浸出物、乙醇浸出物、小分子总糖、多糖、总皂苷等含量,以此为指标综合评判3种炮制方法的优劣,为滇黄精炮制工艺的规范化奠定基础。
1 材料
1.1 仪器 UV-1800PC紫外可见分光光度计[翱艺仪器 (上海)有限公司提供],CP214电子天平[奥豪斯仪器(上海)有限公司提供],SK3300型超声波清洗器(上海科导超声仪器有限公司提供)。
1.2 试剂 无水葡萄糖(天津市风船化学试剂科技有限公司提供),人参皂苷Rbl(南京都莱生物技术有限公司提供,批号:RSZGB2P20140712),其余试剂均为分析纯。黄精(云南绿生药业有限公司提供),经云南中医学院赵荣华教授鉴定为滇黄精(Polygonatum kingianum Coll.et Hemsl.)的根茎。
2 方法与结果
2.1 样品的炮制及制备
2.1.1 方法一[3]取净黄精片200 g,加水适量浸润过夜,加5%生姜、10%黑豆煮2小时,70℃干燥4小时后,加15%蜂蜜及剩余汁液拌匀,蒸24小时,取出,70℃干燥,粉碎,过40目筛,备用。
2.1.2 方法二[4]取净黄精片200 g,加水适量浸润过夜,加黑豆汁及适量水煮4小时后,70℃干燥4小时,再加5%蜂蜜及5%黄酒拌匀,蒸24小时,取出,70℃干燥,粉碎,过40目筛,备用。
2.1.3 方法三[5]取净黄精片200 g,加黑豆汁及水适量浸润过夜,蒸24小时,取出,加5%黄酒和5%蜂蜜拌匀,吸尽,70℃干燥,粉碎,过40目筛,备用。每100 g黄精片,用黑豆10 g,加水浸泡至透,煎煮4小时,过滤,再加水煎煮3小时,过滤,合并2次滤液,浓缩至25 mL,备用。
2.2 浸出物的含量测定 按《中国药典》2010版一部附录XA项下热浸法,用蒸馏水、稀乙醇作溶剂,测定水溶性浸出、醇溶性浸出物,结果见表1。
2.3 糖类成分的含量测定
2.3.1 葡萄糖对照溶液的配制 取经105℃干燥至恒重的无水葡萄糖对照品55.0 mg,精密称定,置50 mL量瓶中,加水溶解并稀释至刻度,摇匀,即得(每1mL中含无水葡萄糖1.1 mg)。
2.3.2 苯酚溶液的配制[6]精密称取2.5 g苯酚,用蒸馏水溶解并定容于50 mL棕色量瓶中。
2.3.3 D N S溶液的配制[6]称取0.650 g 3,5-二硝基水杨酸(DNS),以50 mL蒸馏水溶解并转移至100 mL棕色量瓶中,加入32.5 mL的2 mol/L的NaOH溶液,再加入4.5 g丙三醇,以蒸馏水定容,即得。
2.3.4 供试品溶液的制备 精密称取黄精粉末1.0 g,置250 mL烧瓶中,加80%乙醇100 mL,水浴回流提取1小时,过滤,滤渣用80%乙醇洗2次(每次约10 mL),合并滤液,挥尽乙醇,转移至250 mL量瓶中,加水至刻度,摇匀后用于还原糖和小分子总糖含量测定。药渣挥干乙醇后,用100 mL水回流提取1小时,过滤,残渣用水洗二次,合并滤液,转移至250 mL量瓶中,加水至刻度,用于总多糖的测定。
2.3.5 还原糖测定标准曲线[6]精密量取1.1mg/mL葡萄糖对照品溶液0.2、0.4、0.6、0.8、1.0、1.2mL,分别置于10 mL具塞刻度试管中,加入蒸馏水至4 mL,再分别加入5 mL的DNS溶液,混匀后置沸水浴中煮沸6分钟,冰水冷却至室温,加水至刻度,以空白管为对照,在540 nm处测定吸光度[6-7]。以吸光度(A)为纵坐标,葡萄糖浓度(μg/mL)为横坐标进行回归处理,得回归方程:Y=0.008 1X+0.000 7(r=0.9995),结果表明无水葡萄糖在22~132 μg/mL范围内具有良好的线性关系,应用DNS法测定还原糖。
2.3.6 总糖、多糖测定标准曲线[7]精密量取1.1 mg/mL的葡萄糖对照品溶液1.0、2.0、3.0、4.0、5.0、6.0 mL,分别置于50 mL量瓶中,加水至刻度,然后分别量取上述稀释后的不同浓度的葡萄糖对照品溶液1 mL于10 mL具塞刻度试管中,加入蒸馏水至2 mL,混匀,再加入1 mL的5%苯酚溶液和7 mL的浓硫酸溶液,摇匀,静置5分钟,水浴加热20分钟,冰水冷却至室温,以空白管为对照,在490 nm测定吸光度。以吸光度(A)为纵坐标,葡萄糖浓度(μg/mL)为横坐标进行回归处理,得回归方程:Y=0.0594X-0.0554(r=0.999 5),结果表明无水葡萄糖在2.2~13.2 μg/mL范围内具有良好的线性关系,用于苯酚-硫酸法测定总糖、多糖。
2.3.7 样品的测定 取滇黄精炮制品,按“2.3.4”项下方法制成供试品溶液,分别精密量取供试液1.0 mL稀释到50 mL,精密量取4 mL,按照标准曲线项下的方法自“再分别加入5 mL的DNS溶液”起操作,测定吸光度,计算还原糖含量,结果见表1。
取滇黄精炮制品,按“2.3.4”项下方法制成供试品溶液,分别精密量取供试液1.0 mL稀释到50 mL,精密量取1 mL,按照标准曲线项下的方法自“加入蒸馏水至2 mL”起,测定吸光度,计算小分子总糖含量。取滇黄精炮制品,按“2.3.4”项下方法制成供试品溶液,分别精密量取供试液0.5 mL,按照标准曲线项下的方法自“加入蒸馏水至2 mL”起操作,测定吸光度,计算多糖含量。结果见表1。
2.4 总皂苷含量测定
2.4.1 标准曲线制备[8]称取人参皂苷Rbl标准品11.3 mg于小烧杯中,加甲醇溶解并定容至10 mL,作为标准液。吸取该标准液40、80、120、160、200 μL,置于具塞刻度试管中,挥尽溶剂,加入0.2 mL5%香草醛-冰醋酸溶液(新鲜),冰浴时加入0.8 mL高氯酸,摇匀,60℃水浴加热15分钟后,冰浴2分钟,加入5 mL冰醋酸,摇匀,静置5分钟,于550 nm处测定吸光值(A)[8]。以吸光度(A)为纵坐标,人参皂苷Rbl的质量(μg)为横坐标进行回归处理,得回归方程:Y=0.003 6 X+0.002 4 (r=0.999 2),结果表明人参皂苷Rbl在45.2~226 μg范围内具有良好的线性关系。
2.4.2 供试品溶液制备 称取干燥黄精炮制品粉末1.00 g,加入14倍量水饱和正丁醇,40℃超声提取50分钟,提取2次,合并滤液至25 mL量瓶中,加水饱和正丁醇定容,摇匀,备用[9]。
2.4.3 样品测定 吸取供试液100 μL,挥干溶剂,按“2.4.1”项显色,于550 nm波长处测定吸光度,计算总皂苷含量(%),结果见表1。
2.5 数据处理[10]将测得数值按公式:Xi,j=(Xi,j-/Sj进行标准化处理,Xi,j为供试液i中成分j的含量,为供试液i中成分j的平均值,Sj为成分j的标准偏差,即为标准化后的值,根据各指标成分在药物中的药理活性和特性,给予不同的加权系数,以标准化后的值Xi,j加权求和后,即得综合评价指标Y值。其关系式:Y=(还原糖+小分子总糖+多糖)/3×5+总皂苷×3+ (水浸出物+乙醇浸出物)/2×2。综合评判结果见表1。
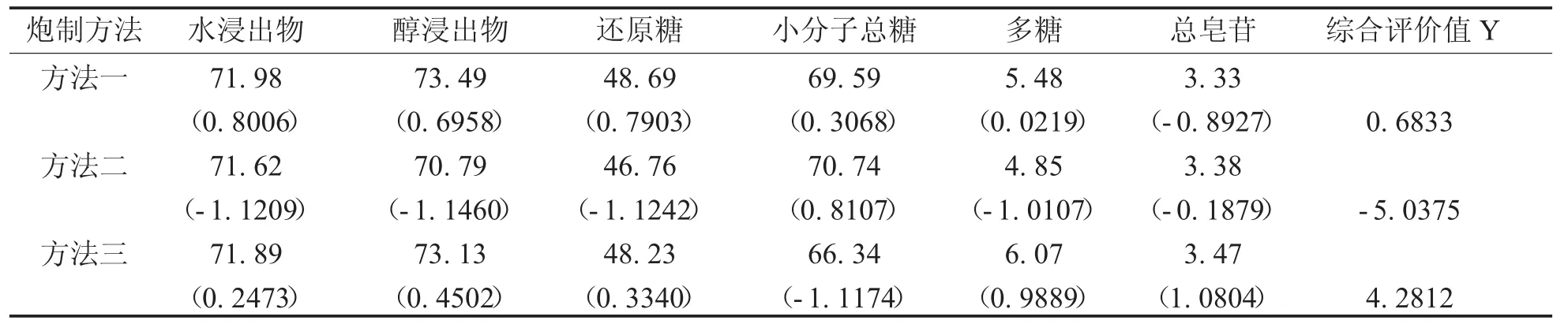
表1 3种不同工艺滇黄精炮制品中各指标成分含量及标准化结果比较(n=3)%
3 讨论
黄精主要含有多糖、甾体皂苷、黄酮、蒽醌类化合物、氨基酸等活性成分,黄精多糖具有增强免疫、降血脂血糖、抗肿瘤、抗病毒、抗衰老等作用;黄精总皂苷具有调节血糖、抗肿瘤、改善记忆力、抗氧化等作用。黄精炮制后增益作用强补,可能与多糖、甾体皂苷的量变和质变有关,故参考药理作用给予各类成分加权系数:糖类5,总皂苷3,浸出物2。
从工艺看3种滇黄精炮制方法主要差异在于现行《云南省中药饮片标准》(2005版)方法为蒸法,民间习用和《云南省中药饮片炮制规范》(86版)方法为先煮2小时和4小时后再蒸法,结果表明,蒸法制品的综合评判Y值高于另外2种先煮后蒸制品,说明先煮制会导致部分有效成分的损失,滇黄精炮制宜直接蒸制。
从辅料上看3种方法都用黑豆和蜂蜜,差别是法规上用酒代替民间用的生姜,黄精味甘,生姜和酒均属辛温之品与黄精合制可起到辛甘化阳,缓和黄精滋腻之性,但酒善入走血分,能行血脉、通经络,生姜偏于温中止呕、解毒,从中医理论讲用生姜与黄精同制更能增强其补脾的作用。2者对滇黄精药性、化学成分和药效的影响有待进一步的研究。
[1] 钟凌云,龚千锋,张的凤,等.黄精炮制研究现状分析[J].中药材,2007,30(12):1618-1621.
[2] 吴建华,张涓,崔於.黄精炮制工艺的研究进展[J].川北医学院学报,2013,28(1):27-29.
[3] 中医研究院中药研究所、北京药品生物制品检定所.中药炮制经验集成[M].北京:人民卫生出版社,1963:113-114.
[4] 云南省卫生厅.云南省中药饮片炮制规范[M].昆明:云南科学技术出版社,1986:111-112.
[5] 云南省食品药品监督管理局.云南省中药饮片标准[M].昆明:云南科学技术出版社,2005:75.
[6] 张志君,孙伟,李永亮,等.3,5-二硝基水杨酸法联合苯酚-浓硫酸法测定不同产地黄精中多糖含量[J].中国实验方剂学杂志,2012,18(6):106-109.
[7] 蓝松.苯酚-硫酸法测定黄精多糖含量研究[J].广东化工,2013,40(18):132-133.
[8] 尤新军,郭蕊,王琳,等.黄精总皂苷超声提取工艺研究[J].西北林学院学报,2010,25(3):163-166.
[9] 秦枫,刘靖,陈玉勇,等.三七总皂苷含量测定方法及超声提取工艺研究[J].安徽农业科学,2008,36(8):3062-3063.
[10]孙秀梅,栾妮娜,张兆旺.黄精饮片3种蒸制工艺的比较[J].山东中医药大学学报,2010,34(6):542-543.
Comparative Study on Three Processing methods of DianHuangJing
DAI Wansheng,ZHAO Shenglan,ZHANG Penghui,CAO Guanhua,XU Zhaoxi,ZHU Zhiyun
Yunnan University of Traditional Chinese Medicine,Kunming 650500,China
Objective:To optimize the processing method of DianHuangJing(Polygonatum Kingianum). Methods:Ultraviolet spectrophotometric method was used to determine the contents of reducing sugar,small molecule total sugar,polysaccharide and total saponins in DianHuangJing with three different processing methods.Contents of extract from DianHuangJing were determined based on pharmacopoeia method to realize its synthetical judge and priority selection.Results:Y values of the synthetical judge from six indexes were Method one:Y=0.6833,Method two:Y=-5.0375,Method three:Y=4.2812.Conclusion:Method of direct steaming of DianHuangJing(Method three)is superior to method of steaming after cooking(Method one and Method two).
DianHuangJing;processing method;comprehensive index
R283
A
1004-6852(2016)08-0032-03
2016-02-15
云南中医学院重点学科资助项目(编号X K 201325)。
戴万生(1967—),男,硕士学位,教授。研究方向:中药炮制及功能食品研发。



