许楠 刘新杰 刘春红 张鹏彦 周冬仙 张桂英
继发性甲状旁腺功能亢进症(Secondary hyperparathyroidism,SHPT)是肾功能衰竭的常见并发症,近年来其发病率呈逐年增加的趋势。治疗方法主要包括内科药物治疗及手术治疗。药物治疗主要为骨化三醇冲击疗法,但易复发[1]。外科手术则是治疗SHPT最有效的方式,术式包括甲状旁腺全切、次全切除术等[2]。如何准确地进行甲状旁腺的定位是该类手术成功的关键所在,对于旁腺的术前定位B超及核素扫描起到一定作用同时具有其局限性,而目前旁腺的术中定位缺乏行之有效的方法,尤其对于一些体积较小的、被脂肪组织包绕的、植入于甲状腺真被膜下的以及异位的增生旁腺。本院从2014年1-12月,采用术中静脉注射亚甲蓝(Methylene blue infusion,MBI)结合术前B超、核素扫描定位诊断和术中甲状旁腺激素快速测定(Intraoperative parathyroid hormone,IOPTH)治疗25例SHPT患者,取得良好效果,现报告如下。
1 资料与方法
1.1 一般资料 选取2014年1-12月共25例在本院行手术治疗的SHPT患者,其中男16例,女9例,年龄29~65岁,平均(42.14±10.56)岁。25例均行血液透析,透析时间12~150个月,平均(54.15±36.76)个月,临床表现骨疼痛、乏力、皮肤瘙痒、软组织钙化、骨质疏松等。
1.2 术前检查 实验室检查:25例SHPT术前PTH 560~5000 pg/mL, 平 均(2016.84±1124.50)pg/mL, 血 钙1.88~2.80 mmol/L,平均(2.39±0.21)mmol/L,血磷 1.02~4.28 mmol/L, 平 均(2.61±0.59)mmol/L, 尿 素 氮 8.1~44.03 mmol/L,平均(21.70±7.7)mmol/L,肌酐243~1735 μmol/L,平均(1016.72±318.36)μmol/L。
影像学检查:25例均行高频超声甲状旁腺检查,发现旁腺肿物影4例有1个、7例有2个、6例有3个、3例有4个、5例阴性,检出率80%,肿物阴影最大直径约3.2 cm。25例均行ECT定位检查,显示甲状旁腺功能亢进12例,其中8例显示1个旁腺亢进,4例显示2个,检出率48%。
1.3 手术指征 适应证:(1)血甲状旁腺激素(intact parathyroid hormone,iPTH)水平长期>500 pg/mL,伴有钙磷代谢明显紊乱者;(2)有明显骨痛皮肤瘙痒血管钙化等临床症状者;(3)内科冲击治疗失败者。手术禁忌证:(1)心肺功能不能耐受全麻者;(2)严重贫血或严重出凝血功能异常者;(3)接受精神类药物治疗者。
1.4 治疗方式及手术方法 亚甲蓝染色定位:手术前配制亚甲蓝溶液(5%葡萄糖注射液500 mL中按5 mg/kg加入1%亚甲蓝),麻醉前30 min由外周静脉快速滴注,全组患者均进行静脉注射亚甲蓝染色定位。
本组病例均采用甲状旁腺全切加前臂自体移植术式,由同组医生完成,均在全麻气管插管下行双侧颈部探查,术中精细化操作,注意蓝染旁腺位置及程度。明确甲状旁腺部位后行甲状旁腺全切,切除顺序自下而上、由大至小进行,术中常规行冰冻切片病理检查证实所切除组织是否为甲状旁腺。切取非结节状增生改变旁腺的一部分(约30 mg),切成组织屑,移植于前臂皮下。
1.5 术后处理 术后按甲状腺外科护理常规观察护理。术后第1天查PTH、电解质。术后静脉补充钙剂,具体以0.9%氯化钠溶液100 mL配10%葡萄糖酸钙40~60 mL(速度为1~2 mg元素钙/kg·h)静滴,待胃肠道功能恢复后改用口服钙尔奇(碳酸钙D3片,含钙剂约1.2~2.4 g/d),同时加用罗盖全(骨化三醇胶丸0.25~0.5 μg/d)。期间患者如有肢体、面部麻木等症状及时复查电解质了解血钙水平,增加补钙剂量,最多静脉补钙16 g/d。同时注意保护血管,预防静脉炎。定期监测血钙,综合运用高钙透析、静脉结合口服补钙、口服骨化三醇等治疗方法,待稳定在2.2 mmol/L后逐渐减静脉补钙量,渐过渡到以口服为主的补钙方式,术后1周内以无肝素透析为主。
1.6 统计学处理 采用SPSS 19.0进行统计分析,计量资料采用(x-±s)表示,比较采用t检验,以P<0.05为差异有统计学意义。
2 结果
术中精细化操作,借助亚甲蓝染色对比探查并明确甲状旁腺部位,该组病例甲状旁腺多数位于甲状腺侧叶后缘上中三分之一交界处,下甲状旁腺均位于甲状腺下极下缘。25例患者经手术切除甲状旁腺总数为101枚,24例发现4枚增生旁腺,1例患者存在5枚增生旁腺,其中1枚为上纵隔异位旁腺。病理均证实为甲状旁腺增生,旁腺形态多为椭圆形,部分呈结节状改变。旁腺大小0.8~3.6 cm,平均(2.42±1.10)cm。剔除1例异位旁腺患者后,蓝染旁腺比例95.8%(92/96),其中87.5%(21/24)为4枚均染色,8.3%(2/24)2例患者为3枚旁腺染色,4.2%(1/24)为2枚染色。术中观察增生旁腺染色程度表现为深蓝色及浅蓝色,其中染深蓝色比例为80.4%(74/92);增生旁腺染色状态可见全染色及部分染色,其中部分染色比例为39.1%(36/92)。24例手术时间为35.0~52.0 min,平均(43.0±5.2)min。术前静滴亚甲蓝10~15 min后,92.0%(23/25)的患者出现不同程度的末梢血氧饱和度(SpO2)监测值降低,波动范围约75%~85%,亚甲蓝静滴结束后SpO2均恢复至正常水平。术后无1例患者出现明显定向障碍、反应迟钝、意识错乱等症状,未见患者有明显皮肤、巩膜等蓝染情况。
术后患者关节疼痛、乏力、皮肤瘙痒得到明显改善,随访至术后6个月时上述症状缓解率分别为92.0%(23/25)、84.0%(21/25)、76.0%(19/25),25例患者经术后静脉及口服补钙治疗,均未发生严重低血钙症状。术后PTH显着降低,术后血钙、血磷水平逐渐降低,随访至术后6个月,术前术后比较差异有统计学意义,见表1(剔除1例存在5枚增生旁腺患者)。
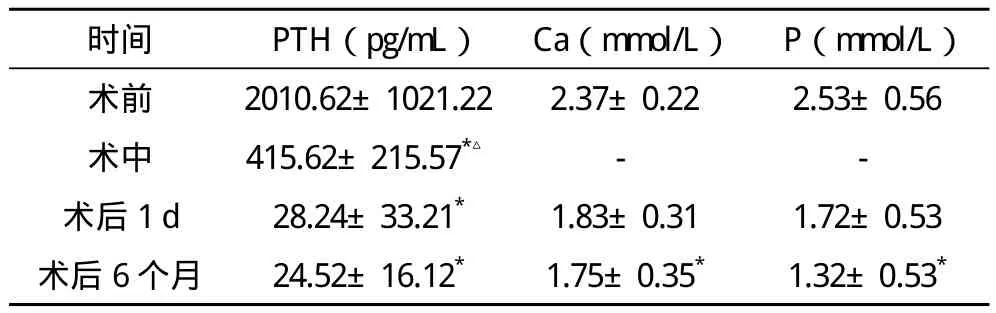
表1 24例患者手术前后血PTH、Ca、P浓度变化比较(x-±s)
3 讨论
亚甲蓝是一种安全有效的染色剂,在乳腺癌前哨淋巴结活检术中应用广泛[3]。1971年Dudley[4]首次报道术前静脉滴注亚甲蓝成功用于定位甲状旁腺,并且未发现明显副反应,亚甲蓝的作用及安全性逐渐得到国内外学者的认可,越来越多的个案报道展示亚甲蓝静脉注射在原发性甲状旁腺切除术中定位旁腺的作用,但目前静脉注射亚甲蓝在继发性甲状旁腺功能亢进手术中的应用却鲜有报道[5-6]。本文回顾性分析了25例应用静脉注射亚甲蓝作为指示剂进行手术治疗的SHPT患者,利用亚甲蓝对于甲状旁腺的正显影功能其进行定位,手术治疗后疗效明显,疗效确切,与笔者前期研究结果相似[7]。
本组继发性甲状旁腺功能亢进患者甲状旁腺染色率为95.8%,明显高于术前彩超及核素扫描对甲状旁腺的检出率,接近于国外报道等应用亚甲蓝对原发性甲状旁腺功能亢进增生旁腺的染色率97%~100%[6-8]。高于Bewick等[9]报道的78.6%染色率,可能因后者应用亚甲蓝浓度3.5 mg/kg低于前两者有关。本组中36枚出现增生旁腺部分蓝染,该类旁腺外观多呈结节状增生,旁腺内部不均匀增生,可能是造成亚甲蓝分布不均现象的原因。18枚旁腺呈现浅蓝色,多为上旁腺,除位置因素外,静脉输注亚甲蓝的速度及时间也是造成其浅染色的原因[10]。本组中共有4枚增生旁腺未染色,均为上旁腺,分析原因为上旁腺多位于甲状腺上极背侧,该处组织间隙较甲状腺下极小,受甲状腺腺体压迫明显,致使上极旁腺血供相对减弱,进而影响亚甲蓝的摄入。
文献[11]报道亚甲蓝用于甲状腺旁腺染色的经典剂量为7.5 mg/kg,也有学者认为5 mg/kg也可达到效果。UK英国国家毒物信息服务(UK National Poison Information Service)则推荐应用剂量为4 mg/kg以下,主要考虑到亚甲蓝可能存在的毒副作用[12]。国外有个案报道称亚甲蓝可能引发5-羟色胺综合征,表现为定向障碍、反应迟钝、意识错乱等,但Shopes等[5]回顾文献发现应用亚甲蓝后出现该类毒副作用的患者多数正在接受精神类药物治疗,原因是由于亚甲蓝的化学构造和酚噻嗪类药物的三环支架结构类似,可能与5-羟色胺能类药物发生交互作用。因此FDA建议避免将亚甲蓝与5-羟色胺能类药物合用。另外,Schirmer等[13]报道亚甲蓝用量超过7 mg/kg,可出现明显胃肠道副作用。本组25例患者仅1例出现术后眩晕症状,术后3 d自行缓解,未出现明显胃肠道副作用病例。本组病例均在麻醉插管前30 min开始滴注亚甲蓝,观察在患者清醒状态下有无头晕、目眩、发热等症状,有助于提前预测和避免严重副反应的发生。为避免可能增加的药物毒性风险,本组患者治疗均采用5 mg/kg,术前30 min静脉滴注,旁腺染色率高,且未见明显眩晕、发热等不良反应。Robert等[14]报道120例亚甲蓝静脉注射病例,亦未见明显副作用发生。另外,本组患者术后第2天均行常规血透,血透可加快血液中亚甲蓝的清除,也是发生副作用的原因之一。
亚甲蓝应用于纵隔内异位旁腺探查术时,利于异位旁腺的快速定位,减少周围组织损伤以及缩短手术时间。本组中1例患者术前核素扫描未提示异位旁腺,PTH为2702.0 pg/mL,术中切除4枚增生旁腺后10 min复查IOPTH为1399.0 pg/mL,因PTH未降至目标水平,再次仔细探查双侧甲状腺背侧,未见蓝染组织,考虑存在非甲状腺区异位的额外旁腺可能,因此未行进一步手术。术后复查核素扫描,见胸骨后旁腺增生影像,遂行胸骨切开异位旁腺探查术,因核素扫描及CT均未能准确定位异位旁腺位置,术前仍静脉注射亚甲蓝,术中探查于上纵隔左头臂静脉后方,左颈总动脉与头臂干夹角处见一蓝染肿物,仔细分离见该肿物椭圆形,包膜完整,部分蓝染,冰冻病理证实为增生的甲状旁腺,切除后10 min PTH降至317.0 pg/mL,术后第1天复测PTH降至13.19 pg/mL。Adachi等[15]也曾报道在静脉亚甲蓝静脉定位的帮助下完成了胸腔镜下纵隔异位甲状旁腺切除术,并指出亚甲蓝定位效果确切,可减小术中损伤,缩短手术时间。
综上所述,静脉注射亚甲蓝是继发性甲状旁腺功能亢进手术中快速定位增生旁腺的一种安全、有效且经济的方法,同时对于异位旁腺手术探查及切除也有较好的定位指引作用,值得临床广泛推广应用。另外其他的旁腺定位方法,例如甲状腺下静脉注射小剂量亚甲蓝染色以及纳米炭负显影功能对甲状旁腺定位的效果和作用有待于进一步探讨。
[1]杨琦,邹晓春,郭宏国.骨化三醇治疗慢性肾衰继发甲状旁腺功能亢进症42例的临床体会[J].中国医学创新,2010,7(1):44.
[2]张凌,闫彩芸.难治性继发性甲状旁腺功能亢进症治疗时机选择[J].中国实用内科杂志,2013,33(2):131-133.
[3]吴耀忠,黄天斌,黄超.亚甲蓝染色在乳腺癌前哨淋巴结清扫术中的应用[J].中国医学创新,2010,7(4):52-53.
[4] Dudley N E.Methylene blue for rapid identification of the parathyroids[J].Br Med J,1971,18,3(5776):680-681.
[5] Shopes E,Gerard W,Baughman J.Methylene blue encephalopathy: a case report and review of published cases[J].AANA J,2013,81(3):215-221.
[6] Patel H P,Chadwick D R,Harrison B J,et al.Systematic review of intravenous methylene blue in parathyroid surgery[J].Br J Surg,2012,99(10):1345-1351.
[7]许楠,刘新杰,周冬仙,等.甲状旁腺全切术治疗继发性甲状旁腺功能亢进症35例[J].暨南大学学报(自然科学与医学版),2014,35(2):182-185.
[8] Kuriloff D B,Sanborn K V.Rapid intraoperative localization of parathyroid glands utilizing methylene blue infusion[J].Otolaryngol Head Neck Surg,2004,131(5):616-622.
[9] Bewick J, Pfleiderer A.The value and role of low dose methylene blue in the surgical management of hyperparathyroidismc[J].Ann R Coll Surg Engl,2014,96(7):526-529.
[10] Traynor S,Adams J R,Andersen P,et al.Appropriate timing and velocity of infusion for the selective staining of parathyroid glands by intravenous methylene blue[J].Am J Surg,1998,176(1):15-17.
[11] Khan M A,North A P,Chadwick D R.Prolonged postoperative altered mental status after methylene blue infusion during parathyroidectomy: a case report and review of the literature[J].Ann R Coll Surg Engl,2007,89(2):W9-11.
[12] Martindale S J,Stedeford J C.Neurological sequelae following methylene blue injection for parathyroidectomy[J].Anaesthesia,2003,58(10):1041-1042.
[13] Schirmer R H,Adler H,Pickhardt M,et al.“Lest we forget you—methylene blue…”[J].Neurobiol Aging,2011,32(12): 2325.e7-16.
[14] Robert J,Delay D,Buhler L,et al.Methylene blue in surgery for primary hyperparathyroidism[J].Ann Endocrinol (Paris),1998,59(1):23-26.
[15] Adachi Y,Nakamura H,Taniguchi Y,et al.Thoracoscopic resection with intraoperative use of methylene blue to localize mediastinal parathyroid adenomas[J].Gen Thorac Cardiovasc Surg,2012,60(3):168-170.



