刘娟弟,何菊仙,春 芽
1.西北妇女儿童医院妇三科,陕西西安 710061;2.陕西省宝鸡市中医医院妇科,陕西宝鸡 721000
卵巢癌发病率及病死率分别列全球女性恶性肿瘤第7、8位[1]。相关研究表明,2020年美国卵巢癌患者新增21 750例,死亡病例达13 940例[2]。卵巢癌早期无典型症状,解剖位置较深,缺乏有效筛查手段,患者首诊多已至中晚期,行肿瘤细胞减灭术辅助铂类药物化疗为主流治疗方案,在一定程度上可缓解临床症状,但3年内复发率达70%左右,多表现为对铂类药物敏感或耐药[3]。为降低复发率,现今研究侧重于分子基因组学基础下的靶向治疗策略,近年研制的贝伐珠单抗(抗血管生成药物)及奥拉帕尼[聚腺苷二磷酸核糖聚合酶(PARP)抑制剂]分别通过了贝伐珠单抗卵巢癌(AURELIA)随机Ⅲ期试验、NCT00753545随机Ⅱ期试验[4-5],并获美国食品药品监督管理局批准用于治疗复发性晚期卵巢癌[6],使卵巢癌治疗模式有了新转变,并且由《卵巢癌靶向治疗的规范化》[7]指南意见为靶向治疗规范化提供了重要循证依据。基于目前临床试验以单独靶向治疗为主,疗效稍有不足,采用双靶向乃至多靶向药物治疗为现今研究的热点,但相关研究较少,疗效及安全性尚有待进一步验证。本研究旨在探讨奥拉帕尼联合贝伐珠单抗治疗对复发性铂类敏感卵巢癌患者疗效及生存预后的影响,现报道如下。
1 资料与方法
1.1一般资料 选取2019年6月至2020年6月西北妇女儿童医院收治的76例复发性铂类敏感卵巢癌患者作为研究对象,按照随机数字表法分为对照组和观察组,每组各38例。对照组年龄32~78岁,平均(52.45±8.15)岁;病理类型:浆液型18例,黏液型12例,透明型7例,混合型1例;复发时间6个月至2年,平均(10.25±3.12)个月;复发部位:盆腔19例,腹腔8例,腹盆腔11例。观察组年龄31~76岁,平均(51.79±7.98)岁;病理类型:浆液型19例,黏液型13例,透明型6例,混合型0例;复发时间6个月至2年,平均(10.64±3.03)个月;复发部位:盆腔21例,腹腔7例,腹盆腔10例。两组患者年龄、病理类型、复发时间、复发部位等一般资料比较,差异均无统计学意义(P>0.05),具有可比性。所有研究对象均知情同意并签署知情同意书。本研究通过西北妇女儿童医院伦理委员会审查批准。
1.2纳入和排除标准
1.2.1纳入标准 (1)符合《卵巢癌诊疗规范(2018年版)》[8]的相关标准;(2)经铂类化疗治疗完全缓解(CR)后≥6个月复发,为复发性铂类敏感类型;(3)年龄30~80岁,卡式功能状态量表评分≥70分,预测生存期≥6个月。
1.2.2排除标准 (1)伴其他恶性肿瘤;(2)存在靶向药物过敏史;(3)肝肾功能重度异常;(4)妊娠期女性;(5)精神及认知功能障碍;(6)临床资料不全。
1.3方法 对照组行卡铂/多柔比星脂质体化疗治疗,即入院后第1天行30 mg/m2多柔比星脂质体(批准文号:H20130186,厂商:Actavis Italy S.p.A)及50 mg/m2卡铂(国药准字:H20059009,厂商:山东鲁抗辰欣药业有限公司)静脉滴注,每3周一次。观察组在对照组的基础上行奥拉帕尼联合贝伐珠单抗治疗,先使用7.5~15.0 mg/kg贝伐珠单抗(国药准字:S20190040,厂商:齐鲁制药有限公司)静脉滴注,每3周一次,再行200 mg奥拉帕尼(批准文号:H20180049,厂商:AstraZeneca)口服,每3周一次,共治疗6个周期。两组患者治疗前后均行对症治疗预防不良反应,诸如胃黏膜保护、水电解质平衡维持、保肝、抗过敏等。按时复查,采用CT或MRI等影像学检查评估病灶情况。
1.4疗效标准 参照2009年实体瘤疗效评价标准[9]分为CR(病灶完全消失4周及以上)、部分缓解(PR,病灶体积较基线缩小>50%,时间≥4周)、疾病稳定(SD,病灶体积较基线缩小25%~50%,时间≥4周)及疾病进展(PD,不符合以上标准)。计算客观缓解率(ORR)及疾病控制率(DCR)。ORR=(CR例数+PR例数)/总例数×100%;DCR=(CR例数+PR例数+SD例数)/总例数×100%。
1.5观察指标 观察两组患者血清肿瘤标志物水平、不良反应及生存预后。(1)血清肿瘤标志物:包括血清人附睾蛋白(HE4)、糖类抗原125(CA125)和循环肿瘤细胞(CTC),HE4、CA125水平采用酶联免疫吸附试验检测,CTC水平采用免疫磁珠及免疫荧光法检测;(2)不良反应:包括胃肠反应、肾脏毒性、血液损伤、骨髓抑制等,并参考美国国立癌症研究通用毒性标准[10]进行分度;(3)生存预后:随访截至2022年1月,记录无进展生存期(PFS)、总生存期(OS)。
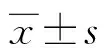
2 结 果
2.1两组患者近期临床疗效比较 观察组患者ORR、DCR分别为52.63%、84.21%,均高于对照组的28.95%、55.26%,差异均有统计学意义(χ2=0.400、7.544,P=0.026、0.006),见表1。
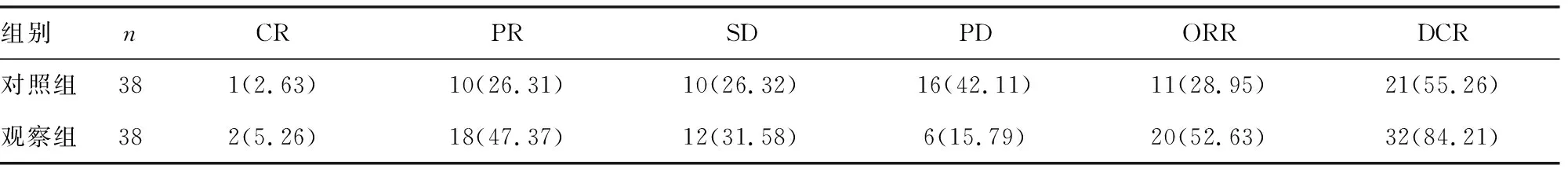
表1 两组患者近期临床疗效比较[n(%)]
2.2两组患者血清肿瘤标志物水平比较 两组患者治疗前HE4、CA125及CTC水平比较,差异均无统计学意义(P>0.05);两组患者治疗后HE4、CA125及CTC水平均降低,且观察组低于对照组,差异均有统计学意义(P<0.05)。见表2。
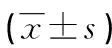
表2 两组患者血清肿瘤标志物水平比较
2.3两组患者不良反应比较 两组患者Ⅲ+Ⅳ级不良反应发生率比较,差异均无统计学意义(P>0.05)。观察组和对照组患者Ⅰ+Ⅱ级不良反应中,肾脏毒性、血液损伤发生率比较,差异均无统计学意义(P>0.05);观察组患者胃肠反应及骨髓抑制发生率均低于对照组,差异均有统计学意义(P<0.05)。见表3。
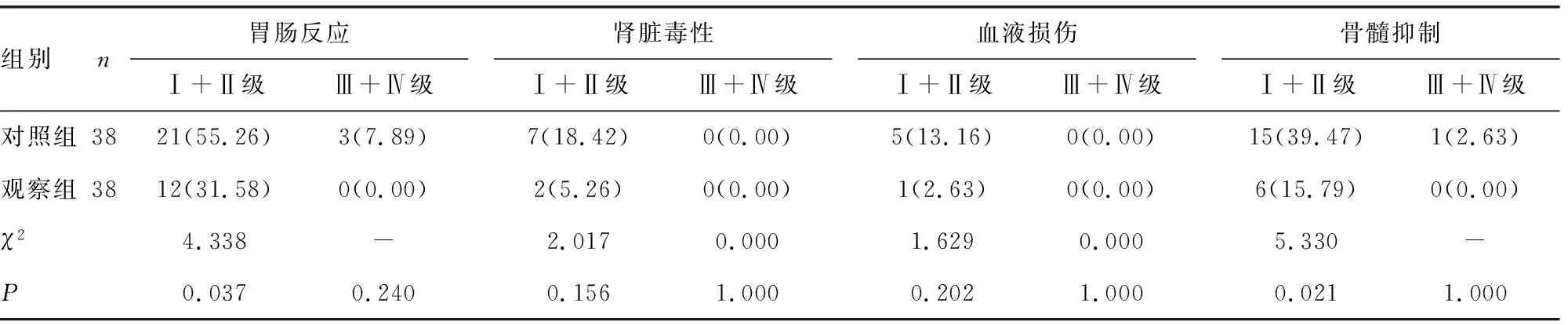
表3 两组患者不良反应比较[n(%)]
2.4两组患者随访生存预后比较 随访截至2022年1月,观察组患者PFS 2.0~16.0个月,中位PFS 8.1个月,OS 2.0~18.0个月,中位OS 10.3个月;对照组患者PFS 2.0~10.0个月,中位PFS 5.3个月,OS 2.0~12.0个月,中位OS 7.0个月。Kaplan-Meier生存曲线结果显示,观察组患者PFS、OS均高于对照组,差异均有统计学意义(Log-Rankχ2=9.265,P<0.05;Log-Rankχ2=9.926,P<0.05)。见图1、图2。
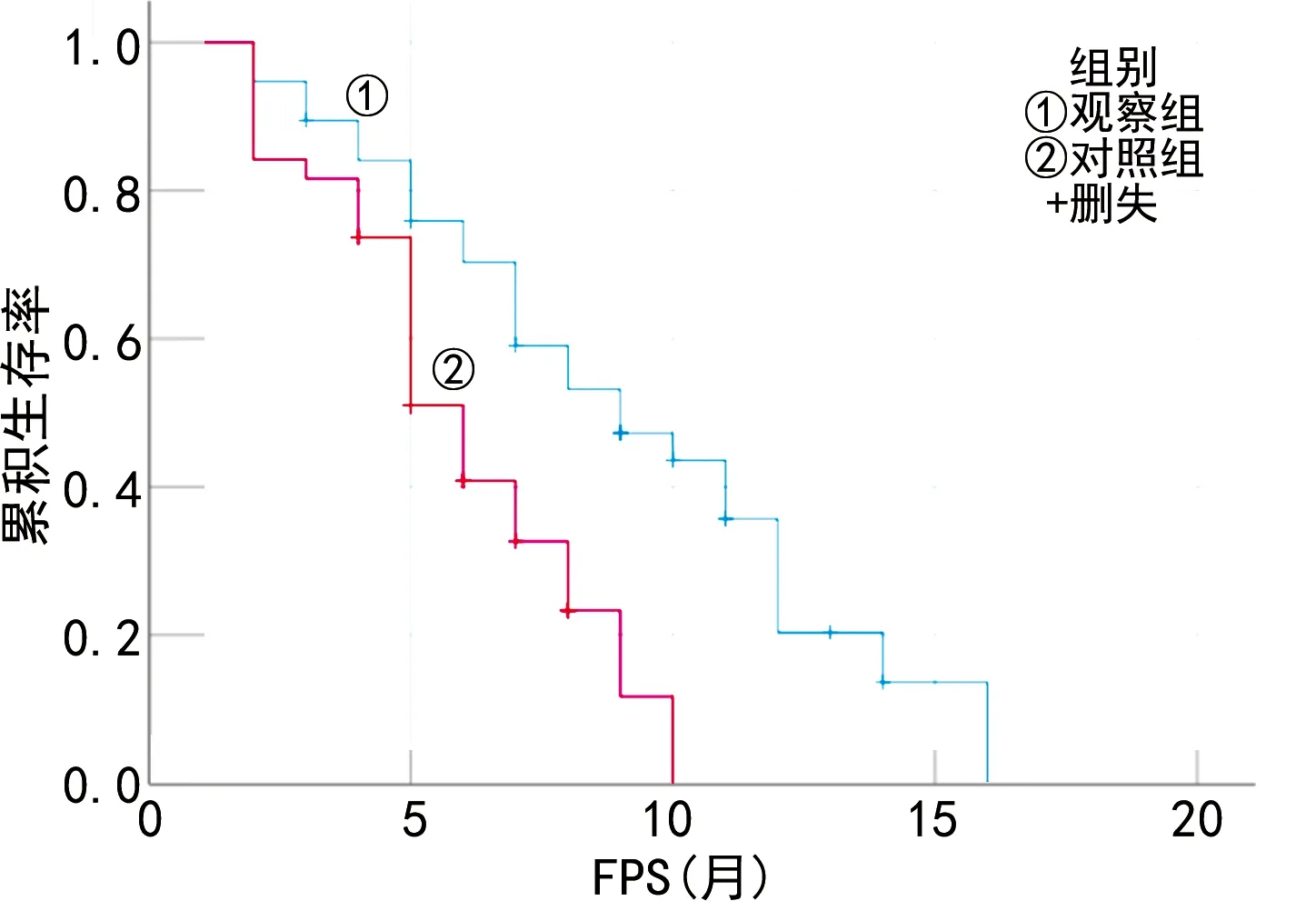
图1 两组患者FPS生存曲线
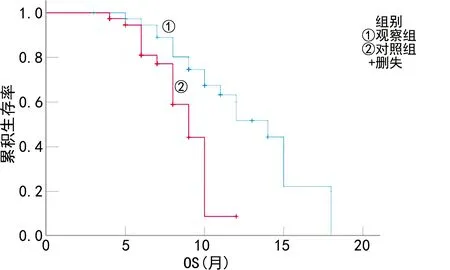
图2 两组患者OS生存曲线
3 讨 论
卵巢癌患者应用手术辅助铂类药物标准化方案治疗后,多数患者对化疗药物耐药导致疾病复发,而耐药机制与血管内皮生长因子(VEGF)信号通路、碱基切除修复信号通路等密切相关。故精准靶向上述耐药通路行个体化治疗可使广大卵巢癌患者获益。作为抗血管生成药物的贝伐珠单抗,不仅可与机体VEGF受体(VEGFR)竞争性结合抑制肿瘤生长,促进畸形血管重塑,还可提高肿瘤细胞对药物的摄取能力,进而增强疗效。基于AURELIA随机Ⅲ期试验之后,韩国妇科肿瘤学组在REBECA试验中证实了单独采用贝伐珠单抗治疗复发性卵巢癌患者的疗效及安全性[11]。但HUANG等[12]荟萃34项研究显示,贝伐珠单抗联合铂类化疗药物虽在一定程度上改善了复发性铂类敏感卵巢癌患者的FPS及OS,但较单独化疗相关不良事件有所增加。而PARP抑制剂可与PARP的烟酰胺腺嘌呤二核苷酸结合造成构象异构,以维持DNA-PARP可逆解离稳定性,因为形成的DNA-PARP复合物在机体长期存在,有助于阻断肿瘤细胞损伤修复进程[13]。奥拉帕尼单药治疗乳腺癌1号/2号基因(BRCA1/2)突变晚期卵巢癌患者表现出明显抗肿瘤活性(ORR 34%,缓解持续时间7.9个月)。一项SOLO Ⅲ期研究显示,奥拉帕尼单独治疗复发性铂类敏感卵巢癌患者,ORR高于化疗组(72.2%vs.52.4%),且不提高不良反应[14]。CSIZMAR等[15]研究指出,PARP抑制剂可与贝伐珠单抗发挥协同作用增强治疗效果。综上所述,目前单一靶向治疗效果有限,且PARP抑制剂可增强贝伐珠单抗的疗效,故将奥拉帕尼联合贝伐珠单抗治疗复发性铂类敏感卵巢癌具有可行性,但疗效及安全性有待进一步证实。
本研究参考2009年实体瘤疗效评价标准[9]并检测复发性铂类敏感卵巢癌患者治疗前后血清肿瘤标志物水平进行综合疗效评估。作为一类酸性抑制性蛋白质的HE4,主要来源于生殖道上皮,通常情况下在正常卵巢细胞中无表达,在卵巢癌患者中呈高表达;CA125为临床预测卵巢癌发生的特异性肿瘤标志物,在健康人群中水平较低,在卵巢癌患者中水平明显上升;CTC是肿瘤细胞转移、脱落进入机体血液循环系统后于血清中的残留,其水平高低可较好地反映卵巢癌的发生和进展情况。本研究结果显示,观察组患者ORR、DCR均高于对照组,且治疗后血清HE4、CA125、CTC水平均更低。由此表明,与铂类药物化疗治疗比较,复发性铂类敏感卵巢癌患者采用奥拉帕尼联合贝伐珠单抗治疗近期疗效更好。究其原因在于奥拉帕尼可与贝伐珠单抗发挥协同作用,具体机制如下:(1)贝伐珠单抗治疗可抑制VEGFR-2介导的血管生成,诱导肿瘤微环境缺氧,在缺氧条件下,蛋白质产生的DNA修复潜力降低,故可增强奥拉帕尼的敏感性;(2)贝伐珠单抗可抑制VEGFR-3,使BRCA表达下调,进而对诱导细胞周期产生阻碍,并发挥化学增敏效果,故VEGFR-3抑制可使BRCA型卵巢癌患者从奥拉帕尼治疗中获益;(3)贝伐珠单抗联合奥拉帕尼还可对卵巢癌细胞侵袭及微血管内皮细胞形成产生抑制。本研究观察组患者ORR为52.63%,原因可能与纳入的研究对象异质性、纳入和排除标准及治疗方案差异所致,与陈昭燕等[16]研究相似。因卵巢癌患者应用贝伐珠单抗治疗胃肠反应、骨髓抑制及肾脏毒性等不良反应较为常见,多为Ⅰ+Ⅱ级,Ⅲ级较少,无Ⅳ级。而使用奥拉帕尼亦较易出现消化不良、腹痛等胃肠反应,贫血等血液损伤,以及骨髓抑制等不良反应。本研究结果显示,两组患者Ⅲ+Ⅳ级不良反应均较少,且Ⅰ+Ⅱ级不良反应中,观察组患者胃肠反应及骨髓抑制发生率均较对照组有所降低,提示奥拉帕尼联合贝伐珠单抗治疗还可降低不良反应发生率。究其原因:为了保证疗效,卡铂/多柔比星脂质体化疗使用剂量通常偏高,并且铂类药物长期使用可导致患者耐受性不佳,由此可加重骨髓抑制、肾脏毒性等不良反应。而贝伐珠单抗在对血管生长产生抑制发挥疗效的同时,可在一定程度上影响机体的凝血功能,由此造成胃肠反应及骨髓抑制。而贝伐珠单抗联合奥拉帕尼治疗后因作用机制不同可发挥协同效应,从而降低贝伐珠单抗的使用剂量,因此相关不良反应有所降低,这与RAY-COQUARD等[17]研究发现奥拉帕尼联合贝伐珠单抗中高血压(>3级)发生率低于贝伐珠单抗相类似。本研究结果显示,观察组患者中位PFS、OS均高于对照组,由此提示该联合治疗策略还有助于生存预后改善,这与权瑞泉等[18]纳入96例复发性铂类敏感卵巢癌患者开展的研究证实,奥拉帕尼联合贝伐珠单抗治疗的PFS为8.3个月,高于化疗治疗的5.5个月类似。
综上所述,复发性铂类敏感卵巢癌患者应用奥拉帕尼联合贝伐珠单抗治疗可获确切的近期疗效,肿瘤标志物水平降低,且不良反应较少,远期生存预后较好。



