曹丽芝,曾 勇,任华益,陈金燕
湖南省肿瘤医院药学部,湖南长沙 410013
卵巢原发性恶性肿瘤中有60%~80%病理类型属于上皮性卵巢癌。卵巢癌作为最常见的女性生殖系统恶性肿瘤,由于其临床发病隐匿,且缺乏特异性的早期发病指征,晚期卵巢癌患者生存率极低,仅达到25%左右[1-3]。目前,上皮性卵巢癌患者的预后以及生活质量均无法得到很好的提升。20世纪90年代以来,多项大规模的临床研究提示,采用紫杉醇联合顺铂作为晚期卵巢癌的标准化疗方案对于该类患者的治疗具有及其重要的地位。但是,在上述联合化疗过程中,因为患者表现的对铂类药物耐药的现象导致疗效不佳是众多临床学者无法回避的客观事实。铂类药物作为一类卵巢癌的化疗过程中最有效的细胞毒药物,通过形成铂-DNA络合物,导致DNA致命性损伤,诱导细胞凋亡发挥作用[4-5]。铂类药物虽然耐药机制十分复杂,最新的研究已经明确DNA损伤修复是其最主要的机制之一。在DNA的损伤修复过程中,DNA聚合酶发挥至关重要的作用,其中聚合酶η起最关键的作用。DNA聚合酶通常分为经典聚合酶以及跨损伤复制聚合酶两种,跨损伤复制聚合酶尤其是聚合酶η蛋白能够在细胞DNA受到损伤的情况下保证细胞的复制得以顺利进行,在保护细胞的同时也造成了耐药现象的发生[6-8]。根据以上背景,笔者认为从聚合酶η蛋白的表达情况出发,分别从基因、蛋白水平研究该聚合酶与顺铂药物敏感性的关系,结合顺铂临床疗效的观察,对于分析顺铂耐药的机制有着积极的意义。本文在基础研究水平,通过MTT法比较siRNA沉默目的基因前后OVCR3细胞对于铂类药物的敏感性,首先验证DNA聚合酶η蛋白与细胞顺铂敏感性的关系。同时,通过分析病理组织标本中聚合酶η蛋白表达情况,观察其与临床资料的相关性。旨在从基础以及临床两个水平分析聚合酶η蛋白在卵巢上皮癌顺铂耐药过程中发挥的作用,为下一步攻克铂类药物耐药现象提供前期研究基础。
1 材料与方法
1.1 材料
1.1.1 细胞 OVCR3细胞购自上海中科院细胞生化所。
1.1.2 病理组织来源 选取我院入院治疗的卵巢上皮癌50例患者手术切除病理组织标本。患者年龄23~63岁,平均43.7岁。所有组织标本经病理证实为上皮性卵巢癌。上皮性卵巢癌按FIGO标准分期和组织学分级(GRADE)。
1.1.3 主要试剂 RNA干扰试剂盒 (Silencer TM siRNA Construction Kit)购自美国Ambion公司;阳离子脂质体转染试剂盒Lipofectamine TM 2000购自Invitrogen公司;噻唑蓝(MTT)(Sigma公司);RT-PCR 试剂盒购自 Sigma公司;目的蛋白鼠单克隆抗体为美国ADI抗体公司产品。
1.2 方法
1.2.1 siRNA的设计及合成 根据DNA聚合酶η蛋白编码基因序列以及siRNA设计原则,由启始密码子开始,选择长度为20个bp的候选序列为siRNA靶序列。通过Blast软件进行同源性分析,排除存在同源序列的靶序列,并最终确定3段长度为21bp的基因序列为靶序列。靶序列的确定与引物合成由Sigma公司完成。
1.2.2 MTT法进行耐药性分析 取对数生长期OVCR3细胞株接种于96孔板,每孔1×106/ml单细胞悬液,每孔接种90 μl,每组设 3 个复孔,加入不同浓度的顺铂(10 μmol/L,30 μmol/L,60 μmol/L),空白对照为细胞培养液,阴性对照为未处理的细胞悬液。培养48 h后加入5 mg/ml MTT溶液,每孔200 μl,孵育12 h后 加入DMSO 100 μl,摇匀10 min,酶标仪测定光密度D570 nm值。通过直线回归法计算药物的IC50。
1.2.3 RT-PCR检测聚合酶η编码基因表达 在6孔板中接种2×105/孔浓度的单细胞悬液,待细胞培养至85%的覆盖率时,使用Trizol提取总RNA,RT-PCR试剂盒逆转录为cDNA,使用引物扩增目的基因。配置2.0%琼脂糖凝胶,在120 V、25 min条件下对PCR产物进行电泳检测,并用凝胶成像系统进行图片的采集。
1.2.4 免疫染色及结果判定 4%甲醛固定标本,石蜡包埋后切片。使用1∶50浓度单抗工作液,采用S-P法染色,阳性着色部位在细胞核。应用枸橼酸盐缓冲液(PH 6.0)以及加热法进行抗原修复。阳性定位于细胞核,镜下见着棕黄色的细胞为阳性,从阳性表达强度和阳性表达率两方面进行双盲法观察与记分。染色强度分 4级:无表达为0分,可疑表达为1分,弱阳性表达为 2分,阳性表达为3分,强阳性表达为4分。表达阳性率按百分比分别记分:<5%为0分,5%~25%为1分,26%~50%为2分,>50%为3分。最后得分为每个研究病例的染色强度和阳性百分数相加数,最后分为3个级别:0~1 分为阴性(-),2~3 分为阳性(+),4~5 分为强阳性(++)。
1.3 临床资料收集
收集患者住院号、姓名、年龄、住院时间、手术日期、术后评价、手术病理分期、肿瘤病理类型、肿瘤组织分化程度、术后至初次化疗开始时间、化疗方案、初次化疗至复发的时间、化疗疗程、CA125水平变化等指标。
1.4 疗效判定标准
完全缓解(CR):所有目标病灶消失;部分缓解(PR):病灶长径总和缩小≥30%;病情稳定(SD):病灶长径总和有缩小但未达到30%或者增加<20%;疾病进展(PD):病灶长径总和增加>20%。 有效率(RR)=完全缓解(CR)+部分缓解(PR)。
1.5 随访
入组通过电话方式进行随访,了解患者的生存期以及是否同期进行相关治疗。患者从初次化疗开始直至死亡或者是研究结束的时间间隔定义为生存期。
1.6 统计学方法
采用SPSS 13.0统计软件进行分析。计量资料采用均数±标准差(±s)表示,两样本均数比较采用t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 siRNA对OVCR3细胞DNA聚合酶η蛋白编码基因表达的影响
采用Alpha Innotech软件采集比较siRNA转染前后,OVCR3细胞DNA聚合酶η蛋白编码基因表达差异,结果显示以30 nmol/L浓度转染细胞24 h后,目的基因表达水平显着降低(P<0.05),在 24 h 后下调(85.37±0.59)%。 见图 1。
2.2 MTT法检测siRNA转染后,OVCR3细胞对顺铂敏感性的改变
分别对对照组细胞以及siRNA处理后的细胞,通过酶标仪在570 nm波长测定吸光度值(OD值)。具体的药物抑制率计算公式为:药物抑制率=(1-OD实验组-OD空白对照/OD阴性对照-OD空白对照)×100%。结果显示,不同浓度顺铂(10μmol/L、30 μmol/L、60 μmol/L) 对 对 照 组 细 胞 的 抑 制 率 分 别 为(35.27±0.98)%、(62.31±0.75)%、(79.26±0.88)%; 不同浓度顺铂(10 μmol/L、30 μmol/L、60 μmol/L)对 siRNA 处理后细胞的抑制率分别为(57.15±0.64)%、(73.57±0.53)%、(88.19±0.55)%。通过拟合回归直线,顺铂对两组细胞的IC50分别为(46.66±2.23)μmol/L、(30.21±3.09)μmol/L,差异有统计学意义(P<0.05)。

2.3 DNA聚合酶η蛋白在卵巢癌组织中的表达
50例组织标本中,DNA聚合酶η蛋白表达为强阳性标本13例,占26.0%;阳性标本25例,占50.0%;阴性标本12例,占24%。见图2-4。
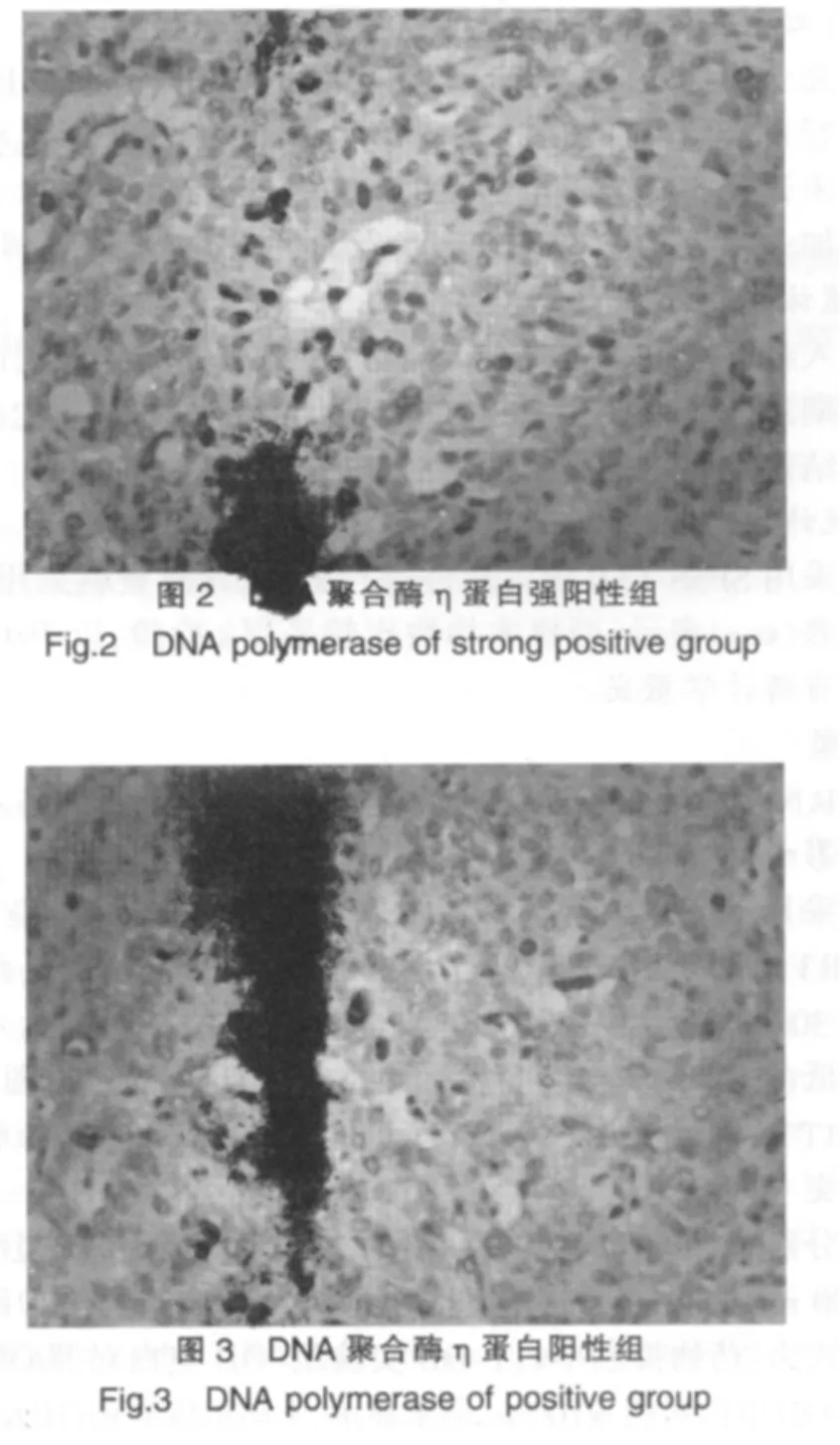
2.4 DNA聚合酶η蛋白表达差异与TP方案治疗患者近期疗效的关系
50例共完成TP化疗322个疗程,平均每个患者6.44个疗程。总有效率为64.0%。其中,聚合酶表达强阳性组有效率为46.2%,阳性组有效率为64.0%,阴性组有效率为83.3%,三组比较差异有统计学意义(P<0.05)。见表1。
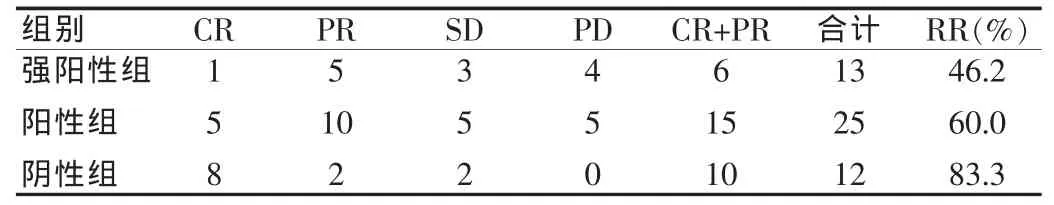
表1 不同DNA聚合酶表达含量组间TP方案治疗近期疗效比较(例)Tab.1 Short term effect of TP therapy strategy among the groups with different DNA polymerase expression(caes)
2.5 DNA聚合酶η蛋白表达差异与TP方案治疗患者远期疗效的关系
截至2010年3月31日,随访50例患者中位生存时间为(23.5±5.1)个月,其中DNA聚合η蛋白表达强阳性组中位生存时间为(15.7±3.6)个月,阳性组为(18.5±2.7)个月,阴性组为(28.3±1.9)个月,三组比较差异有统计学意义(P<0.05)。
3 讨论
卵巢癌的临床诊疗过程具有早发现困难、术后易复发、对化疗中度或低度敏感的特点,目前的临床治疗主要包括肿瘤细胞减灭术以及化疗药物联合治疗两种手段。该类患者近20年的治疗后5年生存率在40%左右。
铂类药物属于影响细胞DNA合成的周期非特异性抗肿瘤药物,具有广谱、对实体瘤尤其是对一般化疗不敏感的肿瘤效果显着的特点。目前,对初次治疗的上皮性卵巢癌的有效率可以达到50%左右,是目前一线化疗方案中的重要治疗药物。
铂类药物的耐药现象一直是临床工作者与科研工作保持高度重视的问题之一。也是导致肿瘤患者无法完成系统化疗的重要原因之一。从药物的作用机制反推耐药发生的机制,并寻求解决的方案是目前探讨铂类耐药的重要研究方向。从作用机制来看,铂类药物是通过破坏细胞中的DNA双链发挥细胞毒作用。目前的研究已经明确,细胞自身存在修复机制对抗药物的破坏进程。如果修复的机制强于药物的破坏进程,细胞将显现出对药物的敏感性降低,甚至是引发耐药现象的发生[9]。DNA聚合η蛋白是细胞修复过程中重要的蛋白,尤其是对于存在结构破坏的DNA的修复[10]。
基于以上背景,笔者开展了本次研究。从细胞水平以及临床观察两个方面对于DNA聚合η蛋白在顺铂耐药现象中发挥的作用进行探讨。在体外研究水平,笔者将目的基因表达使用沉默的方法加以抑制,观察目的基因表达与细胞对顺铂的敏感性的影响。结果显示,未进行目的基因沉默的OVCR3细胞以及基因沉默的OVCR3细胞对顺铂的敏感性差异明显,顺铂对上述两种细胞的IC50分别为(46.66±2.23)μmol/L、(30.21±3.09) μmol/L,差异有统计学意义(P<0.05)。该结果的得出可以明确DNA聚合η蛋白编码基因的表达能够明显影响细胞对于顺铂药物的敏感性,且其表达的下调能够增加细胞的药物敏感性。从机制上分析,目的基因的沉默将直接导致后续相应功能蛋白的表达下调,导致能够发挥修复作用的DNA聚合η蛋白的表达下降,并直接导致细胞对于药物敏感性的增加。在体外研究的基础上,笔者使用免疫组化的方法观察不同患者病理组织的DNA聚合η蛋白的表达。结果提示,不同患者间目的蛋白的表达存在明显差异,且蛋白表达的差异与药物的近期疗效呈现相关性。其中,聚合酶表达强阳性组有效率为46.2%,阳性组有效率为60.0%,阴性组有效率为83.3%,三组比较差异有统计学意义(P<0.05)。结合远期疗效观察,随访50例患者中位生存时间为(23.5±5.1)个月,其中DNA聚合η表达强阳性组中位生存时间为(15.7±3.6)个月,阳性组为(18.5±2.7)个月,阴性组为(28.3±1.9)个月,三组间比较差异有统计学意义(P<0.05)。临床观察的结果显示DNA聚合η蛋白表达相对较低患者,药物治疗的有效率以及患者的生存期均较高。从临床水平能够一定程度的验证DNA聚合η蛋白的表达下降,细胞对顺铂敏感性增高的体外实验结果。
本次观察,分别使用基因沉默技术以及免疫组化的方法,分别从体外细胞水平以及体内临床观察两个层面验证了DNA聚合η蛋白对于肿瘤细胞对顺铂的敏感性以及化疗药物疗效之间的关系,提示DNA聚合η蛋白的表达下调,能够增加肿瘤细胞对药物的敏感性。上述结论为制药企业开发新的化疗药物位点以及临床医生制订治疗模式提供了前期的基础性研究。
[1]Liu J,Matulonis UA.New advances in ovarian cancer [J].Oncology 2010,24(8):721-728.
[2]Miller RE,Rustin GJ.How to follow-up patients with epithelial ovarian cancer[J].Curr Opin Oncol,2010,22(5):498-502.
[3]Roett MA,Evans P.Ovarian cancer:an overview[J].Am Fam Physician,2009,80(6):609-616.
[4]Mei L,Chen H,Wei DM,et al.Maintenance chemotherapy for ovarian cancere[J].Cochrane Database Syst Rev,2010,8(9):74-77.
[5]GlaysherS,GabrielFG,JohnsonP,etal.Molecularbasisofchemosensitivity of platinum pre-treated ovarian cancer to chemotherapy[J].Br J Cancer,2010,103(5):656-662.
[6]Broyde S,Patel DJ.DNA repair:How to accurately bypass damage[J].Nature,2010,465(7301):1023-1024.
[7]Livneh Z,Ziv O,Shachar S.Multiple two-polymerase mechanisms in mammalian translesion DNA synthesis[J].Cell Cycle,2010,9(4):729-735.
[8]Rey L,Sidorova JM,Puget N,et al.Human DNA polymerase eta is required for common fragile site stability during unperturbed DNA replication[J].Mol Cell Biol,2009,29(12):3344-3354.
[9]Ide H,Shoulkamy MI,Nakano T,et al.Repair and biochemical effects of DNA-protein crosslinks[J].Mutat Res,2010,23(5):521-527.
[10]Falik-Zaccai TC,Keren Z,Slor H.The versatile DNA nucleotide excision repair(NER)and its medical significance[J].Pediatr Endocrinol Rev,2009,7(2):117-122.



