杨根欢,吴 为,李砚川,倪 冷,王占启,宋希涛,刘昌伟
1中国医学科学院 北京协和医学院 北京协和医院血管外科,北京100730
2中国医学科学院 北京协和医学院 基础医学研究所医学分子生物学国家重点实验室,北京100005
血红素加氧酶-1(heme oxygenase-1,HO-1)是体内血红素代谢的限速酶,它可以将血红素代谢为胆红素、一氧化氮及Fe2+。胆红素在体内具有强大的抗氧化作用,一氧化氮具有重要的细胞保护作用,Fe2+也是重要的抗氧化损伤的物质[1]。因此HO-1在体内具有重要的抗氧化损伤和细胞保护的作用,同时还发现其具有抗炎、抗凋亡等重要作用[2]。大量研究表明HO-1对机体的多个脏器均具有重要的保护功能,同时还与肿瘤有密切关系[3]。氧化损伤可由活性氧、氧自由基及超氧离子等引起,能够氧化体内的核酸、蛋白质及脂质,给机体带来巨大的损害[4]。有研究证实,氧化损伤能够造成细胞凋亡、细胞信号转导异常、细胞膜流动性异常、炎症的产生及癌症的发生等[5]。本研究构建携带HO-1基因的慢病毒载体,同时筛选出能稳定表达HO-1的单克隆细胞系并对其抗氧化损伤功能进行初步鉴定,为进一步研究HO-1基因的功能奠定基础。
材料和方法
材料 改造的pLentiLox3.7质粒、慢病毒辅助质粒 (plp1、plp2、VSVG),HEK293T细胞由中国医学科学院北京协和医学院基础医学研究所医学分子生物学国家重点实验室惠赠。引物合成 (美国Invitrogen公司),限制性核酸内切酶和T4 DNA连接酶 (英国NEB公司),DNA聚合酶 (北京Transgene生物技术有限公司),FuGENE HD转染试剂 (瑞士Roche公司),高糖-DMEM培养基 (美国Hyclone公司),人脐静脉内皮细胞 (human umbilical vein endothelial cells,HUVEC)及内皮细胞培养基 (ScienCell公司),Opti-MEM(美国Gibco公司),胎牛血清 (美国Gibco公司),鼠抗人HO-1抗体 (美国BD公司),山羊抗小鼠IgG抗体(北京中杉金桥有限公司),细胞内氧化应激活性氧红色荧光检测试剂盒 (上海杰美基因医药科技有限公司)。
引物设计与目的基因扩增 根据Genebank人源HO-1基因的序列设计引物,上下游引物分别加入酶切位点MluⅠ和BamHⅠ。引物序列如下:正向:5’-TAAGAATTCGCCACCATGGAGCGTCCGCAACC-3’;反向:5’-AATACGCGTCATGGCATAAAGCCCTACAGC-3’。PCR扩增HO-1基因,目的基因模板由中国医学科学院北京协和医学院基础医学研究所医学分子生物学国家重点实验室惠赠。PCR反应条件为:94℃预变性2 min,94℃变性1 min,55℃复性45 s,72℃延伸2 min,共30个循环;72℃延伸10 min。将PCR产物进行1%琼脂糖凝胶电泳回收。
重组质粒的构建与鉴定 对PCR产物和改造的病毒空载体pLentiLox3.7(带有标记标签)行MluⅠ和BamHⅠ双酶切。纯化后于4℃过夜连接,并将连接产物转化于感受态大肠杆菌,涂于LB平板后37℃孵育16 h。PCR鉴定3个阳性的克隆,并用3个重组质粒转染HEK293T细胞,Western blot检测 HEK293T中HO-1的表达。收集细胞并用SDS裂解液裂解细胞,充分震荡至液体透明。将细胞裂解后的液体置于100℃中孵育10 min后,常温下12 000 r/min(转矩:3 100 Nm)离心10 min。BCA法测定蛋白浓度并计算上样量。每孔上样20 μg,140 V下10%十二烷基硫酸钠聚丙烯酰胺凝胶电泳60 min。330 mA下转膜60 min,将蛋白转移至NC膜上。5%脱脂奶粉封闭。4℃下单克隆鼠抗HO-1(1∶4 000)抗体孵育过夜。洗膜3次后辣根过氧化物酶标记二抗 (1∶8 000)室温下孵育1 h,再次洗膜3次后显影。
慢病毒的包装和收集 将制备的重组质粒与辅助质粒 (plp1、plp2、VSVG)共同转染HEK293T细胞。转染前1 h更换新鲜培养基。重组质粒与辅助质粒总共50 μg,二者之比为2∶1。将二者加入150 mmol/L的NaCl中,总体积为1 ml。取FuGENE HD转染试剂20 μl加入150 mmol/L的NaCl中,总体积为1 ml,室温静置5 min。将稀释的FuGENE HD转染试剂逐滴加入质粒的稀释溶液中,轻轻混匀并室温静置20 min。将上述转染工作液逐滴加入HEK293T细胞的培养皿中,轻轻混匀,置于37℃、5%CO2的孵箱中。12 h后换液,24和48 h后收集培养基并置于4℃冰箱中保存。将收集的培养基用0.22 μm的滤器过滤,4℃离心机中18 000 r/min(转矩:27 450 Nm)离心3 h。弃掉上清后用200 μl冷PBS重悬病毒,待溶解后置于-80℃冰箱中保存或直接用于感染细胞。
病毒感染HEK293T细胞及单克隆挑选 将HEK293T细胞从液氮中取出立即置于37℃温水中,轻轻震荡使其快速溶解。然后置于离心管中,室温下2 000 r/min(转矩:300 Nm)离心。弃掉上清后,加入新鲜培养基2 ml吹匀,将细胞接种于24孔培养板中。12 h后细胞汇合80%时,分别加入5、10、20 μl病毒液感染。同时加入终浓度为5 μg/μl的聚凝胺辅助感染。感染72 h后于荧光显微镜下观察是否有绿色荧光,消化细胞并调节其终浓度为10个/ml。将细胞悬液接种于96孔细胞培养板行单克隆筛选,每周补液200 μl,4周后挑选带荧光的单克隆进行鉴定和扩大培养。同时行Western blot检测HO-1的表达。
加入过氧化氢的HEK293T及HUVEC内活性氧的检测 用二氢溴化乙啶 (dihydroethidium bromide;DHE)检测细胞内活性氧的含量是基于DHE能够完全自由通过细胞膜并在细胞内长期滞留而不外漏,一旦被细胞内活性氧氧化即转变为溴化乙啶,溴化乙啶进入细胞核后与DNA紧密结合并产生红色荧光。将稳定表达HO-1及正常对照的HEK293T细胞传代于6孔板中,其中实验组传两个孔,对照组传4个孔。细胞铺约80%时,将两个孔的实验组和两个孔的对照组加入终质量浓度为0.5 mmol/L的过氧化氢,留两孔正常HEK293T做空白对照。3 h后换液,加入稀释的DHE(1∶1 000),37℃孵育20 min。吸尽DHE后加入试剂盒中的保存液,置于荧光显微镜下观察各组荧光强度并照相,荧光的强弱代表细胞内活性氧的含量即细胞被氧化的程度。同样复苏人脐静脉内皮细胞于6孔板中,分组同HEK293T。待细胞汇合至50%时,用携带HO-1的慢病毒感染实验组的两个孔的细胞。72 h后进行实验,方法同HEK293T细胞,同时行Western blot检测HUVEC中HO-1的表达情况。
结 果
重组质粒的鉴定 将目的基因扩增产物和改造的病毒空载体pLentiLox3.7行MluⅠ和BamHⅠ双酶切后连接并转化。挑取3个阳性克隆行PCR鉴定,结果显示目的基因HO-1片段大小与预期的相符 (图1)。用3个重组质粒转染HEK293T细胞,48 h后置于荧光显微镜下观察,结果显示绿色荧光明显且转染效率较高(图2)。收集转染重组质粒的细胞行Western blot检测HO-1的表达,结果显示与对照组相比HO-1(带有标记标签)表达明显增高 (图3)。

图2 重组质粒转染HEK293T细胞Fig 2 The HEK293T cells transfected by the recombinant plasmid

图3 转染重组质粒的HEK293T细胞行Western blot检测HO-1Fig 3 Detecting the HO-1 in the transfected HEK293T cells by Western blot
慢病毒包装 将重组质粒与辅助质粒共同转染HEK293T细胞。24 h后置于荧光显微镜下观察有绿色荧光出现,表明质粒转染成功。48 h后荧光显微镜下观察,荧光亮度强且表达率高,表明已成功包装出病毒。
慢病毒感染HEK293T细胞 用包装出的携带H0-1目的基因的慢病毒感染HEK293T细胞并行单克隆筛选,荧光显微镜下观察,结果显示稳定表达HO-1的细胞占总细胞的比例接近100%(图4)。行Western blot检测,结果显示与对照组相比实验组细胞的HO-1表达明显升高 (图5)。
过表达HO-1抗细胞氧化损伤的作用 将过氧化氢分别加入过表达HO-1及正常对照的HEK293T细胞和HUVEC中,用DHE检测细胞内活性氧的含量,结果显示与正常对照组相比,加入过氧化氢的细胞内活性氧的含量明显增多 (荧光强度明显增强)。而过表达HO-1后,细胞内活性氧含量明显减低 (图6)。
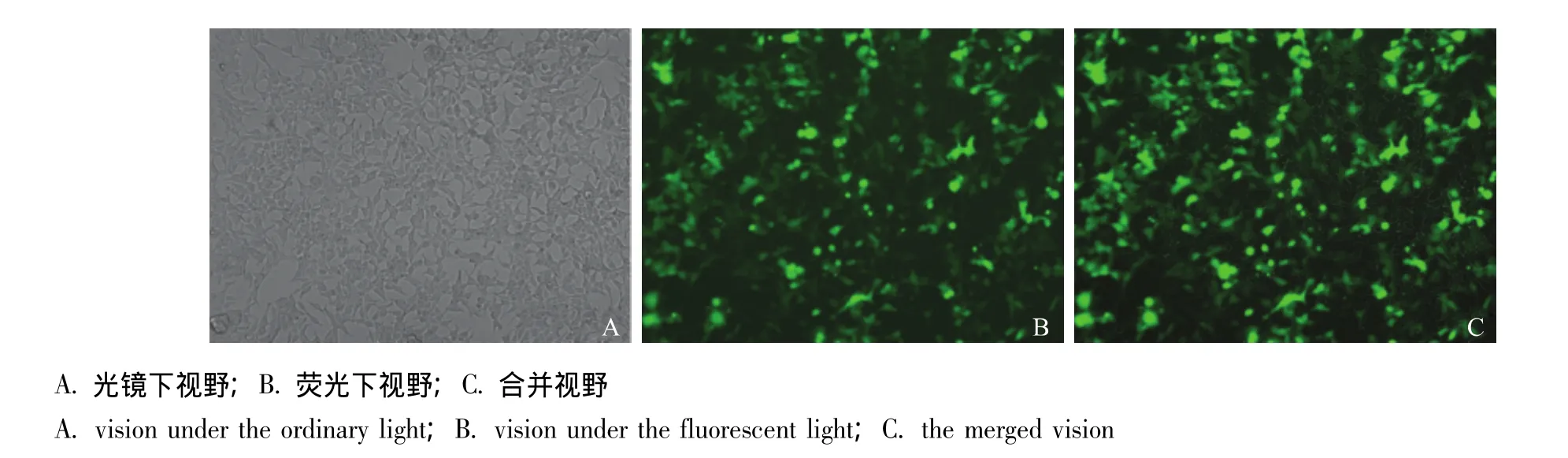
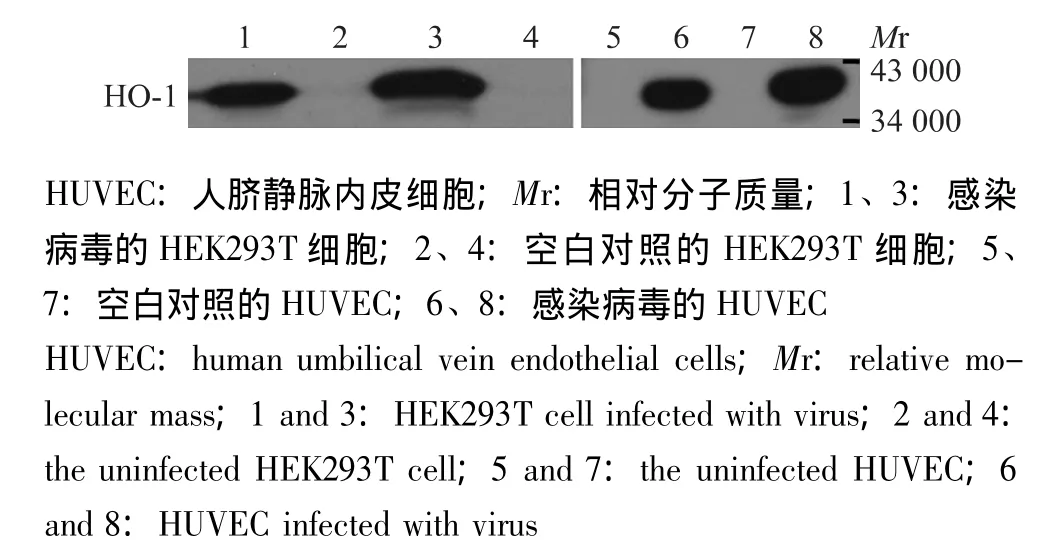
图5 感染慢病毒的HEK293T/HUVEC行Western blot检测HO-1Fig 5 Detecting the HO-1 in the infected HEK293T/HUVEC cells by Western blot
讨 论
人体内的血红素加氧酶有3种不同的亚型,其中HO-1被称为热休克蛋白32,是诱导型的血红素加氧酶。氧化损伤、炎症刺激、缺血、缺氧、感染等均可诱导其表达[6]。在各种诱导因素的作用下,机体的心血管、肝脏、肾脏、肺等多个脏器均可表达HO-1[7]。大量研究表明HO-1与多种疾病密切相关,如炎症相关性疾病 (感染、哮喘)、肺损伤 (肺氧化损伤、肺纤维化、呼吸机相关的肺损伤)、心血管疾病 (心肌梗死、高血压、肺动脉高压、动脉粥样硬化)、缺血再灌注损伤、器官移植、肿瘤等[8]。
目前国内外构建的用于研究HO-1的病毒载体有腺病毒载体、腺相关病毒载体、慢病毒载体及逆转录病毒载体[9-12],各种载体均有其优缺点。慢病毒载体可以有效地将外源基因整合到宿主的染色体上,并且能够使之持久性地表达[13]。慢病毒载体不但能够感染分裂期细胞而且还能够感染非分裂期细胞,其感染细胞的种类范围广泛。同时慢病毒还具有能够容纳外源大片段基因、免疫反应较小、安全性好等优点,是目前研究基因调控及功能的常用载体[14]。本研究构建的携带HO-1的慢病毒载体具有操作简单、可重复性好、产毒量高、感染率高及表达稳定等优点。本研究通过扩增HO-1基因并将其与改造的病毒空载体pLentiLox3.7连接构建出了携带HO-1目的基因的质粒。用此质粒转染HEK293T并行Western blot检测,其HO-1表达明显升高,表明重组质粒构建成功。将包装出的病毒感染HEK293T并行Western blot检测,其HO-1表达明显升高,表明成功包装出携带HO-1的有活力的慢病毒。同时本研究用包装出的病毒感染HEK293T并筛选出能够稳定表达HO-1的细胞系,这解决了正常情况下HO-1在细胞内表达低的难点。本研究对HO-1的功能进行了初步探索,加入过氧化氢的HEK293T及HUVEC内活性氧的含量较空白对照组明显增多,表明过氧化氢对细胞具有明显的氧化损伤作用。而加入过氧化氢后,过表达HO-1的HEK293T及HUVEC内活性氧的含量较对照组明显减少,表明HO-1具有明显抗氧化损伤的作用。
综上,本研究构建了能稳定表达人HO-1的细胞系,并对HO-1的抗氧化损伤作用进行了初步研究,为进一步探索HO-1的功能和机制奠定了基础。
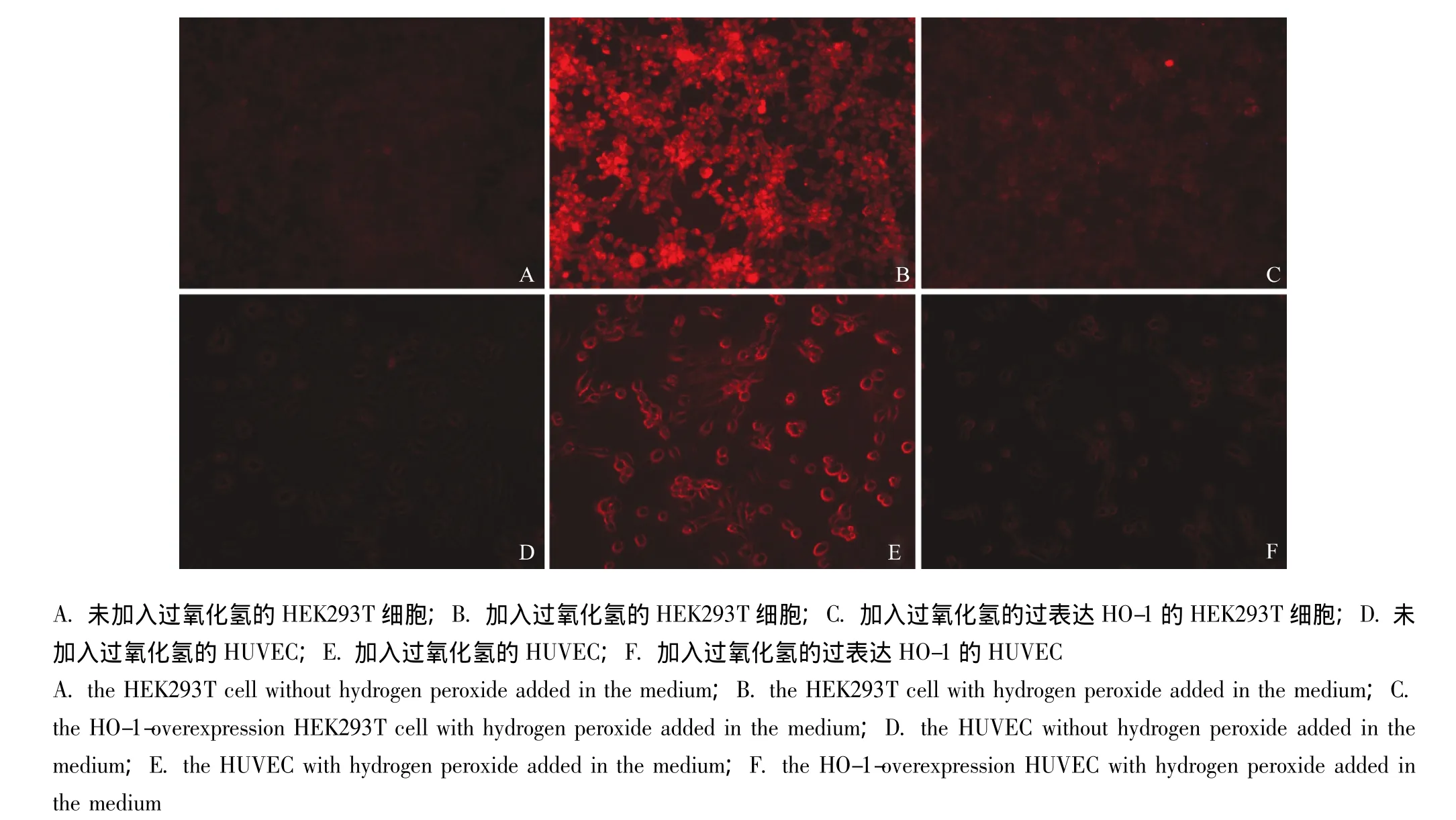
图6 过氧化氢对HEK293T/HUVEC的氧化作用及HO-1的保护作用Fig6 Oxidative role of hydrogen peroxide on the HEK293T/HUVEC and the protective role of HO-1
[1] Origassa CS,Camara NO.Cytoprotective role of heme oxygenase-1 and heme degradation derived end products in liver injury [J].World J Hepatol,2013,5(10):541-549.
[2] Choi AM,Alam J.Heme oxygenase-1:function,regulation,and implication of a novel stress-inducible protein in oxidantinduced lung injury [J].Am J Respir Cell Mol Biol,1996,15(1):9-19.
[3] Wijayanti N,Katz N,Immenschuh S.Biology of heme in health and disease[J].Curr Med Chem,2004,11(8):981-986.
[4] Selman C,Blount JD,Nussey DH.Oxidative damage,ageing,and life-history evolution:where now?[J].Trends Ecol Evol,2012,27(10):570-577.
[5] Fu PP,Xia QS,Hwang HM,et al.Mechanisms of nanotoxicity:generation of reactive oxygen species[J].Yao Wu Shi Pin Fen Xi,2014,22(1,SI):64-75.
[6] Calay D,Mason JC.The multifunctional role and therapeutic potential of ho-1 in the vascular endothelium [J].Antioxid Redox Signal,2014,20(11):1789-1809.
[7] Shibahara S,Muller R,Taguchi H,et al.Cloning and expression of cDNA for rat heme oxygenase[J].Proc Natl Acad Sci U S A,1985,82(23):7865-7869.
[8] Ryter SW,Alam J,Choi AM.Heme oxygenase-1/carbon monoxide:from basic science to therapeutic applications [J].Physiol Rev,2006,86(2):583-650.
[9] Juan SH,Lee TS,Tseng KW,et al.Adenovirus-mediated heme oxygenase-1 gene transfer inhibits the development of atherosclerosis in apolipoprotein E-deficient mice[J].Circu-lation,2001,104(13):1519-1525.
[10] Melo LG,Agrawal R,Zhang LN,et al.Gene therapy strategy for long-term myocardial protection using adeno-associated virus-mediated delivery of heme oxygenase gene[J].Circulation,2002,105(5):602-607.
[11] Abraham NG,Quan S,Mieyal PA,et al.Modulation of cGMP by human HO-1 retrovirus gene transfer in pulmonary microvessel endothelial cells[J].Am J Physiol Lung Cell Mol Physiol,2002,283(5):L1117-L1124.
[12] Laumonier T,Yang S,Konig S,et al.Lentivirus mediated HO-1 gene transfer enhances myogenic precursor cell survival after autologous transplantation in pig [J].Mol Ther,2008,16(2):404-410.
[13] Segura MM,Kamen AA,Garnier A.Viral vectors for gene therapy[M].Barcelona:Humana Press,2011:89-116.
[14] Kaikkonen MU,Lesch HP,Pikkarainen J,et al.(Strept)avidin-displaying lentiviruses as versatile tools for targeting and dual imaging of gene delivery [J].Gene Ther,2009,16(7):894-904.



