林侃如 陆伟辉 贺华 沈卫星 王庆
胆囊息肉样病变是指胆囊壁向腔内呈息肉状生长的所有非结石性病变,包括肿瘤性息肉和非肿瘤性息肉[1],其发病可能与胆囊结石、慢性胆囊炎、胆固醇代谢紊乱等相关[2]。肿瘤性息肉病变早期缺乏特异性的临床症状,病理诊断有助于临床治疗方案的制定,且对预后具有重要意义[3]。随着人们健康意识的提高和影像学技术的快速发展,肿瘤性息肉病变的检出率逐渐提升,国内一些地区的发病率高达4%以上,恶性病变的发生率为0.8%~27%,具有较高的恶变潜能[5]。本研究通过观察胆囊肿瘤性息肉病变发生恶性变的影像学特征,并分析其影响因素,为临床的预防及治疗提供依据。
1 资料与方法
1.1 临床资料 回顾性收集2015年6月至2020年5月于本院普外科进行手术的胆囊息肉样病变患者500 例。其中,男264例,女236例;年龄(48.57±13.94)岁;肿瘤性息肉91例,作为肿瘤性息肉组;非肿瘤性息肉409例,作为非肿瘤性息肉组。(1)纳入标准:①术前常规超声检查,确认为胆囊息肉病变,并接受磁共振动态增强扫描(DCE-MRI)检查;②经术后病理诊断结果证实;③签署知情同意书。(2)排除标准:①严重心肺功能损害、造影剂有禁忌的患者;②妊娠和哺乳期妇女;③术后病理证实为慢性胆囊炎者;④高血压、肺动脉高压以及呼吸窘迫综合症的患者。
1.2 研究方法 (1)资料收集:包括患者的性别、年龄、临床症状、息肉大小、息肉数目、是否伴有结石等情况,以及病理诊断结果。(2)实验室指标检测:抽取所有患者的空腹静脉血3 mL,采用全自动生化分析仪(日本SYSMEX XN-1000)检测谷丙转氨酶(ALT)、碱性磷酸酶(ALP)、谷草转氨酶(AST)、总胆汁酸(TBA)、总胆固醇(CHOL)、甘油三酯(TG)、高密度脂蛋白-胆固醇(HDL-C)、低密度脂蛋白-胆固醇(LDL-C)、总胆红素(TBIL)、直接胆红素(DBIL)等指标水平;采用全自动微粒子化学发光免疫分析仪(美国雅培公司i2000)检测甲胎蛋白(AFP)、癌胚抗原(CEA)、糖类抗原(CA199)等指标水平。(3)DCEMRI检查:采用 GE Signa HDxt 3.0T 磁共振。检查前4 h内禁食、禁水,排空膀胱,取仰卧位,脚先进,身体居中。常规扫描,T1WI序列参数:TR 360 ms,层厚4 mm,层距为1 mm,FOV为280 mm×280 mm,矩阵为384×192,带宽为62.5,扫描时间 2 min 22 s;T2WI序列参数:TR 3,500 ms,层厚4 mm,层距1 mm,FOV为280 mm×280 mm,矩阵为320×256,带宽为 50;T2WIFS检测参数:TR3,800 ms,层厚4 mm,层距1 mm,FOV为280 mm×280 mm,带宽为 50。常规扫描完成后,患者肘静脉注射造影剂钆-喷替酸葡甲胺0.2 mL/kg,注射速率为 3 mL/s,注射完成后冲入0.9%NaCl溶液20 mL,之后进行三维容积超快速多期动态增强序列扫描,通过GEfunctool 4.4后处理工作站对数据进行处理,并绘制信号强度-时间(SI-T)曲线,采用3个参数描述SI-T 曲线特征,包括到达峰值时间(从开始扫描到强化峰值所需时间)、最大强化程度(峰值信号强度减去开始强化时的信号强度,再除以开始强化时的信号强度)、最快强化率(最大强化程度减去开始强化时的信号强度,再除以达峰值时间)。
1.3 统计学方法 采用SPSS 20.0统计软件。计数资料以[n(%)]表示,组间比较采用χ2检验或Fisher精确检验;计量资料符合正态分布以(±s)表示,采用t检验;肿瘤性息肉病变的危险因素采用多变量Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 病理诊断结果 肿瘤性息肉组,腺瘤69例、胆囊癌22例;按照Nevin分期,胆囊癌I期8例,Ⅱ期14例,其中11例伴有胆结石;腺瘤病变,多发41例,单发28例。非肿瘤性息肉组,胆固醇性息肉353例,其中合并胆结石者192例,合并胆囊炎者237例,病变单发者89例,病变多发者264例;息肉样增生28例,其中合并胆结石者15例,合并胆囊炎者11例,病变单发13例,病变多发15例;腺瘤样瘤息肉17例,其中合并胆结石者7例,合并胆囊炎者5例,病变单发6例,病变多发11例;炎性息肉11例,其中合并胆结石者4例,合并胆囊炎者3例,病变单发4例,病变多发7例。
2.2 肿瘤性息肉组与非肿瘤性息肉组患者的临床资料比较 两组患者的年龄、息肉大小、息肉数目比较,差异有统计学意义(P<0.05)。见表1。
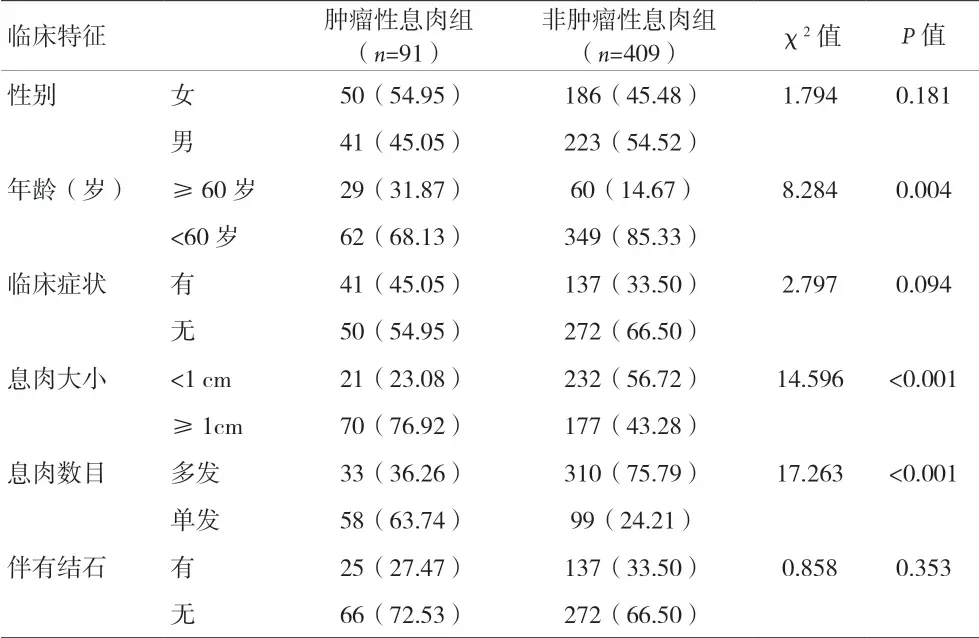
表1 两组的临床资料比较[n(%)]
2.3 肿瘤性息肉组与非肿瘤性息肉组患者的实验室指标比较 肿瘤性息肉组患者的CHOL、TG、LDL-C水平均明显高于非肿瘤性息肉组,差异有统计学意义(P<0.05)。见表2。
表2 两组患者的实验室指标水平比较(±s)
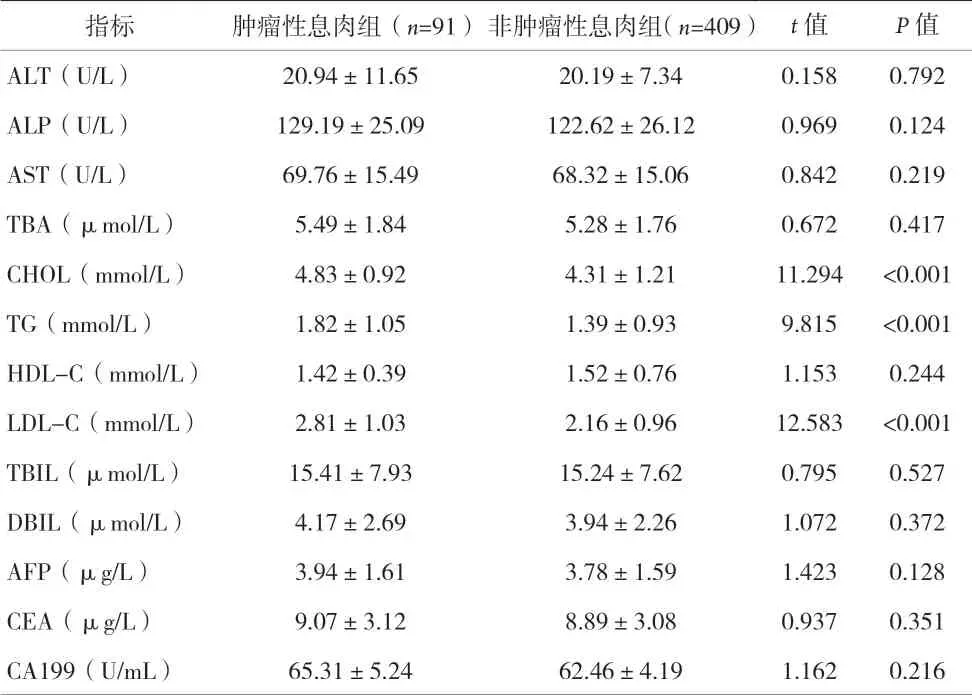
表2 两组患者的实验室指标水平比较(±s)
指标 肿瘤性息肉组(n=91)非肿瘤性息肉组(n=409) t值 P值ALT(U/L) 20.94±11.65 20.19±7.34 0.158 0.792 ALP(U/L) 129.19±25.09 122.62±26.12 0.969 0.124 AST(U/L) 69.76±15.49 68.32±15.06 0.842 0.219 TBA(μmol/L) 5.49±1.84 5.28±1.76 0.672 0.417 CHOL(mmol/L) 4.83±0.92 4.31±1.21 11.294 <0.001 TG(mmol/L) 1.82±1.05 1.39±0.93 9.815 <0.001 HDL-C(mmol/L) 1.42±0.39 1.52±0.76 1.153 0.244 LDL-C(mmol/L) 2.81±1.03 2.16±0.96 12.583 <0.001 TBIL(μmol/L) 15.41±7.93 15.24±7.62 0.795 0.527 DBIL(μmol/L) 4.17±2.69 3.94±2.26 1.072 0.372 AFP(μg/L) 3.94±1.61 3.78±1.59 1.423 0.128 CEA(μg/L) 9.07±3.12 8.89±3.08 0.937 0.351 CA199(U/mL) 65.31±5.24 62.46±4.19 1.162 0.216
2.4 肿瘤性息肉组与非肿瘤性息肉组患者的影像学特征比较 SI-T曲线呈廓清型者,多数为肿瘤性息肉,少数为非肿瘤性息肉,组间差异有统计学意义(P<0.05)。SI-T 曲线呈平台型和上升型者,多数为非肿瘤性息肉,少数为肿瘤性息肉,组间差异有统计学意义(P<0.05)。两组到达峰值时间、最大强化程度和最快强化率比较,差异均具有统计学意义(P<0.05)。若以SI-T曲线呈廓清型作为肿瘤性息肉的诊断标准,SI-T曲线呈平台型和上升型作为非肿瘤性息肉的诊断标准,敏感度为73.56%,特异度为 94.13%。见表3。
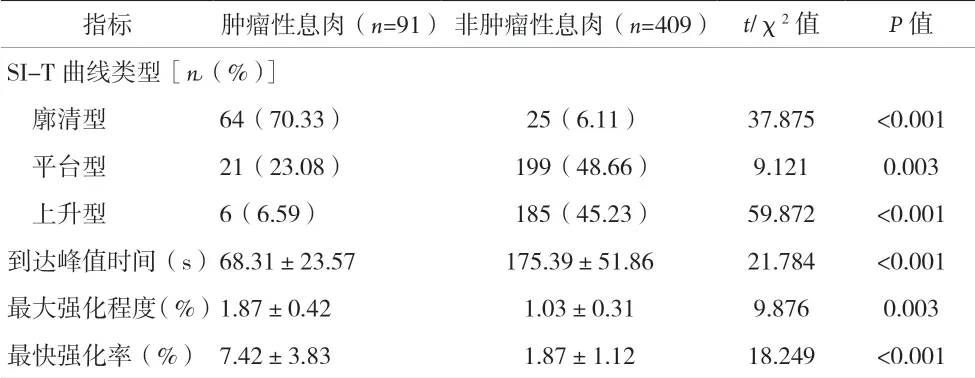
表3 两组的影像学特征比较
2.5 多因素Logistic回归分析 结果显示,年龄≥60岁、息肉≥1 cm、单发息肉、CHOL、TG、LDL-C、SI-T曲线呈廓清型、到达峰值时间、最大强化程度和最快强化率是肿瘤性息肉病变的独立危险因素,而SI-T 曲线平台型是肿瘤性息肉病变的保护因素(P<0.05)。见表4。
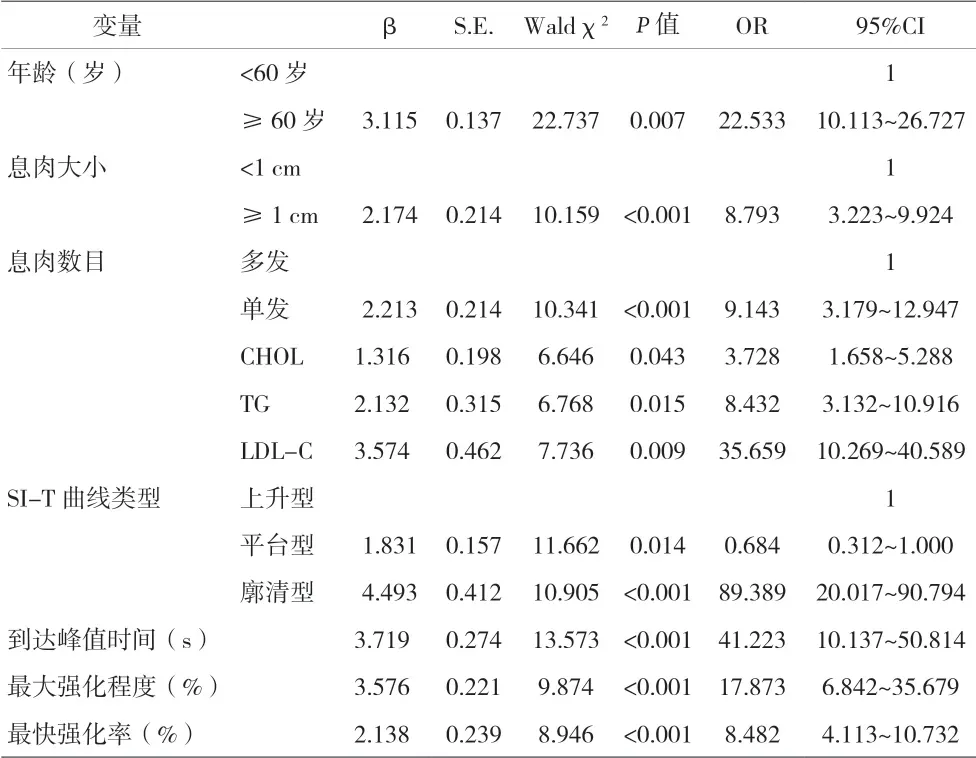
表4 肿瘤性息肉危险因素的多因素logistic回归分析
3 讨论
胆囊息肉样病变的发病机制较为复杂,是多因素相互作用的结果[5]。不同性质的胆囊息肉样病变病因各异,胆固醇异常、胆囊局部炎症反应导致胆汁合成分泌功能紊乱,以及胆囊黏膜增生、炎症刺激、胆囊壁增厚等均可能导致胆囊息肉样病变的发生和发展[6]。我国胆囊息肉样病变的发病率较高(>4%),且呈现逐年增长趋势[7],发病年龄集中在30~40岁,以男性居多[8],发病早期无明显症状,只有少数病人会出现右上腹疼痛、食欲减退、恶心、呕吐等症状[9],大多数是在健康体检中发现,目前临床诊断主要依靠超声检查,但只能说明息肉的存在,并不能解释息肉的病理性质[10]。随着影像仪器的更新迭代,胆囊息肉样病变较大者可采用CT仿真内镜、内镜超声、增强CT或磁共振检查,有助于鉴别胆囊息肉样病变、胆囊腺瘤和胆囊癌。
胆囊息肉样病变也存在向癌症转变的倾向,尤其是腺瘤,具有较高的恶性潜能,提醒临床重视[11]。通过查阅胆囊肿瘤性息肉样病变危险因素的相关研究,均提示胆囊息肉样病变>1 cm和年龄>50岁是肿瘤性息肉样病变的危险因素。本研究首先对肿瘤性息肉组与非肿瘤性息肉组患者临床资料进行比较分析,发现肿瘤性息肉组中年龄>60岁、息肉≥1 cm、息肉为单发的患者明显多于非肿瘤性息肉组,患者的年龄、息肉大小、息肉数目组间比较,差异有统计学意义(P<0.05)。再对肿瘤性息肉组与非肿瘤性息肉组患者的实验室指标及影像学特征进行比较分析,结果显示肿瘤性息肉组患者的CHOL、TG、LDL-C水平明显高于非肿瘤性息肉组;SI-T曲线呈廓清型者多数为肿瘤性息肉,少数为非肿瘤性息肉; SI-T曲线呈平台型和上升型者多数为非肿瘤性息肉,少数为肿瘤性息肉;肿瘤性息肉组和非肿瘤性息肉组的到达峰值时间、最大强化程度和最快强化率比较,差异均有统计学意义(P<0.05)。进一步采用多因素logistic 回归分析胆囊息肉样病变的危险因素,结果显示,年龄≥60岁、息肉≥1 cm、单发息肉、CHOL、TG、LDL-C、SI-T 曲线呈廓清型、到达峰值时间、最大强化程度和最快强化率是肿瘤性息肉病变的独立危险因素,而SI-T 曲线平台型是肿瘤性息肉的保护因素。在今后的诊疗中,可以结合危险因素提早制定干预措施,并进行随访观察,一经发现胆囊息肉样病变异常,应及时进行手术切除治疗。



