简丽?吴绮楠?赵启全?吕欣璐
【摘要】目的 提高临床医师对自身免疫性多内分泌腺综合征2型(APS-2)患者出现危重症并发症的诊治水平,减少漏诊和误诊。方法 报道1例出现多种内分泌腺危象的46岁APS-2女性患者,并以 “自身免疫性多内分泌腺综合征”“糖尿病急性并发症”“甲状腺功能亢进危象(甲亢危象)”(包括中英文)为检索词,对以下数据库的相关论文进行检索:PubMed、中国生物医学文献服务系统(SinoMed)、CNKI、万方数据知识服务平台、维普中文科技期刊数据库。收集并分析检索到的APS患者中合并糖尿病急性并发症、甲亢危象者的资料。结果 该例患者反复多尿、多饮18年,以恶心、呕吐半日为主要表现入院。完善相关检查后提示患者存在糖尿病酮症酸中毒合并乳酸性酸中毒、甲亢危象,最终诊断为APS-2。文献仅检索到APS-3同时合并糖尿病急性并发症及甲亢危象的2例病例,未检索到APS-2或其他APS分型的同类病例。结论 APS-2同时并发糖尿病急性并发症及甲亢危象者罕见,易被漏诊而延误病情,临床医师应提高诊治水平,及早治疗有助于患者获得良好转归。
【关键词】自身免疫性多内分泌腺综合征2型;糖尿病急性并发症;甲亢危象
Autoimmune polyendocrine syndrome type 2 complicated with hyperthyroidism crisis and diabetic acute complications: a case report and literature review Jian Li△, Wu Qinan, Zhao Qiquan, LYU Xinlu.△Department of Endocrinology, the Peoples Hospital of Dazu District, Chongqing 402360, China
Corresponding author, LYU Xinlu, E-mail: antebellumlsy@163.com
【Abstract】Objective To enhance clinicians diagnosis and treatment capability for autoimmune polyendocrine syndrome type 2 (APS-2),and reduce missed diagnosis and misdiagnosis. Methods A 46-year-old female APS-2 patient with polyendocrine crisis was reported. Using the key words of “autoimmune polyendocrine syndrome” “diabetic acute complications” and “hyperthyroidism crisis” ,relevant literatures were searched from PubMed,SinoMed,CNKI,Wanfang Data and China Science and Technology Journal Database. Data of APS patients complicated with diabetic acute complications and hyperthyroidism crisis were collected and analyzed. Results The main manifestations of this patient were repeated polyuria and polydipsia for 18 years. She was admitted due to nausea and vomiting for half a day. Relevant examinations suggested the signs of diabetic ketoacidosis complicated with lactic acidosis and hyperthyroidism crisis,and the diagnosis of APS-2 was confirmed. Only 2 cases of APS-3 combined with acute diabetic complications and hyperthyroidism crisis were found in the literature,no APS-2 or other APS types patient complicated with diabetic acute complications and hyperthyroidism crisis was searched. Conclusions APS-2 patients complicated with diabetic acute complications and hyperthyroidism crisis are rare,which is likely to miss diagnosis and delay the diagnosis and treatment. Clinicians should improve relevant diagnosis and treatment capability. Prompt treatment contributes to favorable prognosis.
【Key words】Autoimmune polyendocrine syndrome type 2;Diabetic acute complication;Hyperthyroidism crisis
自身免疫性多内分泌腺综合征2型(APS-2)是由于免疫耐受丧失导致多个内分泌腺功能受损的临床综合征,为多基因病,致病基因位于6号染色体短臂上,遗传易感性可能与细胞毒性T淋巴细胞相关抗原4 (CTLA-4)和人类白细胞抗原(HLA)相关[1]。APS-2患者至少有以下3种内分泌疾病中的2种:1型糖尿病、自身免疫性甲状腺疾病和原发性慢性肾上腺皮质功能减退症(Addison病)[1]。乳酸性酸中毒是由于乳酸生成过多、利用减少或排除障碍导致的大量乳酸在体内堆积引起的一种代谢性酸中毒,其诊断标准为血乳酸>
5 mmol/L,pH≤7.35。APS-2患者出现糖尿病酮症酸中毒合并乳酸性酸中毒、甲状腺功能亢进危象(甲亢危象)较为罕见。本文报道1例APS-2型患者出现糖尿病酮症酸中毒合并乳酸性酸中毒、甲亢危象、MODS病例,以提高临床医师对同类患者的诊治水平。
对象与方法
一、1例出现多种内分泌腺危象的APS-2患者临床资料的收集
我科于2019年4月诊治1例以糖尿病急性并发症、甲亢危象为主要表现的出现多种内分泌腺危象的46岁女性患者,收集并分析其病史、体格检查、实验室及辅助检查、治疗等资料。
二、文献检索
以“自身免疫性多内分泌腺综合征”“糖尿病急性并发症”“甲亢危象”(包括中英文)为检索词,对以下数据库截至2023年1月收录的相关论文进行检索:PubMed、中国生物医学文献服务系统(SinoMed)、CNKI、万方数据知识服务平台、维普中文科技期刊数据库。收集并分析检索到的病例中以糖尿病急性并发症、甲亢危象为临床表现的APS患者资料。
结果
一、1例出现多种内分泌腺危象的APS患者临床资料
1.入院主诉及检查
患者女,46岁,因“反复多尿、多饮18年,恶心、呕吐半日”于 2019年4月20日入院。18年前,患者无明显诱因出现“三多一少”症状,院外检查空腹静脉血糖高达20 mmol/L,查糖尿病相关抗体阴性,空腹C肽0.5 ng/dL,诊断为“1型糖尿病”,长期接受“三餐前门冬胰岛素8 U+睡前甘精胰岛素13 U”皮下注射降血糖,血糖波动大。近10年来患者反复出现恶心、呕吐,反复住院,均被诊断为“糖尿病酮症酸中毒”,经对症治疗后好转出院。本次入院前半日,患者再次出现恶心、呕吐,呕吐物为胃内容物,伴口干、多饮、多尿,无胸闷、胸痛,无视物模糊、四肢麻木,无间歇性跛行,急诊以“糖尿病酮症酸中毒”收住入院。
其他既往史:入院前1年被诊断为Graves病,长期接受规律抗甲亢治疗,目前服用甲巯咪唑
5 mg/d治疗。婚育史:已婚,育有3女1子。家族史:父母已去世,死因不详,子女均身体健康。
2.体格检查、实验室及辅助检查
体格检查:体温38.6℃,心率128次/分,呼吸22次/分,血压86/46 mmHg(1 mmHg=0.133 kPa),
血氧饱和度98%,BMI 21.75 kg/m2。嗜睡状态,脱水貌,无四肢冰凉、大理石花斑纹,眼球突出,甲状腺Ⅰ°肿大,质软,表面光滑,心、肺、腹无明显异常,双下肢无水肿。
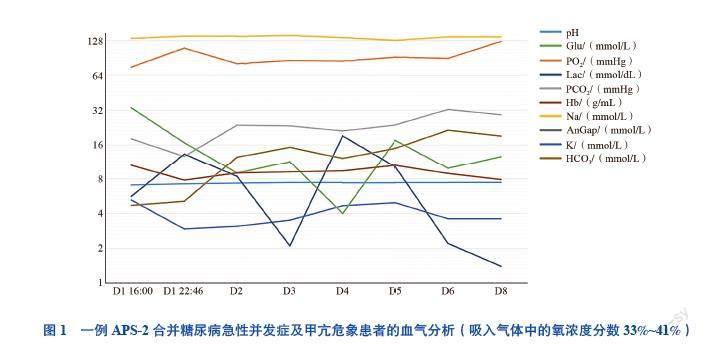
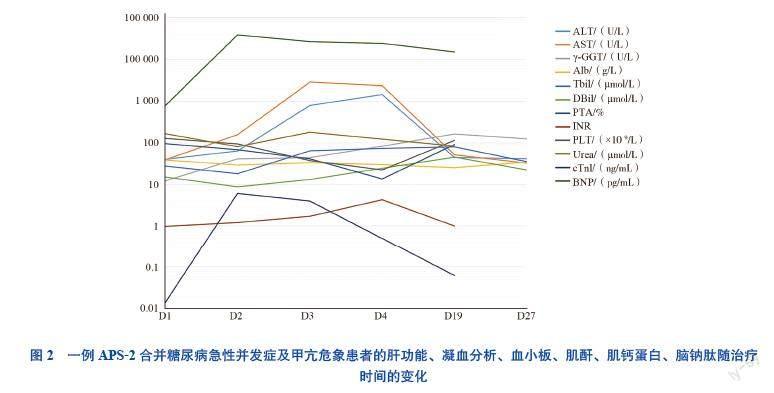
实验室及辅助检查:血红蛋白85 g/L,红细胞2.8×109/L,白细胞24.9×1012/L,中性粒细胞0.93,红细胞压积26.5%。尿葡萄糖(++)。血糖51.1 mmol/L,降钙素原6.6 ng/mL。钾5.8 mmol/L,钠132.0 mmol/L,氯94.0 mmol/L,FT3 4.9 pmol/L,FT4 31.2 pmol/L,TSH 0.1 mIU/L,促甲状腺激素受体抗体(TRAb)23.0 IU/L。血气分析、肝功能、凝血功能、血小板、肾功能、肌钙蛋白Ⅰ、氨基
端-B型利钠肽等见图1~2。血培养示少见嗜铜菌,对氨曲南、头孢唑啉、美洛培南耐药,对头孢哌酮/舒巴坦、头孢他啶、头孢呋辛敏感。戊肝抗体呈弱阳性。尿培养呈阴性。CRP、ESR、血淀粉酶、脂肪酶、凝血功能、术前感染四项(乙型肝炎、丙型肝炎、梅毒和获得性免疫缺陷综合征)、心肌酶谱、粪常规、皮质醇、抗胰岛细胞抗体(ICA)、抗GAD56、抗胰岛素抗体(IAA)、自身免疫性肝病抗体未见明显异常。心电图示窦性心动过速(120次/分),T波改变。入院第4日查血氨
241 μmol/L。心脏彩色多普勒超声检查(彩超)示三尖瓣重度反流,二尖瓣、肺动脉瓣轻度反流,肺动脉高压(轻度),左心室舒张功能减低。头部+胸腹部CT示头颅平扫未见明显异常(必要时行MRI检查);双肺下叶间质性炎症;双侧胸腔积液(少至中量),邻近肺组织外压性不张;上腔静脉内见导管影;心影增大,心包少量积液;脂肪肝,肝包膜下少量积液;胃窦壁增厚,走形僵直。
完善各项检查后,患者被诊断为:①MODS(急性肝衰竭、急性心功能不全、急性肾损伤、呼吸衰竭);②感染性休克;③少见嗜铜菌性败血症;④肝性脑病;⑤APS-2型(1型糖尿病、Graves病);⑥糖尿病酮症酸中毒合并乳酸性酸中毒;⑦甲亢;⑧肺部感染;⑨瓣膜性心脏病,三尖瓣重度反流。
3.治疗过程
对患者行深静脉穿刺置管术,检测中心静脉压为11 mmHg,超声检查示下腔静脉最大径约
2.1 cm,予补液以维持水电解质平衡、碳酸氢钠纠正酸中毒、静脉胰岛素泵降血糖、美罗培南抗感染、去甲肾上腺素维持血压、甲巯咪唑5 mg/d抗甲亢。入院第3日上午患者出现昏睡,心电图示窦性心动过速,心率波动于160~170次/分,考虑存在甲亢危象可能,遂停用甲巯咪唑,调整为予丙基硫氧嘧啶100 mg、3次/日,减少甲状腺激素的释放及合成,氢化可的松100 mg、1次/8 h改善肾上腺皮质功能相对不足,普萘洛尔10 mg、
4次/日控制心律,予去甲肾上腺素维持血压,多巴酚丁胺强心,并行持续性动静脉血液滤过治疗,患者心率控制在90~110次/分。入院第3日晚上患者出现神志恍惚、烦躁不安,查肝功能示急性肝衰竭、肝性脑病,见图2,遂停用丙基硫氧嘧啶,调整为予甲巯咪唑10 mg/d抗甲亢,维生素K辅助改善凝血功能,行血浆置换1次,每日输注血浆、冷沉淀,行连续性肾脏替代治疗(CRRT),予前列地尔改善循环、右美托米定镇静,多烯磷脂胆碱、丁二磺酸腺苷蛋氨酸、促肝细胞生长因子保肝,门冬氨酸鸟氨酸、支链氨基酸、精氨酸等治疗肝性脑病;调整抗生素为替加环素及头孢哌酮舒巴坦。入院第19日患者病情稳定,转至感染科继续接受保肝治疗,入院第27日患者情况好转、各项指标改善,见图2,遂予出院。
二、以糖尿病急性并发症、甲亢危象为临床表现的自身免疫性多内分泌腺综合征的相关文献结果
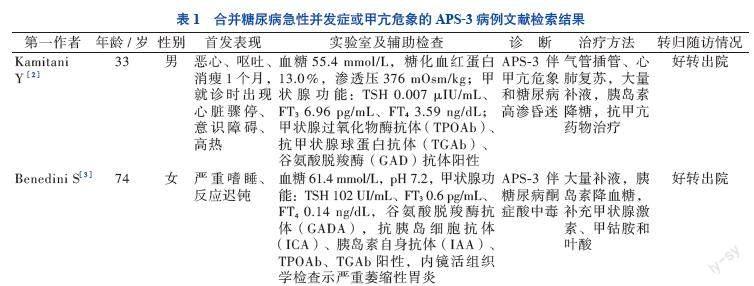
收集到以糖尿病急性并发症、甲亢危象为临床表现的APS-3型病例2例,没有APS-2型或APS其他型的相关病例。见表1。
讨论
一、APS-2型出现多内分泌腺危象的机制探讨
APS-2患者除了出现内分泌疾病之外,还可能会出现其他非内分泌器官的自身免疫性疾病,且出现的先后顺序不一,包括自身免疫性胃炎、乳糜泻、脱发、白癜风、原发性卵巢功能不全和恶性贫血病[4]。APS-2发病率为1∶20 000,女性多见,男女比例为1∶3,可于青春期或成年后发病[5]。本例患者存在1型糖尿病合并自身免疫性甲状腺疾病,肾上腺功能正常,考虑为APS-2,且出现多种内分泌腺危象,可能的机制为多个内分泌腺功能受损,各内分泌腺受损又相互影响。由于自身免疫耐受性丧失,胰岛功能损坏严重,APS-2患者的胰岛功能较普通糖尿病患者差,更容易出现糖尿病急性并发症。APS-2患者合并非内分泌器官的自身免疫性疾病,如自身免疫性胃炎、乳糜泻,容易出现脱水,更容易出现糖尿病酮症酸中毒。APS-2患者体内存在多种自身抗体,可能更容易激活或衔接T淋巴细胞和(或)其他免疫效应细胞而引起超生理反应[6]。
二、糖尿病乳酸性酸中毒原因
在无氧糖酵解的代谢过程中,当缺氧时大量丙酮就会转化为乳酸[7]。乳酸生成过多、利用和排泄减少都可能导致乳酸性酸中毒[7]。血乳酸浓度高低可以预测糖尿病患者的死亡风险。
二甲双胍是治疗糖尿病的一线药物,过量服用二甲双胍可导致乳酸性酸中毒,糖尿病患者出现乳酸性酸中毒首先需排除双胍相关乳酸性酸中毒[8]。Satici等 [9]报道了1例因服用30 g二甲双胍片后出现乳酸性酸中毒致死的33岁女性病例。本例患者使用胰岛素降糖,未使用双胍类药物,因此不考虑双胍相关乳酸性酸中毒。
线粒体DNA(m.3243A>G)中3243位核苷酸的A-G转换突变可导致线粒体脑肌病伴乳酸酸中毒和卒中样发作综合征(MELAS),核心症状是累及大脑皮层为主的卒中样发作以及痴呆、癫痫、乳酸性酸中毒、肌病、头痛、听力下降、糖尿病和身材矮小等[10]。MELAS发病的机制仍存在争议,一种机制是线粒体细胞病,另外一种机制是由于血浆L-精氨酸、一氧化氮(NO)和环磷酸鸟苷降低引起内皮功能障碍从而导致血管扩张障碍[11-12]。本例患者不能排除MELAS,可完善mtDNA3243基因检测,如阴性则可完善线粒体基因组测序 (NGS),但患者经济条件差未同意实施检查。
三、糖尿病酮症酸中毒合并乳酸性酸中毒机制
Kristin等(2012年)的研究提示在酮症酸中毒中,乳酸性酸中毒比传统认识的更常见,糖尿病酮症酸中毒患者中有68%的乳酸水平>2.5 mmol/L,
40%乳酸水平>4 mmol/L。酮症酸中毒患者的乳酸水平有时候极高,Lu等[13]报道乳酸水平在酮症酸中毒患者中可能高达10 mmol/L,会加重中毒和使阴离子间隙升高。酮症酸中毒并发乳酸性酸中毒可能与以下机制有关:首先,低灌注和低氧合(由于血管内体积缩小,大血管疾病和微血管病的存在,糖化血红蛋白含量增加,以及血小板功能异常而加重)导致乳酸生成过多[14]。其次,酮症酸中毒患者体内的代谢紊乱会促使乳酸水平升高,这种情况下,乳酸水平对糖尿病酮症酸中毒预后的判断,比基于实际乳酸水平对预后的判断更有利[15]。Cully等[16]的研究表明,乳酸性酸中毒是急诊科儿科酮症酸中毒患者的常见症状,单独使用血清乳酸不能作为儿童酮症酸中毒预后的预测指标。
四、治 疗
本例患者在血糖控制差合并感染情况下出现糖尿病酮症酸中毒、乳酸性酸中毒,迅速出现微循环障碍、细胞因子风暴,进一步出现MOSD,加重了乳酸性酸中毒。在予以积极补液、维持水电解质平衡、抗炎、抑制甲状腺激素分泌、应用敏感抗菌药物,根据情况应用碳酸氢钠纠正酸中毒等支持对症治疗后情况好转。在血液动力学受损的患者中,恢复组织灌注至关重要,应根据需要给予血管升压药和正性肌力药,但高乳酸血症会减弱机体对儿茶酚胺的反应,因此需要增加剂量[17]。高剂量儿茶酚胺可通过减少组织灌注或过度刺激β2肾上腺素受体而加重高乳酸血症,因此应仔细调整药物剂量[7]。本例患者有甲亢,有使用肾上腺素、异丙肾上腺素禁忌证,故选用了去甲肾上腺素加多巴酚丁胺改善组织灌注。同时应用CRRT,这对纠正糖尿病乳酸性酸中毒有一定疗效,可从根源上阻断恶性循环[18]。患者出现一种自身免疫性疾病极可能只是疾病的“冰山一角”,随着病程进展很可能相继出现其他自身免疫性疾病,早期的自身免疫相关抗体筛查对疾病的风险评估具有重要意义[18]。
五、总 结
综上所述,APS-2型并发糖尿病酮症酸中毒及乳酸性酸中毒,出现MOSD会危及患者生命。治疗的关键是阻断乳酸性酸中毒的恶性循环,抑制细胞因子风暴。在疾病早期积极筛查自身免疫相关抗体有助于临床医师对疾病进展和预后的把控。
参 考 文 献
[1] Krzymień J, Karnafel W. Lactic acidosis in patients with diabetes. Pol Arch Intern Med, 2013, 123(3): 91-97.
[2] Kamitani Y, Harada Y, Uchikura T, et al. Autoimmune polyendocrine syndrome Type3 with thyrotoxic crisis and diabetic coma. J Jpn Soc Intern Med, 2011, 100(4): 1051-1053.
[3] Benedini S, Tufano A, Passeri E, et al. Autoimmune polyendocrine syndrome 3 onset with severe ketoacidosis in a 74-year-old woman. Case Rep Endocrinol, 2015, 2015: 960615.
[4] Kluger N. New insights in autoimmune polyendocrine syndromes 1 and 2, 2015.
[5] 管明琰, 李阳阳, 刘煜. 自身免疫性多内分泌腺病综合征的临床进展. 国际内分泌代谢杂志, 2011, 31(1): 62-65.
[6] Fajgenbaum D C, June C H. Cytokine storm. N Engl J Med, 2020, 383(23): 2255-2273.
[7] Kraut J A, Madias N E. Lactic acidosis. N Engl J Med, 2014, 371(24): 2309-2319.
[8] Lá?ticová M, Ví?ek J, Zima O, et al. Metformin-associated lactic acidosis. Vnitr Lek, 2020, 66(7): 438-442.
[9] Satici M O, Algin A, Aksel G, et al. A rare case of metformin intoxication with mortal course. Medeni Med J, 2020, 35(2): 175-178.
[10] 国家卫生健康委办公厅. 罕见病诊疗指南(2019年版). 北京: 人民卫生出版社, 2019: 23.
[11] Finsterer J. Mitochondrial metabolic stroke: Phenotype and genetics of stroke-like episodes. J Neurol Sci, 2019, 400: 135-141.
[12] Ikawa M, Povalko N, Koga Y. Arginine therapy in mitochondrial myopathy, encephalopathy, lactic acidosis, and stroke-like episodes. Curr Opin Clin Nutr Metab Care, 2020, 23(1): 17-22.
[13] Lu J, Zello G A, Randell E, et al. Closing the anion gap: contribution of d-lactate to diabetic ketoacidosis. Clin Chim Acta, 2011, 412(3/4): 286-291.
[14] Feenstra R A, Kiewiet M K P, Boerma E C, et al. Lactic acidosis in diabetic ketoacidosis. Case Rep, 2014, 2014(mar20 1): bcr2014203594.
[15] Bo J, Li W, Chen Z, et al. D-lactate: a novel contributor to metabolic acidosis and high anion gap in diabetic ketoacidosis. Clin Chem, 2013, 59(9): 1406-1407.
[16] Cully M, Thompson A D, DePiero A D. Is lactic acidosis predictive of outcomes in pediatric diabetic ketoacidosis? Am J Emerg Med, 2020, 38(2): 329-332.
[17] Kraut J A, Madias N E. Treatment of acute metabolic acidosis: a pathophysiologic approach. Nat Rev Nephrol, 2012, 8(10): 589-601.
[18] 游凯斌. 连续性肾脏替代疗法治疗糖尿病乳酸酸中毒患者的效果及对患者预后的影响. 糖尿病新世界, 2020, 23(22): 181-183.
(收稿日期:2022-05-21)
(本文编辑:洪悦民)



