匡菊香,安丹丹
(1.遵义医学院附属医院 药剂科,贵州 遵义 563099;2. 遵义医学院,贵州 遵义 563099)
慢性萎缩性胃炎(CAG)是一种消化道疾病,转变为消化系统恶性肿瘤几率较大,临床诊疗表明中医药防治慢性萎缩性胃炎独具特色,能有效控制该病向肿瘤转化。舌莲胃康处方源于本院一名老中医临床上治疗慢性萎缩性胃炎的基础方,在临床实践中广泛应用并取得良好效果。由白花蛇舌草、半枝莲、白术、黄芪[1]等药材组成,该方组方合理、标本兼治、能扶正祛邪,增强机体免疫力。将舌莲胃康处方研发为胶囊剂作为医院制剂,可达到质量可控,临床使用方便快捷之目的。舌莲胃康胶囊由该处方中的药材经提取纯化、过滤、浓缩、制备干膏、粉碎、制囊和质检等过程自制而成。该方主药白花蛇舌草和半枝莲具有良好的抗肿瘤功效[2-5],其主要生物活性成分是黄酮类物质[6-10],其中含芦丁含量丰富,故以芦丁为考察指标,对该胶囊中的总黄酮进行含量测定[10-11],确保舌莲胃康胶囊剂质量的稳定。
1 仪器与试药
1.1 仪器 TU -1901双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);RE -2000旋转蒸发器(上海亚荣生化仪器厂);SHB - IIIA循环水式多用真空泵(郑州长城工贸有限公司);FW 80微型高速万能试样粉碎机(北京市永光明医疗仪器厂);手工(0号)胶囊填充板(浙江省新昌县汇普锦机械设备厂);KQ -500DE 数控超声波清洗器(昆山市超声仪器有限公司);DHA -9123A 型电热恒温鼓风干燥箱(上海精宏实验设备有限公司);Sartorius BS 224S电子天平(赛多利斯科学仪器北京有限公司);1200 UV/VIS 紫外检测器;DZKW -4型电子恒温水浴锅(上海科析试验仪器厂);80-2B 台式离心机(上海安亭科学仪器厂)。
1.2 试药 芦丁标准品(中国食品药品检定研究院,批号:100081-200907);糊精(天津市科密欧化学试剂有限公司);中药材购自重庆慧远药业有限公司;其余试剂均为分析纯。
2 舌莲胃康胶囊的制备
2.1 舌莲胃康胶囊处方 白花蛇舌草150g,半枝莲150g,黄芪 100g和白术75g等组成。
2.2 舌莲胃康药材的提取 舌莲胃康处方中各药物的有效成分具有良好的水溶性,因此选择水作为提取剂。每次加药材6倍量的水即5 700 mL,煎煮3次,每次1小时,滤去药渣合并煎液[12]。
2.3 药物溶液的纯化、干燥及胶囊的制备 将舌莲胃康药物提取液静置后,进行抽滤,滤液经过旋转蒸发仪浓缩至1∶1(干药材重量g:浓缩液体积mL)约为950 mL,按最佳纯化工艺(6倍65%的乙醇,沉淀24 h)进行处理,然后回收乙醇,低温干燥,最后放入真空干燥箱中,干燥至恒重,称量并记录[12]。将得到的干浸膏放入粉碎机中粉碎成细粉,将预先制备好的80目的三七粉混入药物干膏粉中,加入适量糊精,混匀,过80目筛后,所得药物粉末用0号手工胶囊板进行填充、压紧,制备成0号胶囊[12-13]。分别用天平称取20颗胶囊,所得胶囊平均重量为0.58g,RSD=3.8%,说明胶囊重量均匀,装量差异小。
3 舌莲胃康胶囊总黄酮的含量测定
3.1 选择测定波长 以芦丁作为考察指标,测定舌莲胃康胶囊中总黄酮的含量[14-18]。精密称取芦丁对照品25.00 mg置25 mL量瓶中,加5%亚硝酸钠溶液1 mL,摇匀,静置6 min,再加入10% 硝酸铝溶液1 mL,摇匀,继续静置6 min,加1 mol·L-1氢氧化钠溶液10 mL,摇匀,静置15 min 显色[14-15],定容至25 mL;用 60%乙醇溶液进行相同处理后作为空白溶液,在400~700 nm下扫描光谱图(见图1),测得对照品最大吸收峰为506 nm,样品按照芦丁对照品配制的方法进行相同处理,在该波长处检测也有明显的吸收峰出现,且无干扰,故选择测定波长为506 nm[15-16]。
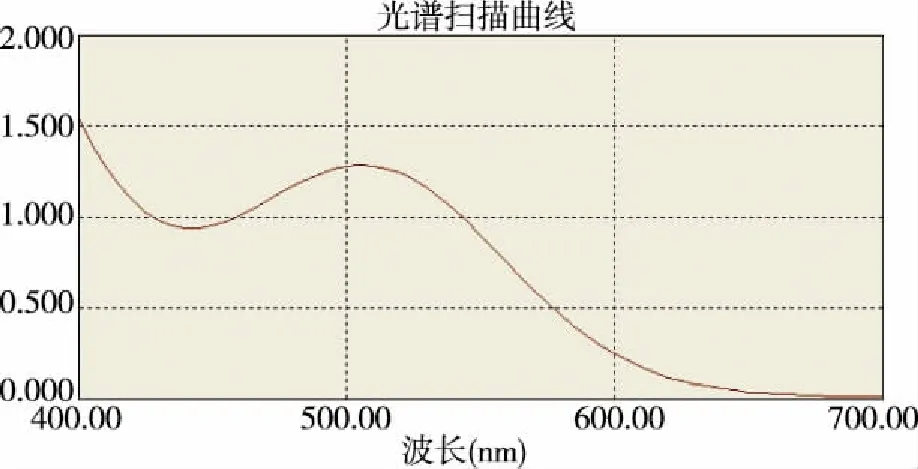
图1 芦丁标准品波谱扫描图
3.2 对照品溶液的制备 精密称取芦丁标准品25.00 mg,加60%乙醇超声溶解30 min,并该浓度的乙醇定容成25 mL,即得1 mg·mL-1的芦丁对照品溶液,备用。
3.3 供试品溶液的制备 取舌连胃康胶囊,去胶囊壳,精密称取药物粉末0.2 g,加60%乙醇25 mL后摇匀,超声提取30 min后用离心机离心10 min,取上清液用微孔滤膜过滤,收集滤液,即得供试品溶液[15-17]。
3.4 标准曲线的绘制 精密吸取芦丁标准品溶液0.5、1.0、1.5、2.0、2.5、3.0 mL分别装入6个25 mL容量瓶中,加入60%乙醇溶液定容到10 mL,按“3.1”项显色反应后,以显色后的60%乙醇溶液作空白,在506 nm处测定波长,并以吸光度为纵坐标、浓度为横坐标做标准曲线。得回归方程Y=0.0107X+ 0.0079(r=0.9984)(见图2)。结果表明,芦丁质量浓度在20~120 μg·mL-1范围内与吸光度线性关系良好。
表1芦丁对照品溶液的浓度、吸光度值(n=6)
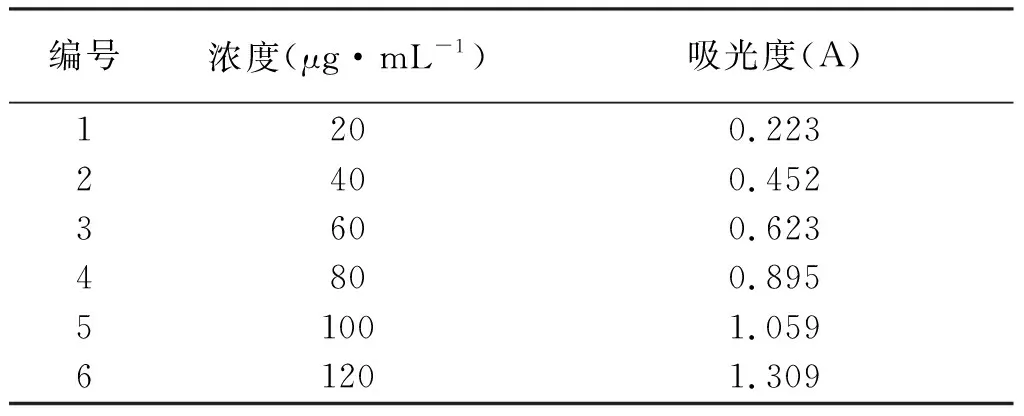
编号浓度(μg·mL-1)吸光度(A)123456204060801001200.2230.4520.6230.8951.0591.309

图2 芦丁标准曲线
3.5 精密度试验 精密吸取对照品溶液2.5mL定容于25 mL容量瓶中,显色反应后,连续测定6 次,记录吸光度,并计算RSD=0.66%(n=6) (见表2),表明仪器精密度较好。
表2芦丁对照品溶液精密度试验结果(n=6)
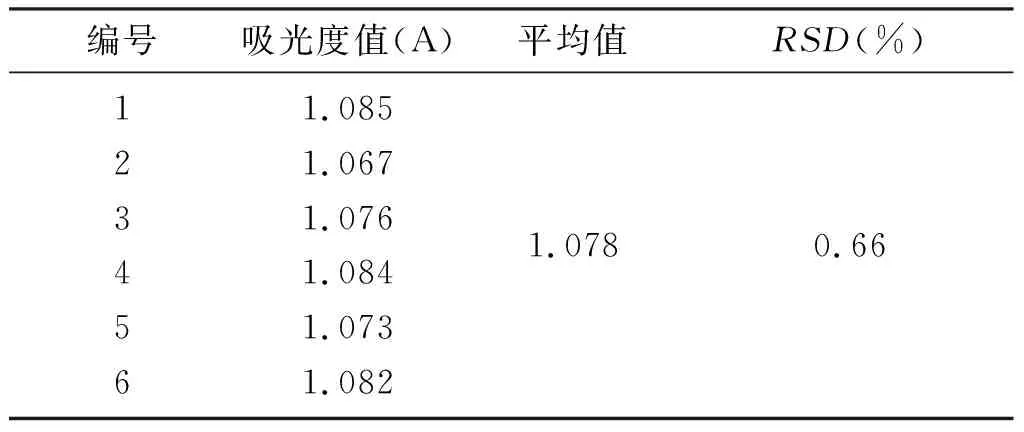
编号吸光度值(A)平均值RSD(%)1234561.0851.0671.0761.0841.0731.0821.0780.66
3.6 重复性试验 按“3.2”项下方法,制备同批次样品溶液6份,按既定方法处理后,测定并记录吸光度,计算RSD值(见表3)。
根据Y=0.0107X+0.0079,计算出该测试样品溶液浓度X=(0.254-0.0079)/0.0107=22.25 μg.mL-1。即每克粉末中芦丁的含量为22.25 μg·mL-1×25 mL÷2.5 mL×25 mL÷0.2 g=27 812.5 μg·g-1,即27.813 mg·g-1。
表3样品重复性性试验结果(n=6)

编号吸光度平均值RSD(%)1234560.2560.2580.2570.2530.2540.2470.2541.6
3.7 稳定性试验 取同一供试品溶液1份2.5 mL置于25 mL容量瓶中,显色反应后分别于0、1、2、4、6、8 h,在506 mm波长处测定其吸光度(见表4)。
表4供试品稳定性试验结果(n=6)
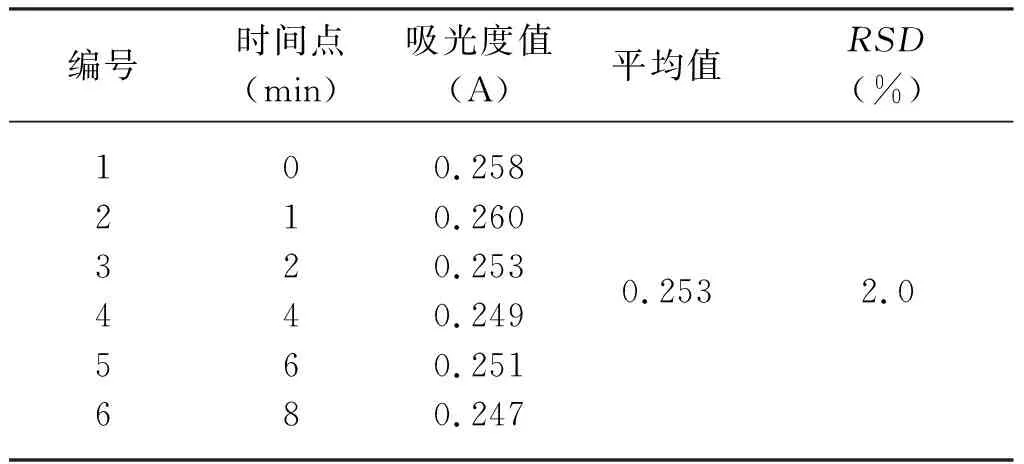
编号时间点(min)吸光度值(A)平均值RSD(%)1234560124680.2580.2600.2530.2490.2510.2470.2532.0
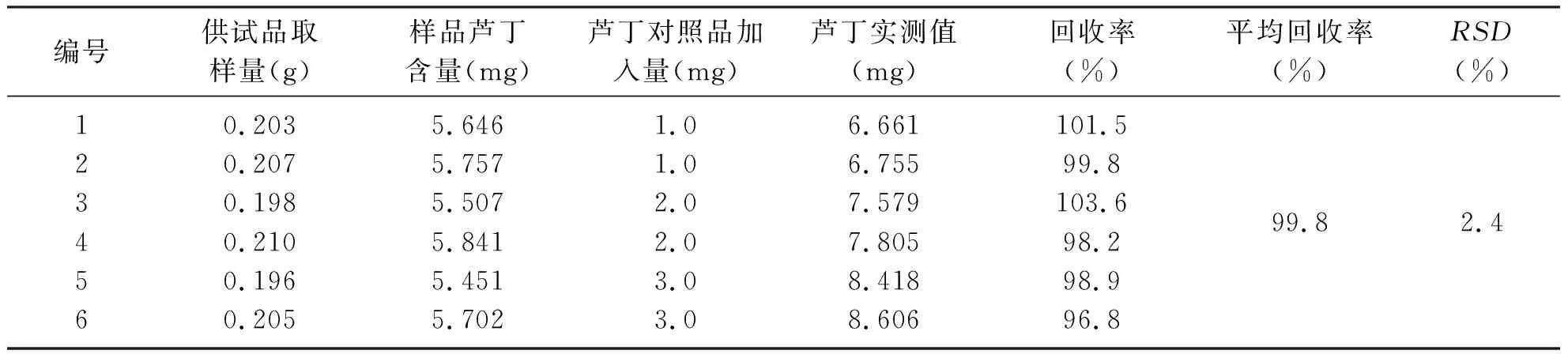
3.8 加样回收率试验 取同一批号(110127)含量27.813 mg·g-1供试品6份,按“3.2”项供试品制备方法处理,每份精密加入芦丁对照品溶液。按“3.3”项方法显色,在506 nm波长下测定,并记录吸光度值分别为0.293、0.297、0.288、0.300、0.283和0.294。根据 Y=0.0107 X+0.0079,计算出加标样品溶液浓度,从而计算出芦丁的实测值,按 [加标回收率=(加标准品样品的测定值量-样品理论含量)/标准品加入量×100%]计算回收率,结果(见表5),RSD=2.4%,说明此法有较好的回收率。
表5芦丁加样回收率测定(n=6)
编号供试品取样量(g)样品芦丁含量(mg)芦丁对照品加入量(mg)芦丁实测值(mg)回收率(%)平均回收率(%)RSD(%)1234560.2030.2070.1980.2100.1960.2055.6465.7575.5075.8415.4515.7021.01.02.02.03.03.06.6616.7557.5797.8058.4188.606101.599.8103.698.298.996.899.82.4
3.9 芦丁含量测定 取3个批次(201311-1、201311-2、201311-3)自制备用的舌莲胃康胶囊,按3.3项下方法分别配制样品溶液于双光束紫外分光光度计上各测定吸光度3次,并计算各样品的平均吸光度值,再根据平均吸光度据算RSD值为3.9%,说明该胶囊的提取纯化方法稳定、检测方法可靠。
表6样品芦丁含量测定结果(n=3)

样品吸光度(A)吸光度平均值RSD(%)201311-10.2630.2670.2650.265201311-20.2480.2430.2460.246201311-30.2470.2500.2530.2503.9
4 讨论
将舌莲胃康处方药材经过提取、纯化等工艺处理制成干浸膏细粉,再加入备用三七粉以及适量糊精,混合均匀,填充灌装成0号胶囊。经测试胶囊装量均匀、重量差异小,表明制囊工艺稳定。
以芦丁作为对照品,采用紫外分光光度法测定舌莲胃康胶囊中总黄酮的含量[14-18],通过紫外波普扫描,精密度、重复性和稳定性等方法学考察,以及对3个批次舌莲胃康胶囊样品的含量测定,结果显示各批次舌莲胃康胶囊的总黄酮含量较稳定,表明紫外分光光度法测定舌莲胃康胶囊中总黄酮的含量可行,操作简单快捷、效率高、经济实用。
[参考文献]
[1] 王立,张肖楠,卢训丛.黄芪与白花蛇舌草配伍应用举隅[J].中药与临床,2013,4(6):45-46.
[2] 望琴,倪峰.白花蛇舌草抗肿瘤有效成分的研究进展[J].海峡药学,2013,25(4):23-25.
[3] 朱立俏.白花蛇舌草的化学成分和抗肿瘤活性的研究进展[J].化工时刊,2012,26(10):37-40.
[4] 王博,林圣云.含黄酮类的中药抗癌抗肿瘤作用研究概况[J].浙江中医药大学学报,2012,36(7):838-840.
[5] 牛国晓,李洁.半枝莲抗肿瘤机制研究进展[J].肿瘤防治研究,2012,39(2):231-233.
[6] 朱大诚,高永涛,马晓鹏.白花蛇舌草化学成分的研究进展[J].江西中医学院学报,2011,(23)2:84-88.
[7] 刘志刚,颜仁梁,罗佳波.不同产地白花蛇舌草总黄酮含量比较[J].中国中医药科技,2009,16(5):382-383.
[8] 刘军海.白花蛇舌草中总黄酮微波辅助提取工艺研究[J].化工科技,2013,21(3):23-26.
[9] 谢璟,陈永刚.超声提取白花蛇舌草总黄酮工艺研究[J].医药导报,2012,31(5):640-642.
[10] 胡荣,李召辉,杨荣平.复方白花蛇舌草和半枝莲总黄酮提取工艺的研究[J].天然产物研究与开发,2013,25(10):1442-1444.
[11] 王本富,彭燕,李冬,等.HPLC测定百花蛇舌草注射液中芦丁的含量[J].华西药学杂志,2009,24(5):532-533.
[12] 匡菊香,蒲顺林,张倩茹,等.优选舌莲胃康胶囊最佳制备工艺[J].黑龙江医药,2011,24(5):740-743.
[13] 邓苏平,王晓利,李来秀.胃宁胶囊的制备与临床应用[J].中国医院药学杂志,2007,27(2):263-264.
[14] 朱华,唐桂兴,张可锋,等.基于紫外分光光度法的金花茶叶中总黄酮含量的测定[J].安徽农业科学,2010,38(9):4559-4561.
[15] 史国举.紫外-可见分光光度法测定复方红景天胶囊中总黄酮含量[J].中国医药科学,2011,14(1):45-46.
[16] 林君红,叶珍珍,崔升淼.紫外分光光度法测定康丽胶囊中总黄酮的含量[J].广东药学院学报,2012,28(6):619-622.
[17] 朱志凯,江灿,陈敏,等.大叶蛇葡萄胶囊中总黄酮含量测定的研究[J].时珍国医国药,2013,24(8):1828-1829.
[18] 姚倩,郭晓强,张良蕾,等.分光光度法测定芦丁颗粒剂中总黄酮含量[J].成都大学学报:自然科学版,2010,29(1):23-24.



