倪子惠,曹可馨,刘 晓,3,4,陈志鹏,3,4,李伟东,3,4,吴 丽,2,3,4△
(1.南京中医药大学药学院,南京 210023;2.江苏省中药药效与安全性评价重点实验室,南京 210023; 3.江苏省中药功效物质重点实验室,南京 210023;4.江苏省中药炮制重点实验室,南京 210023)
恶性肿瘤是严重威胁人类健康的一类常见病和多发病,其发病率呈逐年上升趋势。化疗是手术后、肿瘤晚期患者的主要治疗策略,虽然疗效显着,但因不良反应大、易产生耐药等原因限制了其应用。中医药完全不同于化疗、放疗、手术等西医的抗肿瘤思路,在减轻患者临床症状、减少化疗不良反应、提高患者免疫力等方面显示出明显优势,是肿瘤综合治疗的重要组成部分[1],已成为该领域的研究热点。
1 大黄虫丸抗肿瘤中医药理论研究
张仲景在其编着的《金匮要略》中,不仅对肿瘤晚期恶病质患者的临床表现进行了精准描述,并推荐使用大黄虫丸:“五劳极虚羸瘦,腹满不能饮食,食伤,忧伤,房室伤,饥伤,劳伤,经络营卫气伤,内有干血,肌肤甲错,两目黯黑,缓中补虚,大黄虫丸主之。”本方以大黄、虫为君药,水蛭、虻虫、蛴螬、桃仁和干漆为臣药,佐以黄芩、白芍、苦杏仁和地黄,再加使药甘草制成。临床以胁下癖块,触之鞕痛,推之不移,舌黯无华,脉弦细为证治要点,可用于多种肿瘤的综合治疗,即抑制肿瘤的迅速增长,改善患者的生存质量,增加肿瘤患者存活时间;与西药联合治疗,还能降低化疗药物剂量,增强化疗效果,减轻药物不良反应,延缓肿瘤耐药,可谓历经千年的抗癌名方。
1.1 “缓中补虚、攻补兼施”是大黄虫丸发挥抗肿瘤作用的重要机制
张璐在《张氏医通》中强调:“举世皆以参、芪、归、地等以补虚,仲景独以大黄虫丸补虚,苟非神圣,不能行是法也……仲景乘其元气未离,先用大黄、虫、水蛭、虻虫、蛴螬等蠕动吸血之物,佐以干漆、生地、桃仁、杏仁行去其血,略兼甘草、芍药以缓中补虚,黄芩开通瘀热,酒服以行药势,待干血行尽,然后纯行缓中补虚之功。”在《绛雪园古方选注》中,王晋三强调:“仲景治以大黄虫丸……缓中补虚者,缓舒也,绰也,指方中宽舒润血之品而言也。”尤在泾在其编着的《金匮心典》中进一步阐释:“润以濡其干,虫以动其瘀,通以去其闭,而仍以地黄、芍药、甘草和养其虚,攻血而不主专于血”,认为本方具有“攻补兼施,扶正不留瘀、祛瘀不伤正”的治病特色。
1.2 多种药对配伍的“活性化瘀”功效是大黄虫丸发挥抗癌作用的重要特色
表1显示,本方多种药物具有活血化瘀作用,具体分析本方的配伍,除了广为熟知的君臣佐使配伍理论,还蕴含了多种经典药对的配伍原理[2]。它们在功效上多以相须(虫水蛭、水蛭虻虫、熟地黄白芍)、相使(大黄虫、大黄桃仁)为用,协同增强泻热破血、逐瘀通络之功;芍药、熟地黄与桃仁、干漆、虻虫、水蛭、蛴螬、虫补泻同用,若病变证机挟有阴血亏虚,芍药、地黄即滋补阴血;若无挟阴血亏虚,则属相恶配伍,芍药、地黄即制约破血逐瘀药伤血。此外,甘草与大黄属于相恶配伍,甘草益气缓急,制约大黄泻下破血伤正[3]。诸多药对,发挥既相对独立又密切联系的功效,协同参与整方药效的发挥。
表1 大黄虫丸中蕴含的药对配伍

表1 大黄虫丸中蕴含的药对配伍
药对配伍配伍机制大黄、虫大黄苦寒攻下,荡涤肠胃实热积滞,又能入血分,破血行瘀。虫咸寒,善入血分,具破血逐瘀、消症散结之功。二药合用,相使相助,并入血分,破血逐瘀,通经止痛,消症散结之力增强,且药力峻猛而迅速,有一过不留之势。 虫、水蛭虫长于逐瘀破积,通络续筋骨。水蛭长于破血通经,二药配伍,相须为用,增强其破血逐瘀之功。大黄、桃仁桃仁破血行瘀,润燥滑肠。其得大黄能破积滑肠通便,大黄得桃仁则能破积血、逐瘀血,二药配伍相使为用,共奏活血破积、泄热解毒、攻下积滞之功。大黄、甘草大黄苦寒泄热,力猛善行,荡涤肠胃。甘草甘平,健脾和中,清火解毒。二药配伍,甘草制大黄苦寒攻下之性,降逆止呕而不伤胃气,同时助大黄泻火解毒。熟地黄、白芍熟地黄善补肝肾,填精血。白芍入肝养血补血,二药配伍,相须为用,滋阴补肾、养血补血功效显着。 白芍、甘草甘草缓急止痛,偏补阳气。白芍柔肝止痛,偏补阴血。二药互补为用,阴阳交融,气血双益。白芍、黄芩黄芩苦能燥湿,寒能清热,尤以清肺火为多用,且具解少阳清大肠之功。白芍酸寒敛阴,苦寒泄热,且能缓肠急、止痛。两药合用,一泄大肠之热,一敛阴和营之虚,可清热止痢,坚阴止痛。水蛭、虻虫 虻虫苦寒降泄,遍行经络,通利血脉,破血消症;水蛭作用缓和持久,迟缓则生血不伤,善入则坚积易破,且又可活用。二药配伍,相须为用,性慢者消积于久缓,力速者逐瘀于倾刻,能祛除真气运行难到之处的瘀血。 杏仁、桃仁 杏仁行气散结,止咳平喘。桃仁破血行瘀,合用以润燥结,破血降气。
2 大黄虫丸抗肿瘤临床及基础实验进展
2.1 肝癌
赵宁宁[4]等用大黄虫丸治疗原发性肝癌15例,显着降低血中甲胎蛋白和碱性磷酸酶水平,缩小肿瘤体积。谢美清[5]等使用大黄虫丸治疗40例经导管化疗栓塞致肝纤维化的肝癌患者,显着降低透明质酸、层黏蛋白、肝胆酸水平,提示大黄虫丸对肝癌患者介入治疗后所致的肝纤维化有一定改善作用。
2.2 肺癌
齐元富[6]等使用大黄虫丸配合化疗方案治疗30例肺癌患者,以瘤灶、症状、卡氏评分、体质量、免疫功能、血液流变学指标,内皮4项的变化情况为观察指标。结果表明,大黄虫丸具有一定的抗肺癌作用,其机制与调节细胞免疫功能、改善肿瘤高黏滞状态、调节血管内皮因子等作用有关。
曹慧慧[7]通过对Lewis荷瘤小鼠用大黄虫丸混悬液灌胃给药,发现大黄虫丸能够抑制肿瘤生长,其机制与增加胸腺指数、提高血清 IL-2水平,降低免疫抑制性Foxp3+Treg细胞水平有关。
2.3 胃癌
姜罡远[8]连续给予MKN45荷瘤小鼠大黄虫丸后发现,大黄虫丸能改善局部细胞缺氧,抑制肿瘤新生血管形成,方中的虫类药材释放大量的纤维蛋白溶酶原水解片段,能显着抑制血管内皮细胞生长。
2.4 胰腺癌
徐军[9]将18例胰腺癌患者在化疗的基础上辅以大黄虫丸进行治疗,患者的临床症状、机体免疫功能、血液高凝状况均得到改善,毒副反应也有所减轻。其机制可能与抑制血小板聚集及抗血栓形成,溶解已形成的血栓,改善血液流变性,降低血浓度,扩张血管,改善微循环,促进瘀血吸收,恢复器官功能有关。
2.5 白血病
刘丽娟[10]等对10例白血病患者在服用羟基脲的基础上加服大黄虫丸,观察临床症状和检测外周血白细胞及淋巴细胞、骨髓中淋巴细胞、血小板、血红蛋白等指标。结果提示,其作用机制可能为抑制血小板聚集、抗血栓形成和增强机体的免疫功能。
秦宝宁[11]等考察大黄虫丸含药血清对慢性粒细胞白血病系K562细胞的影响,结果提示大黄虫丸能通过抑制PI3K/AKT 信号通路的激活,将K562细胞阻滞于G0 /G1期来抑制其增殖,并能诱导细胞凋亡。
表2显示,总结目前临床及实验研究结果,临床以中西联合治疗的综合治疗方案为主,剂量较大、疗程长、效果显着;实验研究选择荷瘤鼠及肿瘤细胞系,治疗周期相对较短,以单用大黄虫丸多见,剂量偏小;大黄虫丸的抗癌作用与抑制肿瘤增殖、诱导凋亡、抑制血管生成、调节免疫等作用相关。
表2 大黄虫丸抗肿瘤临床及基础研究情况
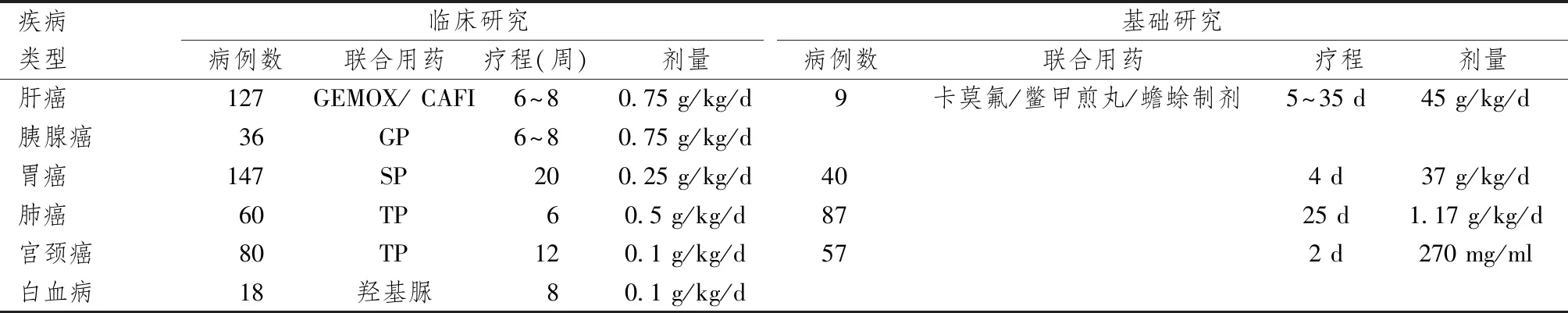
表2 大黄虫丸抗肿瘤临床及基础研究情况
疾病类型临床研究基础研究病例数联合用药疗程(周)剂量病例数联合用药疗程剂量肝癌127GEMOX/ CAFI 6~80.75 g/kg/d9卡莫氟/鳖甲煎丸/蟾蜍制剂 5~35 d45 g/kg/d胰腺癌36GP6~80.75 g/kg/d胃癌147SP200.25 g/kg/d404 d37 g/kg/d肺癌60TP 60.5 g/kg/d8725 d1.17 g/kg/d宫颈癌80TP 120.1 g/kg/d572 d270 mg/ml白血病18羟基脲80.1 g/kg/d
3 大黄虫抗肿瘤机制研究策略
3.1 缓中补虚在抗肿瘤中的作用
中医认为,“正虚”是包括肿瘤在内众多疾病发生发展的根本原因,因此“攻补兼施”是中医治疗肿瘤的重要法则,在攻逐病邪同时辅以扶正治法,这与现代医学调节机体免疫功能、抵抗疾病的策略是一致的。从免疫调节角度揭示大黄虫丸发挥“扶正治本”“补虚消痞”的抗癌功效重要方面,虽然目前尚未见系统的研究报道,但方中地黄[12]、大黄[13]、白芍[14]、桃仁[15]、甘草[16]、虫[17]、虻虫[18]等能调节机体免疫,特别是地黄、白芍激活T细胞的功效显着,值得进一步探索。
3.2 活血化瘀功效在抗肿瘤中的作用
3.2.1 抑制肿瘤血管的形成 肿瘤新血管的生成是肿瘤生长、转移的必要条件,活血化瘀中药通过干扰血管生成因子的释放及作用,抑制内皮细胞的增殖,诱生肿瘤坏死因子TNF,并提高其活性、增加内源性抑制血管生成类固醇的活性等[11,19-20]。
3.2.2 改善血液高黏滞状态、抗凝、抑制肿瘤细胞侵袭黏附 当血液黏度增加、凝血系统异常、微循环功能障碍时,癌细胞极易黏附、扩散和转移,形成微血栓,还有利于癌细胞躲避机体免疫识别系统。活血化瘀中药能促进纤维蛋白溶解,降低纤维蛋白含量,以改善血液的高凝状态;通过降低毛细血管通透性,解除微血管痉挛,抑制血小板聚集作用显着减少肿瘤细胞的滞留黏附侵袭[19];此外,活血化瘀中药能减少肿瘤细胞相关黏附分子的表达,减少肿瘤细胞对基底膜和血管内皮细胞的黏附而抑制其转移[21]。
此外,活血化瘀中药的抗肿瘤作用与其抑制端粒酶的活性[21]、调控肿瘤细胞基因表达、诱导细胞分化、凋亡[22]有关。
3.3 寒凉药物对能量代谢影响在抗肿瘤治疗中的作用
能量代谢重编程,包括有氧糖酵解、线粒体能量代谢异常等有利于肿瘤生长的能量代谢变化,是肿瘤细胞代谢的重要特征,具有明显的异质性和可变性。如肝癌细胞HepG2细胞在给予化疗药物氯乙基亚硝基脲治疗后,线粒体能量代谢被迅速激活,并呈现出显着的抗凋亡作用[23]。同样,剥夺肝癌HepG2 细胞培养液中的葡萄糖能激活线粒体呼吸链,ATP合酶β亚基表达水平增加[24]。墨西哥国立大学研发的抗癌新药Casiopeina,能够同时抑制肝癌细胞氧化磷酸化及糖酵解过程,其抗癌效果明显优于糖酵解抑制药3-溴噻吩[25]。上述成果为寒凉药物治疗肿瘤机制研究提供了有益的借鉴思路。
众所周知,药性理论是对中药作用于人体后产生多种治疗作用和效果的高度概括,是指导中医临床用药的重要依据。基于药性理论研究中药对细胞能量代谢的影响,一直是该研究领域的热点,在国家重点基础研究发展计划973计划课题等重大项目的资助下,寒性药物对细胞能量代谢的影响及机制得到了广泛的研究[26]。已有多项研究表明,多种临床常用抗肿瘤寒性中药如大黄、黄芩、苦参、栀子、黄柏、黄连等均能抑制细胞能量代谢[27-29]。



