关 媛,高燕玲,李贵庆
225000 江苏省扬州市第一人民医院内分泌科
·论著·
唑来膦酸注射液治疗高龄老年性骨质疏松的药物不良反应发生情况研究
关 媛*,高燕玲,李贵庆
225000 江苏省扬州市第一人民医院内分泌科
目的了解唑来膦酸注射液治疗高龄老年性骨质疏松的药物不良反应发生情况,并探讨高龄与药物不良反应发生的相关性。方法选取2011年3月—2016年7月在扬州市第一人民医院就诊的老年性骨质疏松患者45例,根据年龄分为老年组(年龄60~74岁,n=26)和高龄组(年龄75~88岁,n=19)。收集并比较两组患者的基线资料和药物不良反应发生情况,采用偏相关分析探讨高龄与药物不良反应发生的相关性。结果两组患者性别、BMI、骨钙素、钙离子、磷离子、碱性磷酸酶(ALP)、甲状旁腺激素(PTH)、25-羟维生素D〔25-(OH)D〕、腰椎L1-4和股骨颈骨密度、骨吸收抑制剂使用率及合并高血压、糖尿病、心脏病发生率比较,差异无统计学意义(P>0.05)。高龄组患者药物不良反应发生率低于老年组,差异有统计学意义(P<0.05)。是否发生药物不良反应患者的年龄、骨吸收抑制剂使用率比较,差异有统计学意义(P<0.05);控制骨吸收抑制剂使用情况因素后,高龄与药物不良反应发生呈负相关(P<0.05)。结论唑来膦酸注射液治疗75岁及以上高龄老年性骨质疏松患者的急性期不良反应发生率低于75岁以下患者,高龄与不良反应发生呈负相关。
骨质疏松;唑来膦酸;药物毒性;高龄
关媛,高燕玲,李贵庆.唑来膦酸注射液治疗高龄老年性骨质疏松的药物不良反应发生情况研究[J].中国全科医学,2017,20(28):3522-3526.[www.chinagp.net]
GUAN Y,GAO Y L,LI G Q.Adverse reactions to zoledronic acid injection in Chinese elders aged 75 or over with osteoporosis[J].Chinese General Practice,2017,20(28):3522-3526.
骨质疏松是一种因骨量低下和骨微结构损坏导致的以骨脆性增加、易发生骨折为特征的全身性骨病[1]。随着人口平均寿命的增长,老年性骨质疏松的发病率逐年增加,髋部或脊柱骨折是其严重并发症,严重影响了老年人的生活质量和寿命[1]。治疗老年性骨质疏松的药物包括钙剂、维生素D制剂、降钙素、二膦酸盐、甲状旁腺激素(PTH)及锶盐等。其中,二膦酸盐可以明显提高老年性骨质疏松患者的骨密度,降低髋部、脊柱及其他部位的骨折风险[2];但随着其在临床上的广泛应用,不良反应报道也逐渐增多。2005、2007、2010年,美国食品药品管理局(FDA)分别发布了二膦酸盐可增加下颌骨坏死、心房颤动、非典型股骨骨折风险的建议指南,临床上对该药不良反应的担心导致其使用率明显下降[3]。唑来膦酸是第三代二膦酸盐制剂,每年使用1次,可大大提高患者依从性[4]。本研究旨在了解唑来膦酸注射液治疗老年性骨质疏松的药物不良反应发生情况,并探讨高龄与不良反应发生的相关性,从而为唑来膦酸治疗老年性骨质疏松的耐受性和安全性研究提供参考。
1 对象与方法
1.1 研究对象 选取2011年3月—2016年7月在扬州市第一人民医院就诊的老年性骨质疏松患者45例。纳入标准:(1)符合1998年和2004年WHO发布的骨质疏松症诊断标准,经双能X线测定骨密度,低于同性别、同种族健康成年人骨峰值的2.5个及以上标准差[1];(2)年龄>60岁[1];(3)就诊期间接受唑来膦酸注射液治疗;(4)自愿参加本研究,并签署知情同意书。排除标准:(1)非老年性骨质疏松,如继发性骨质疏松、绝经后骨质疏松;(2)伴有严重心肺疾病、肝肾功能异常,不能耐受本研究治疗方法;(3)肌酐清除率≤35 ml/min,存在唑来膦酸注射液使用禁忌证;(4)近6个月内接受过二膦酸盐类抗骨质疏松药物治疗。
1.2 研究方法 根据2014年国际年龄标准的年龄划分方法[5],将纳入患者分为老年组(年龄60~74岁,n=26)和高龄组(年龄75~88岁,n=19)。收集并比较两组患者的基线资料(包括性别、年龄、BMI、合并症、骨吸收抑制剂使用情况、实验室检查结果)和不良反应发生情况,分析高龄与不良反应发生的相关性。
1.2.1 治疗方法 两组患者均服用钙尔奇D 600 mg/次、2次/d,阿法骨化醇或骨化三醇0.5 μg/次、1次/d。治疗10 d左右,静脉滴注唑来膦酸注射液(诺华制药有限公司,生产批号:S0211,规格:5 mg/100 ml),滴注时间≥15 min,用药前采用500 ml 0.9%氯化钠注射液静滴水化,用药后嘱患者多饮水(>2 000 ml/d)。如出现发热、肌痛,则采用复方对乙酰氨基酚对症治疗;部分疼痛较严重患者,在采用唑来膦酸注射液治疗前皮下注射降钙素(密钙息)50 μg/次、1次/2 d。
1.2.2 实验室检查 (1)治疗前采用美国GE公司Lunar Prodigy Advance PA+300164型双能X线骨密度仪检测腰椎L1-4、股骨颈的骨密度。(2)采用雅培C-16000生化仪,检测钙离子、磷离子(比色法,罗氏试剂盒)及碱性磷酸酶(ALP)(NPP底物-AMP缓冲液法,中生北控生物科技有限公司试剂盒);采用罗氏170化学发光仪,检测骨钙素(电化学发光法,罗氏试剂盒);采用贝克曼UniCel DxI800免疫发光仪,检测PTH(化学发光法,贝克曼试剂盒);采用MAGLUMI4000+全自动化学发光免疫分析仪,检测25-羟维生素D〔25-(OH)D〕(化学发光法,深圳新产业试剂盒)。
1.2.3 药物不良反应评价 (1)观察并记录两组患者用药后3 d内的急性不良反应发生情况,包括发热、骨痛、胸痛、头昏、心房颤动等;(2)出院1个月后,采用电话随访方式记录患者的下颌骨坏死、非典型股骨骨折情况。
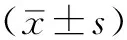
2 结果
2.1 两组患者基线资料比较 老年组患者年龄为60~74岁,平均年龄(69.3±3.8)岁;高龄组患者年龄为75~88岁,平均年龄(81.4±4.3)岁。两组患者性别、BMI、骨钙素、钙离子、磷离子、ALP、PTH、25-(OH)D、L1-4和股骨颈骨密度、骨吸收抑制剂使用率及合并高血压、糖尿病、心脏病发生率比较,差异无统计学意义(P>0.05,见表1)。
2.2 两组患者药物不良反应发生率比较 两组患者均无明显肾功能损害、下颌骨坏死、非典型股骨骨折等严重不良反应发生。老年组患者的药物不良反应发生率为61.5%(16/26),高龄组患者的药物不良反应发生率为31.6%(6/19)。两组患者药物不良反应发生率比较,差异有统计学意义(χ2=3.943,P=0.047,见表2)。
2.3 是否发生药物不良反应患者的基线资料比较 是否发生药物不良反应患者的性别、骨钙素、钙离子、L1-4和股骨颈骨密度比较,差异无统计学意义(P>0.05);年龄、骨吸收抑制剂使用率比较,差异有统计学意义(P<0.05,见表3)。
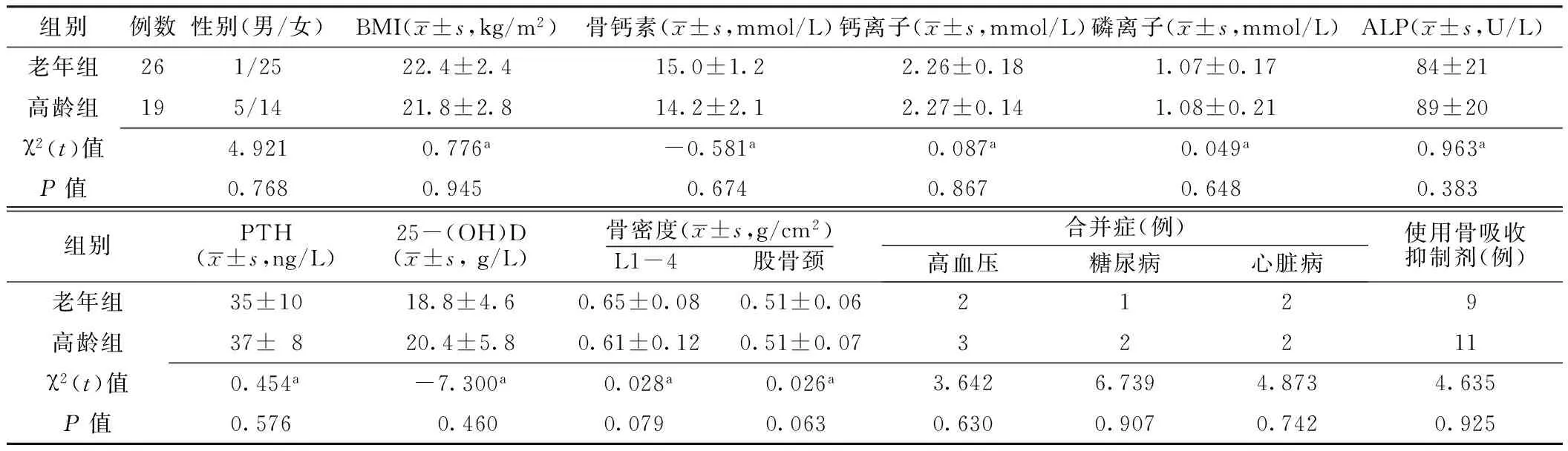
表1 两组患者基线资料比较
注:a为t值;ALP=碱性磷酸酶,PTH=甲状旁腺激素,25-(OH)D=25-羟维生素D

表3 是否发生药物不良反应患者的基线资料比较
注:a为t值
表2 两组患者药物不良反应发生情况比较(例)
Table2 Comparison of the adverse reactions to zoledronic acid injection between the two groups
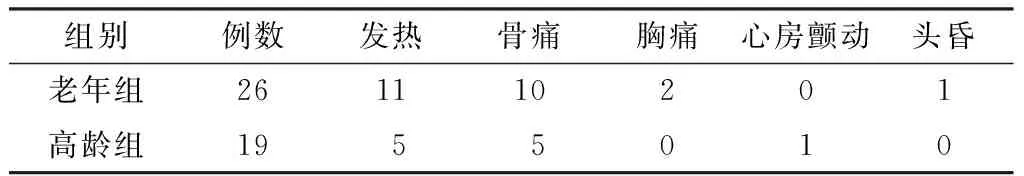
组别例数发热骨痛胸痛心房颤动头昏老年组261110201高龄组19 5 5 010
2.4 高龄与药物不良反应发生的相关性分析 控制骨吸收抑制剂使用情况因素后,对年龄和是否发生药物不良反应进行偏相关分析。结果显示,高龄与药物不良反应发生呈负相关(r=-0.223,P=0.027)。
3 讨论
3.1 唑来膦酸注射液治疗高龄老年性骨质疏松的疗效 二膦酸盐已经成为预防和治疗骨质疏松的一线药物,研究表明,二膦酸盐可以明显降低骨转换标志物、增加骨密度、减少骨折风险[6]。目前,二膦酸盐已经被广泛应用于Paget′s病、肿瘤骨转移、多发性骨髓瘤、高钙血症、骨质疏松等疾病[7]。但口服二膦酸盐的依从性较差,CRAMER等[8]的研究结果显示,虽然每周服用二膦酸盐较每日服用的依从性稍好,患者坚持治疗1年的比例从17.9%到78.0%不等,但总体依从性仍欠佳。而唑来膦酸注射液每年使用1次,可大大提高患者的依从性[4]。连续3年应用唑来膦酸5 mg治疗,可明显提高髋部和椎体骨密度、降低髋部和椎体骨折发生率[2]。SANDERSON等[9]的meta分析结果显示,二膦酸盐预防脆性骨折的效果确切,但没有证据表明其在不同性别和年龄患者中的效果存在差异。同时,也有研究结果表明,唑来膦酸注射液治疗老年性骨质疏松的疗效确切[6]。因此,唑来膦酸注射液治疗老年性骨质疏松的疗效是肯定的,对于高龄患者同样具有良好疗效。
3.2 唑来膦酸注射液的药物不良反应 近年来,FDA多次发布了二膦酸盐可以升高患者下颌骨坏死、心房颤动及非典型股骨骨折的发生风险[3]。但国外的一项meta分析结果显示,唑来膦酸在治疗绝经后骨质疏松患者中,无明显严重不良事件发生,患者具有良好的耐受性[10]。本研究中,患者出现发热、骨痛、胸痛、头晕等常见药物不良反应,多发生在用药后3 d内,为自限性,可通过应用非甾体抗炎药缓解,且高龄组患者的药物不良反应发生率低于老年组。未发现肾功能损害、下颌骨坏死、非典型股骨骨折等严重药物不良反应,仅1例患者用药后发生心房颤动,为老年组患者,该例患者既往有阵发性心房颤动病史,经美托洛尔对症治疗后恢复窦性心律。
3.2.1 发热 发热是唑来膦酸的主要药物不良反应,KOTIAN等[11]研究发现,在应用唑来膦酸注射液治疗的女性骨质疏松患者中,发热的发生率达到78%,一般集中在用药后16~72 h发生。考虑与体内的某些炎性递质,如肿瘤坏死因子α(TNF-α)、白介素(IL-6)的释放有关[12]。唑来膦酸注射液引起的急性不良反应在非日本的亚洲人群中更常见,多发于年轻、未使用非甾体抗炎药的患者,而在吸烟、合并糖尿病、既往应用过二膦酸盐药物、拉丁美洲人群中相对较少[13]。本研究中,高龄组患者的发热例数相对较少,与上述研究结果相符。
3.2.2 肾损伤 二膦酸盐可能会导致肾损伤发生,其发病机制为肾前性氮质血症和药物导致的急性肾小管坏死[14]。既往有肾脏病病史、高龄、应用其他肾毒性药物(尤其是利尿剂)的患者是二膦酸盐导致肾损害的高危人群,而治疗前后的大量水化会明显降低肾脏损害的发生率[15]。同时,静脉输注速度过快也是导致肾损害的原因之一[16]。研究表明,对于肌酐清除率>35 ml/min的患者,唑来膦酸注射液引起的肾损害发生率较低[17];但也有研究证明,唑来膦酸注射液与安慰剂在肾毒性方面无差异[18]。本研究中并无发生肾损害的病例,这可能与应用唑来膦酸注射液治疗前后的水化、减慢输液速度及用药前患者的筛选有关。因此,建议在应用唑来膦酸注射液前常规应用0.9%氯化钠溶液500 ml,治疗后嘱患者大量饮水(>2 000 ml/d),输注时间>15 min。另外,在应用唑来膦酸注射液治疗前,充分评估患者肾功能十分重要,对于肌酐清除率<35 ml/min的患者应避免使用。
3.2.3 下颌骨坏死、心房颤动、非典型股骨骨折 下颌骨坏死是罕见及毁灭性的并发症,既往牙周疾病病史、吸烟、饮酒、类固醇激素使用是其发生的高危因素[19]。二膦酸盐抑制了破骨细胞的活性,导致下颌骨缺血坏死[20]。目前尚没有证据证明二膦酸盐会增加心血管事件的发生风险,但有研究显示其可以小幅度增加患者的心房颤动发生风险[21]。本研究中的心房颤动患者通过对症治疗后,很快恢复窦性心律。非典型股骨骨折的特点是在缺乏明显创伤的情况下发生,位置局限于股骨转子下方和股骨颈区域的横形或斜形非粉碎性骨折,伴有内侧尖锐凸起[22]。BLACK等[2]的研究发现,非典型股骨骨折的发生率较低,约为2.3·万人-1·年-1。本研究随访过程中,未发现上述罕见药物不良反应,也未发现皮肤红疹、皮肤瘙痒、局部疼痛、低钙血症等药物不良反应。
3.3 高龄与药物不良反应发生的相关性 本研究中,高龄组患者的药物不良反应发生率明显低于老年组,未发现严重药物不良反应。这可能是因为年龄低的患者体内有较高水平的γδ T淋巴细胞,而高龄患者的免疫功能偏低[23]。既往研究结果显示,应用唑来膦酸注射液治疗前,应用骨吸收抑制剂、钙剂、维生素D是唑来膦酸注射液发生药物不良反应的保护性因素[24]。在控制了骨吸收抑制剂使用情况这一因素后,进行偏相关分析,结果显示,高龄与药物不良反应发生呈负相关。
综上所述,唑来膦酸注射液对75岁及以上的高龄老年性骨质疏松患者具有良好的安全性和耐受性,且可通过实施保护性措施减少其药物不良反应的发生。但本研究也存在一定的局限性,包括样本量较小、未对合并用药进行分析、未监测肌酐和血钾等生化指标、未对患者生活质量改善情况进行评价、缺乏长期药物不良反应监测等,因此所得结论尚有待进一步研究的证实。
作者贡献:关媛负责文章的构思与设计、研究的实施与可行性分析、数据整理、统计学处理、结果的分析与解释、论文的撰写与修订,对文章整体负责,监督管理;高燕玲负责数据收集;李贵庆负责英文的修订、文章的质量控制及审校。
本文无利益冲突。
[1]中华医学会骨质疏松和骨矿盐局部分会.原发性骨质疏松症诊治指南(2011年)[J].中华骨质疏松和骨矿盐疾病杂志,2011,4(1):2-17.DOI:10.3969/j.isn.1674-2591.2011.01.002.
[2]BLACK D,DELMAS P,EASTELL R,et al.Once-yearly zoledronic acid for treatment of postmenopausal osteoporosis[J].N Engl J Med,2007,356(18):1809-1822.DOI:10.1056/NEJMoa067312.
[3]KIM S C,KIM D H,MOGUN H,et al.Impact of the US food and drug administration′s safety-related announcements on the use of bisphosphonates after hip fracture[J].J Bone Miner Res,2016,31(8):1536-1540.DOI:10.1002/jbmr.2832.
[4]李国新,袁忠治,温健,等.口服及静脉应用双磷酸盐治疗绝经后的骨质疏松临床研究[J].中国骨质疏松杂志,2013,19(9):988-990.DOI:10.3969/j.issn.1006-7108.2013.09.025.
LI G X,YUAN Z Z,WEN J,et al.Clinical study of oral administration or intravenous injection of bisphosphonate for the treatment of postmenopausal osteoporosis[J].Chinese Journal of Osteoporosis,2013,19(9):988-990.DOI:10.3969/j.issn.1006-7108.2013.09.025.
[5]人类年龄段划分新标准[J].现代养生,2005,21(9):16.
New standards for the division of human age[J].Modern Regimen,2005,21(9):16.
[6]袁元杏,李青,梅治,等.唑来膦酸钠治疗老年骨质疏松98例[J].中国老年学杂志,2012,32(11):2395-2396.DOI:10.3969/j.issn.1005-9202.2012.11.094.
YUAN Y X,LI Q,MEI Z,et al.Clinical effect of zoledronic acid in the treatment of 98 cases senile osteoporosis[J].Chinese Journal of Gerontology,2012,32(11):2395-2396.DOI:10.3969/j.issn.1005-9202.2012.11.094.
[7]FAVUS M J.Bisphosphonates for osteoporosis[J].New England Journal of Medicine,2010,363(21):2027-2035.DOI:10.1056/NEJMct1004903.
[8]CRAMER J A,GOLD D T,SILVERMAN S L,et al.A systematic review of persistence and compliance with bisphosphonates for osteoporosis[J].Osteoporosis International,2007,18(8):1023-1031.DOI:10.1007/s00198-006-0322-8.
[9]SANDERSON J,MARTYN-ST JAMES M,STEVENS J,et al.Clinical effectiveness of bisphosphonates for the prevention of fragility fractures:a systematic review and network meta-analysis[J].Bone,2016,89(7):52-58.DOI:10.1016/j.bone.2016.05.013.
[10]WANG C.Efficacy and safety of zoledronic acid for treatment of postmenopausal osteoporosis:a meta-analysis of randomized controlled trials[J].American Journal of Therapeutics,2017,24(5):e544-552.DOI:10.1097/MJT.0000000000000415.
[11]KOTIAN P,BOLOOR A,SREENIVASAN S.Study of adverse effect profile of parenteral zoledronic acid in female patients with osteoporosis[J].Journal of Clinical & Diagnostic Research,2016,10(1):4-6.DOI:10.7860/JCDR/2016/17061.7021.
[12]DICUONZO G,VINCENZI B,SANTINI D,et al.Fever after zoledronic acid administration is due to increase in TNF-alpha and IL-6[J].J Interferon Cytokine Res,2003,23(11):649-654.DOI:10.1089/107999003322558782.
[13]REID I,GAMBLE G,MESENBRINK P,et al.Characterization of and risk factors for the acute-phase response after zoledronic acid[J].J Clin Endocrinol Metab,2010,95(9):4380-4387.DOI:10.1210/jc.2010-0597.
[14]PERAZELLA M,MARKOWITZ G.Bisphosphonate nephrotoxicity[J].Kidney Int,2008,74(11):1385-1393.DOI:10.1038/ki.2008.356.
[15]ORWOLL E,BLANK J B,BARRETT-CONNOR E,et al.Design and baseline characteristics of the osteoporotic fractures in men(MrOS) study——a large observational study of the determinants of fracture in older men[J].Contemp Clin Trials,2005,26(5):569-585.DOI:10.1016/j.cct.2005.05.006.
[16]BERENSON J,HIRSCHBERG R.Safety and convenience of a 15-minute infusion of zoledronic acid[J].Oncologist,2009,9(3):319-329.DOI:10.1634/theoncologist.10-5-309.
[17]FDA.Safety alerts for human medical products-reclast(zoledronic acid):drug safety communication-new contraindication and updated warning on kidney impairment[EB/OL].[2017-01-09].https://www.fda.gov/Safety/MedWatch/SafetyInformation/Safe-
tyAlertsforHumanMedicalProducts/ucm270464.htm.
[18]LYLES K,COLON-EMERIC C,MAGAZINER J,et al.Zoledronic acid and clinical fractures and mortality after hip fracture[J].N Engl J Med,2007,357(18):1799-1809.DOI:10.1056/NEJMoa074941.
[19]KHOSLA S,BURR D,CAULEY J,et al.Bisphosphonate-associated osteonecrosis of the jaw:report of a task force of the American Society for Bone and Mineral Research[J].J Bone Miner Res,2007,22(10):1479-1491.DOI:10.1359/jbmr.0707onj.
[20]MARX R,SAWATARI Y,FORTIN M,et al.Bisphosphonate-induced exposed bone(osteonecrosis/osteopetrosis) of the jaws:risk factors,recognition,prevention,and treatment[J].J Oral Maxillofac Surg,2005,63(11):1567-1575.DOI:10.1016/j.joms.2005.07.010.
[21]KIM D H,ROGERS J R,FULCHINO L A,et al.Bisphosphonates and risk of cardiovascular events:a meta-analysis[J].PLoS One,2015,10(4):e0122646.DOI:10.1371/journal.pone.0122646.
[22]SHANE E,BURR D,EBELING P,et al.Atypical sub trochanteric and diaphyseal femoral fractures:report of a task force of the American Society for Bone and Mineral Research[J].J Bone Miner Res,2010,25(11):2267-2294.
[23]ROSSINI M,ADAMI S,VIAPIANA O,et al.Circulating γδ T cells and the risk of acute-phase response after zoledronic acid administration[J].J Bone Miner Res,2012,27(1):227-230.DOI:10.1002/jbmr.521.
[24]赵蕾.唑来膦酸注射液治疗绝经后骨质疏松症所致不良反应及相关因素分析[J].药物不良反应杂志,2016,18(2):116-120.DOI:10.3760/cma.j.issn.1008-5734.2016.02.008.
ZHAO L.Analysis of adverse reactions and related factor of zoledronic acid injection in postmenopausal osteoporosis patients[J].Adverse Drug Reactions Journal,2016,18(2):116-120.DOI:10.3760/cma.j.issn.1008-5734.2016.02.008.
AdverseReactionstoZoledronicAcidInjectioninChineseEldersAged75orOverwithOsteoporosis
GUANYuan*,GAOYan-ling,LIGui-qing
DepartmentofEndocrinology,YangzhouFirstPeople′sHospital,Yangzhou225000,China
ObjectiveTo investigate the adverse reactions to zoledronic acid injection in Chinese elders with osteoporosis,and based on this,to evaluate the correlation between advanced age(≥75 years) and the occurrence of adverse drug reactions.MethodsForty-five consecutive elderly patients with osteoporosis who were treated with zoledronic acid injection in Yangzhou First People′s Hospital from March 2011 to July 2016 were enrolled and divided into elderly group(aged 60-74 years,n=26) and very elderly group(aged 75-88 years,n=19).The baseline data and information about adverse reactions to zoledronic acid injection of both groups were collected.Partial correlation analysis was performed to find the correlation between advanced age and the incidence of adverse drug reactions.ResultsSex distribution,values of BMI,osteocalcin,calcium ion,phosphorus ion,alkaline phosphatase(ALP),parathyroid hormone(PTH),25-hydroxyvitamin D〔25-(OH)D〕 and bone mineral density of lumbar L1-4 and femoral neck,utilization rate of bone resorption inhibitors,incidence of hypertension,diabetes mellitus and heart disease did not differ significantly between the two groups(P>0.05).Adverse reactions to zoledronic acid injection occurred significantly less in very elderly group than in the elderly group(P<0.05).The age and utilization rate of bone resorption inhibitors differed significantly between patients with adverse reactions to zoledronic acid injection and those without(P<0.05).After adjusting for the use of bone resorption inhibitors,advanced age presented a negative correlation with the incidence of adverse drug reactions(P<0.05).ConclusionPatients aged 75 or over with acute exacerbation of osteoporosis are less likely to have adverse reactions to zoledronic acid injection compared with those less than 75 years old.Advanced age is negatively correlated with the incidence of adverse drug reactions.
Osteoporosis;Zoledronic acid;Drug toxicity;Advanced age
*通信作者:关媛,主治医师;E-mail:lgq333gy@163.com
R 681
A
10.3969/j.issn.1007-9572.2017.28.014
*Correspondingauthor:GUANYuan,Attendingphysician;E-mail:lgq333gy@163.com
2017-05-04;
2017-09-05)
(本文编辑:王凤微)



