胡巍 蔡思敏 廖盛欢



【摘要】 目的:探讨贝伐珠单抗联合化疗对非小细胞肺癌(NSCLC)患者免疫功能及生活质量的影响。方法:选择2017年11月-2020年1月就诊于本院的90例NSCLC患者。按随机数字表法将患者分为观察组和对照组,各45例。对照组行常规GP化疗方案治疗,观察组在对照组基础上加用贝伐珠单抗注射液治疗。比较两组临床疗效、免疫功能、生活质量、不良反应发生情况。结果:观察组治疗总有效率高于对照组,差异有统计学意义(P<0.05)。治疗后,观察组CD3、CD4、CD8、CD4/CD8均高于对照组,差异均有统计学意义(P<0.05)。治疗后,两组KPS评分均高于治疗前,且观察组高于对照组,差异均有统计学意义(P<0.05)。观察组血小板减少、肝功能损害、恶心/呕吐发生率均低于对照组,差异均有统计学意义(P<0.05);两组白细胞减少、骨髓抑制发生率比较,差异均无统计学意义(P>0.05)。结论:贝伐珠单抗联合化疗治疗NSCLC患者能够有效控制肿瘤生长,提高免疫功能和生活质量,减少不良反应发生,安全性较高。
【关键词】 非小细胞肺癌 贝伐珠单抗 免疫功能 化疗 生活质量
Effect of Bevacizumab Combined with Chemotherapy on Immune Function and Quality of Life in Patients with Non-small Cell Lung Cancer/HU Wei, CAI Simin, LIAO Shenghuan. //Medical Innovation of China, 2021, 18(23): 0-063
[Abstract] Objective: To investigate the effects of Bevacizumab combined with chemotherapy on immune function and quality of life in patients with non-small cell lung cancer (NSCLC). Method: A total of 90 patients with NSCLC admitted to our hospital from November 2017 to January 2020 were selected. The patients were divided into observation group and control group by random number table method, 45 cases in each group. The control group received conventional GP chemotherapy, the observation group was treated with Bevacizumab Injection on the basis of the control group. Clinical efficacy, immune function, quality of life and the occurrence of adverse reactions were compared between the two groups. Result: The total effective rate of the observation group was higher than that of the control group, the difference was statistically significant (P<0.05). After treatment, CD3+, CD4+, CD8+ and CD4+/CD8+ in the observation group were higher than those in the control group, the differences were statistically significant (P<0.05). After treatment, KPS scores in both groups were higher than those before treatment, and the observation group was higher than that of the control group, the differences were statistically significant (P<0.05). The incidence of thrombocytopenia, liver function damage and nausea/vomiting in the observation group were lower than those in the control group, the differences were statistically significant (P<0.05). The incidence of leukopenia and bone marrow suppression were compared between the two groups, there were no significant differences (P>0.05). Conclusion: Bevacizumab combined with chemotherapy in the treatment of NSCLC patients can effectively control tumor growth, improve immune function and quality of life, reduce adverse reactions and have high safety.
[Key words] Non-small cell lung cancer Bevacizumab Immune function Chemotherapy Quality of life
First-author’s address: Xinyu Second Hospital, Xinyu 338000, China
doi:10.3969/j.issn.1674-4985.2021.23.015
非小细胞肺癌(NSCLC)发病率约占肺癌的85%,因患者早期无典型性临床表现,不易受到重视,约57%患者就诊时病情已发展至ⅢB或Ⅳ期,错失手术治疗最佳时机,预后较差,死亡率较高[1-3]。针对此类患者临床多使用化疗方案治疗,其中GP方案较为常见,能够杀死或去除肿瘤组织,控制疾病发展,延长患者生存期,但仍有部分患者经GP化疗方案治疗后病情仍会进展,难以达到理想的治疗效果[4-5]。贝伐珠单抗属于重组抗人VEGF单克隆抗体,能高亲和力结合血管内皮生长因子(VEGF),减弱、阻止VEGF及其受体结合,发挥抗肿瘤作用,逐渐被应用于临床。本研究分析贝伐珠单抗联合化疗对NSCLC患者免疫功能及生活质量的影响,为临床治疗提供参考依据,现报道如下。
1 资料与方法
1.1 一般资料 选择2017年11月-2020年1月就诊于本院的90例NSCLC患者。(1)纳入标准:CT、MRI等检查确诊为NSCLC;血常规正常;肝肾功能正常;预计生存期>3个月;认知功能正常;拒绝或无法实施手术治疗者。(2)排除标准:拒绝化疗;精神疾患;进展期肾脏疾病;骨质增生;存在化疗禁忌证;过敏体质;血液系统疾病。按随机数字表法将患者分为观察组和对照组,各45例。患者或家属签署知情同意书,本研究经医学伦理委员会审核批准。
1.2 方法 对照组行常规GP化疗方案治疗,即在250 mL的0.9%氯化钠中加入1.0 g/m2注射用盐酸吉西他滨[生产厂家:江苏豪森药业集团有限公司,批准文号:国药准字H20030104,规格:0.2 g(以CHFNO计)]行静脉滴注,30 min内滴完,第1、8天给药;静脉滴注注射用顺铂(生产厂家:齐鲁制药有限公司,批准文号:国药准字H20023461,规格:20 mg)30 mg/m,第2~4天给药,1次/d。观察组在此基础上加用贝伐珠单抗注射液(生产厂家:德国Roche Diagnostics GmbH,批准文号:注册证号S20170036,规格:400 mg︰16 mL)治疗,在100 mL 0.9%氯化钠溶液中加入7.5 mg/kg贝伐珠单抗行静脉滴注,第1天化疗后给药。两组患者均连续治疗6个周期,每个周期21 d。
1.3 观察指标及判定标准 (1)比较两组临床疗效,完全缓解(CR):病灶消失,肿瘤标记物检测未出现异常,维持4周以上;部分缓解(PR):病灶肿瘤最大直径减小≥50%,肿瘤标记物检测未出现异常,维持4周以上;稳定(SD):病灶肿瘤最大直径减小>30%且<50%,无新肿瘤病灶出现;进展(PD):出现新病灶,或病灶肿瘤最大径增加>20%。总有效=CR+PR+SD。(2)比较两组治疗前后免疫功能水平,治疗前、治疗6个周期后,采集两组患者5 mL空腹肘静脉血,离心10 min,3 000 r/min,获取上清液,使用BD公司的FACSCanto型流式细胞仪测定CD3、CD8、CD4、CD4/CD8。(3)比较两组治疗前后生活质量评分,以卡氏功能状态(KPS)评分评估两组治疗前、治疗6个周期后的生活质量,包括是否能自如活动、疾病严重程度等,总分为100分,分值高低与生存质量呈正相关。(4)比较两组不良反应发生情况,包括血小板减少、白细胞减少、肝功能损害、恶心/呕吐、骨髓抑制[6]。
1.4 统计学处理 采用SPSS 21.0软件对所得数据进行统计分析,计量资料用(x±s)表示,组间比较采用独立样本t检验,组内比较采用配对t检验;计数资料以率(%)表示,比较采用χ检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较 观察组男26例,女19例;年龄36~78岁,平均(56.31±2.16)岁;病程1~7年,平均(3.42±0.32)年;疾病类型:鳞癌15例,腺癌20例,腺磷癌10例。对照组男23例,女22例;年龄34~77岁,平均(56.26±2.09)岁;病程2~6年,平均(3.37±0.28)年;疾病类型:鳞癌17例,腺癌22例,腺磷癌6例。两组一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
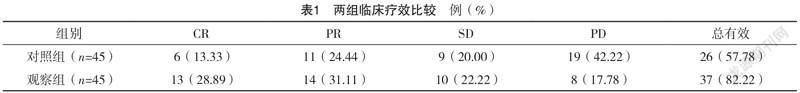
2.2 两组临床疗效比较 观察组治疗总有效率高于对照组,差异有统计学意义(χ=6.402,P=0.011),见表1。
2.3 两组治疗前后免疫功能水平比较 治疗前,两组免疫功能各指标比较,差异均无统计学意义(P>0.05);治疗后,观察组CD3+、CD4+、CD8+、CD4+/CD8+均高于对照组,差异均有统计学意义(P<0.05)。见表2。
2.4 两组治疗前后生活质量评分比较 治疗前,两组KPS评分比较,差异无统计学意义(P>0.05);治疗后,两组KPS评分均高于治疗前,且观察组高于对照组,差异均有统计学意义(P<0.05)。见表3。
2.5 两组不良反应发生情况比较 观察组血小板减少、肝功能损害、恶心/呕吐发生率均低于对照组,差异均有统计学意义(P<0.05);两组白细胞减少、骨髓抑制发生率比较,差异均无统计学意义(P>0.05)。见表4。
3 讨论
NSCLC发生与环境污染、吸烟、遗传、电离辐射等密切相关,是我国恶性肿瘤致死的首要原因,多数患者就诊时已发展至中晚期,5年生存率较低[7-8]。化疗是治疗NSCLC的常用全身性治疗手段,化疗药物能阻止癌细胞浸润、增殖和转移,能有效缓解患者临床症状,延缓病情发展,延长患者生存期[9-12]。但化疗时,化疗药物无明显的选择性,杀灭癌细胞的同时,易损伤机体正常细胞,引起药物性不良反应,影响疾病转归[13]。
VEGF在新生血管形成中起到促进作用,其能特异性结合血管内皮细胞,调控肿瘤细胞增殖、生成和迁移等过程[14-15]。贝伐珠单抗能够竞争性结合VEGF受体,造成内源性VEGF生物活性丧失,拮抗新生血管生成和细胞的有丝分裂,抑制肿瘤转移、生长[16-17]。本研究结果显示,治疗后,观察组治疗总有效率、CD3、CD4、CD8、CD4/CD8、KPS评分均较对照组高,肝功能损害、血小板减少、恶心/呕吐发生率均较对照组低,提示化疗联合贝伐珠单抗治疗能够增强治疗效果,增强免疫功能,减少不良反应发生,提高生活质量。贝伐珠单抗属于抗肿瘤血管生成药物,作用机制包括以下几点:(1)定点清除肿瘤血管系统,避免癌组织转移至身体其他部位,同时能特异性结合VEGF,阻止其与血管内皮细胞表面受体相互作用,抑制新生血管形成和内皮细胞增殖,切断血行转移,发挥抗肿瘤作用。(2)能够促进血管发展退变,对癌组织内血管生长发挥抑制作用,促进癌组织萎缩,提高抗癌作用,使患者生存期延长[18]。(3)能够关闭癌组织血管内皮窗口和细胞间隙,使血管通透性降低,缓解组织间压力,促使化疗药物快速通过血管,强化化疗药物效果,增强抗肿瘤作用[19-20]。(4)可降低化疗的毒副反应,改善机体免疫功能与抗病能力。
综上所述,NSCLC患者行贝伐珠单抗联合化疗治疗具有良好的安全性,能够有效控制肿瘤生长,提高免疫功能和生活质量。
参考文献
[1]蒋友国,王韬渊,刘军涛,等.贝伐珠单抗联合埃克替尼治疗中晚期非小细胞肺癌的临床研究[J].现代药物与临床,2018,33(12):3259-3263.
[2]杨学宁,林俊涛.贝伐珠单抗在可手术非小细胞肺癌术后辅助治疗中的作用[J].循证医学,2018,18(4):233-235.
[3]邢若,王鹏,刘玉豪.贝伐珠单抗辅助常规化疗治疗非小细胞肺癌的临床研究[J].中国临床药理学杂志,2019,35(1):17-19.
[4]梅雪,王豪勋,马军.VEGFR2基因多态性与贝伐珠单抗联合化疗一线治疗晚期非小细胞肺癌患者疗效的关系[J].肿瘤,2018,38(11):1055-1063.
[5]陶虹,郭丽丽,吴洪波,等.贝伐珠单抗联合化疗对复治晚期非鳞非小细胞肺癌患者的疗效及预后分析[J].中国肿瘤临床,2018,45(10):503-507.
[6]石磊,蒋继宗,刘青旭,等.贝伐珠单抗联合治疗晚期非小细胞肺癌的疗效和安全性[J].医药导报,2018,37(5):554-558.
[7]孙丽艳,张军,葛星剑,等.贝伐珠单抗联合TP化疗方案治疗晚期非鳞癌非小细胞肺癌的临床研究[J].临床和实验医学杂志,2019,18(15):1631-1634.
[8]王旭,高晓玲,李建强.贝伐珠单抗联合化疗治疗表皮生长因子受体无突变非小细胞肺癌的临床研究[J].中国药物与临床,2018,18(8):92-94.
[9]樊慧杰,袁静,吴晶晶,等.VEGFR2多态性对贝伐珠单抗联合化疗一线治疗晚期非小细胞肺癌患者效果及安全性的影响[J].中华医学杂志,2019,99(2):99-104.
[10]郑宣轩,王慧娟,张国伟,等.二线及以上应用贝伐珠单抗联合化疗治疗晚期非鳞非小细胞肺癌的疗效及安全性观察[J].中国肺癌杂志,2018,21(7):513-518.
[11]赵仔君,谷晓媛,张为强,等.贝伐珠单抗联合阿法替尼治疗非小细胞肺癌临床疗效观察[J].海南医学院学报,2019,25(2):55-58.
[12]杨海波,王翠鳌,王晓光,等.贝伐珠单抗治疗老年NSCLC合并脑转移的疗效分析[J].西南国防医药,2018,28(7):69-71.
[13]孙志佳,杜楠,祁楠,等.胸腔灌注吉西他滨联合贝伐珠单抗治疗恶性胸腔积液的疗效分析[J].解放军医学院学报,2018,39(4):275-278.
[14]柯华,刘咏梅,陈维永,等.贝伐珠单抗联合化疗对肺腺癌患者恶性胸腔积液的疗效及安全性研究[J].中国临床保健杂志,2019,22(4):484-487.
[15]魏智民,张维强,高峰,等.淋巴细胞亚群对晚期非小细胞肺癌患者化疗效果及远期生存的影响[J].中国医学科学院学报,2017,39(3):371-376.
[16]谭宝利,尚东,张进儒,等.鸦胆子油乳、艾迪注射液对非小细胞肺癌化疗效果的影响[J].现代生物医学进展,2017,17(17):141-144.
[17]曾焘.FOLFOX方案与贝伐珠单抗共同治疗晚期结肠癌的临床研究[J].中国医学创新,2019,16(8):48-51.
[18]薛艳峰.紫杉醇/卡铂联合贝伐珠单抗治疗培美曲塞失败/耐药后的肺腺癌10例效果观察[J].中国药物与临床,2017,17(3):389-392.
[19]张亚年.康艾注射液联合贝伐珠单抗和DP方案治疗非小细胞肺癌的临床研究[J].现代药物与临床,2019,34(12):3690-3695.
[20]苏爱江,孙永琨,毛爱琴.贝伐珠单抗联合化疗对晚期结直肠癌的疗效及免疫功能的影响[J].现代消化及介入诊疗,2018,23(2):61-63.
(收稿日期:2020-09-21) (本文编辑:姬思雨)



