崔艳玲,汪丽静,孙丽敏,孙雪莲,赵溶冰
大庆油田总医院集团脑血管医院,黑龙江大庆 163000
动脉硬化引起脑血管腔内狭窄是引起脑血栓形成的主要原因,而颅内血管狭窄以亚洲人最常见,尤其在大脑中动脉,颅内动脉狭窄是缺血性卒中的一个重要原因,而大脑中动脉狭窄的患者每年卒中的发生率为7.0%~17.7%[1]。大约10%的缺血性卒中及8%的短暂性脑缺血发作(TIA)是由此引起的,而黄种人这个比例可能还要更高。长期以来抗血小板、调脂等内科疗法一直被认为是治疗缺血性脑卒中的有效的治疗方法。然而,单纯药物治疗对于症状性大脑中动脉狭窄的患者,疗效十分有限[2]。笔者根据2005年1月~2009年6月收治的症状性大脑中动脉狭窄的患者60例进行临床特点分析,旨在探索和提高临床防治效果,现总结如下:
1 资料与方法
1.1 一般资料
收集2005年1月~2009年6月在我院住院的脑梗死患者60例,所有病例均经TCD检查诊断为大脑中动脉狭窄,研究对象都进行前瞻性连续登记。其中,男38例,女22例;年龄最小44岁,最大81岁,平均(62.2±11.5)岁。随机选择我院同期确诊的无症状性大脑中动脉狭窄的脑梗死患者60例作为对照组,其中,男33例,女27例;年龄最小43岁,最大79岁,平均(61.5±10.1)岁。两组患者年龄、性别等一般情况差异无统计学意义(P>0.05),具有可比性。
1.2 检查方法
所用TCD仪为DWL公司的X4型或T型仪,采用标准的探查方法。TCD诊断大脑中动脉狭窄的标准:局部平均血流速度≥120 cm/s,伴有轻微血流杂音;或局部平均血流速度≥100 cm/s,伴有明显的血流杂音和频谱紊乱。均需除外代偿性血流速度增快。对于经TCD发现大脑中动脉狭窄的患者,询问其病史,既往有脑血管病(包括脑梗死、短暂性脑缺血发作、脑出血)病史者排除。对于符合条件者,统计其有无高血压病、糖尿病、肥胖、高脂血症、脑血管病家族史等,并行头颅CT检查,观察有无异常,资料齐全者纳入统计。
1.3 评价标准[3]
TCD是一种基于证据的、很有价值的预测MCA狭窄预后的诊断方法。MCA狭窄的进展程度、狭窄数目、严重程度及与颅外动脉狭窄并存,是MCA狭窄复发性缺血性事件的预测因子。具体证据水平及推荐级别如下:①在目前的临床实践中,TCD是一种预测MCA狭窄预后的很有价值的研究工具1b级证据4个,A级推荐。②MCA狭窄的进展程度是新的缺血性事件的独立预测因子1b级证据2个,A级推荐。③颅内大动脉闭塞性病变的数目为新的脑血管性事件独立的预测因子1b级证据1个,B级推荐。④颅内、外动脉狭窄并存的患者发生脑血管性事件的危险性很高1b级证据1个,B级推荐。⑤症状性MCA高度狭窄容易发生脑血管事件(4级证据1个,C级推荐)。
1.4 统计学方法
数据以均数±标准差(x±s)表示。采用t检验和χ2检验,P<0.05表示差异有统计学意义。
2 结果
本组60例大脑中动脉狭窄患者,主要临床表现为头昏(26 例)、头痛(24 例)、头沉(18 例)、记忆力下降(13 例)、反应迟钝(12例)等。头颅CT检查发现患者病变部位无差异(χ2=1.862,P>0.05)。与普通人群相比,脑血管病家族史、高血压、糖尿病的患病比例明显增高(χ2=2.185,P>0.01)。
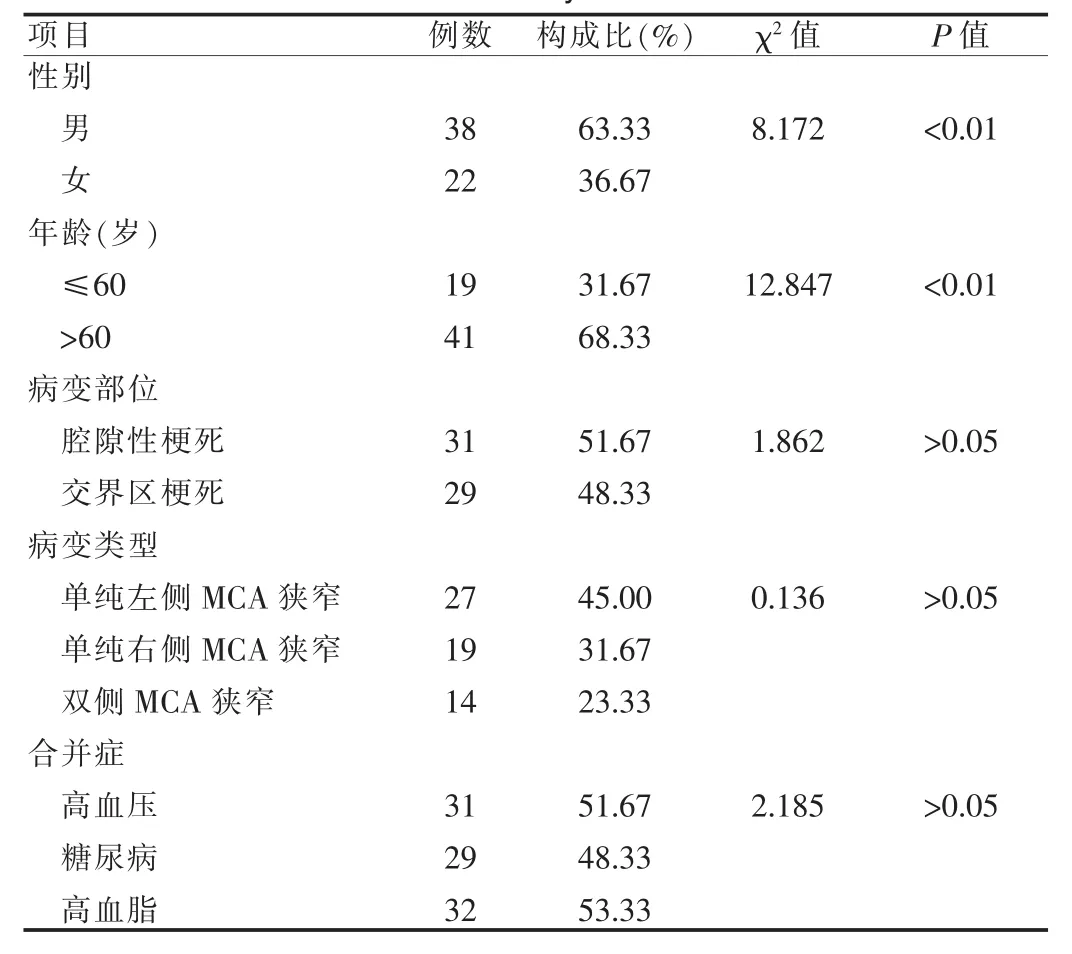
表1 60例大脑中动脉狭窄患者的临床分析Tab.1 Clinical analysis of the date of 60 patients with cerebrum median artery narrow
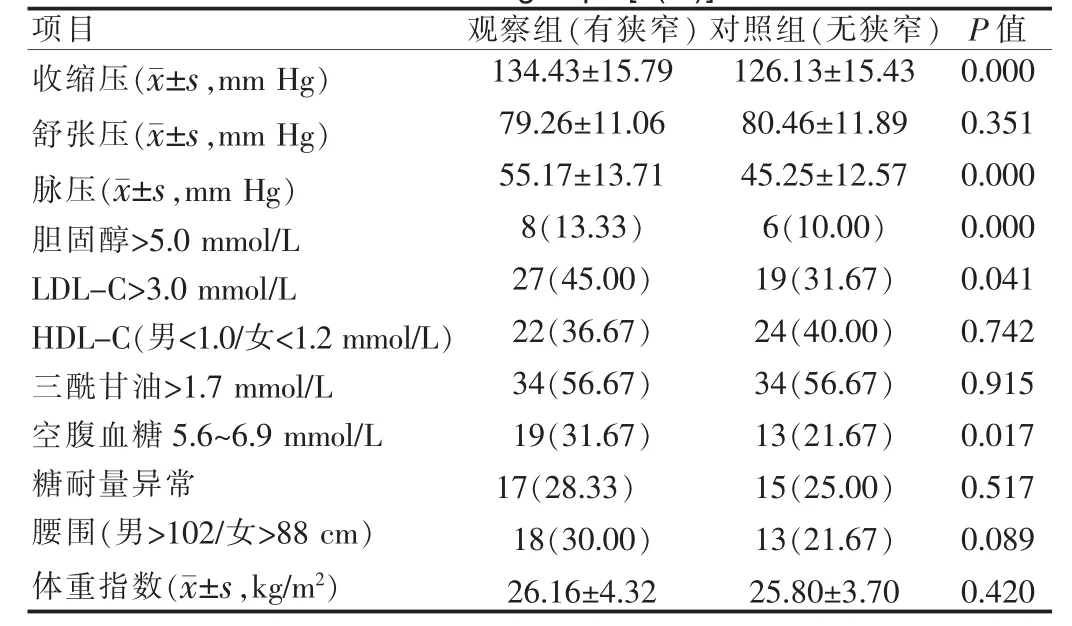
表2 两组患者心血管危险因素比较[n(%)]Tab.2 Comparison of cardiovascular hazard factor in the two groups[n(%)]
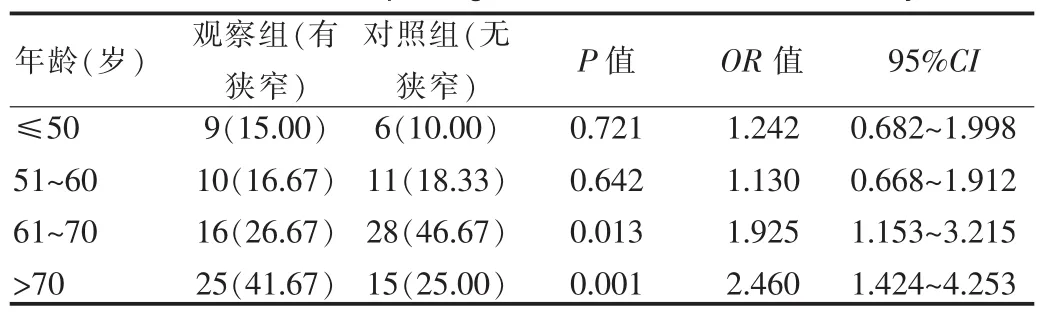
表3 年龄与大脑中动脉狭窄临床关系Tab.3 Clinical relationship of age and cerebrum median artery narrow
3 讨论
颅内大动脉狭窄是卒中的一个重要原因。颅内大动脉狭窄常见的诊断方法有:数字减影血管造影(DSA)、磁共振血管造影(MRA)、计算机断层扫描血管造影(CTA)及经颅多普勒超声(TCD)等。这些方法独立或联合使用已经使颅内大动脉狭窄诊断率大大提高,但这些诊断方法、治疗方法及预后的相关性尚不明确。
本文通过检索相关参考文献,主要调查大脑中动脉(MCA)或颅内动脉的不同诊断方法与预后相关性的文献。研究颅内大动脉狭窄的预后及临床特点,评价方法包括复发性脑缺血性事件及其他的血管性事件,如缺血性心脏病或死亡。本研究结果显示,颅内大动脉狭窄发生频率有随着年龄增长而增加的趋势。性别是否为颅内大动脉狭窄的独立危险因素尚不清楚。其他研究也未显示出性别为颅内颈动脉狭窄的独立的危险因素。高血压是颅内动脉狭窄的独立危险因素各家报道不一。国内一系列研究表明高血压是颅内动脉狭窄的独立危险因素[4]。国外研究证实了糖尿病为颅内大动脉狭窄的独立危险因素,本研究也支持上述观点。糖尿病促进颅内大动脉粥样硬化性狭窄的机制可能是通过多种不同的途径[5]。其中,与胰岛素抵抗相关的纤维蛋白溶解活性的降低可能是最有意义的途径之一[6]。颅内大动脉粥样硬化最严重者往往是那些糖尿病合并脂蛋白(α)水平增高的患者,并推测两种危险因素可能协同促进了颅内动脉粥样硬化的形成,两者均可导致纤维蛋白溶解活性系统的紊乱并进一步导致内皮细胞损伤促进血栓形成,而导致狭窄[7]。最近一项研究显示,LDL水平增高是颅内动脉粥样硬化的独立危险因素。血清脂蛋白(α)的水平与颅内大动脉狭窄的数量呈正相关(r=0.22)。国内的一项研究则显示,高密度脂蛋白胆固醇(HDLC)水平对脑动脉的保护因素,HDL-C的水平越高,患脑动脉狭窄的可能性越小,而并未发现总胆固醇、低密度脂蛋白胆固醇(LDL)、三酰甘油(TG)与脑动脉狭窄的关系[8]。
本研究结果显示,MCA的狭窄进程是其同侧缺血性事件或任何原因死亡的独立预测因子。颅内大动脉病变的数目可以预测复发性血管性事件或死亡。颅内大动脉狭窄的患者,发生脑血管性事件及死亡的危险性较大。我们通过应用血管造影的研究探讨了颅内动脉狭窄的进展程度与预后的相关性,因样本数较少,无法进行统计学分析。另外,颅内动脉狭窄患者,其狭窄病灶呈动态演变过程。由于某些患者颅内狭窄可能是一个良性过程,有自行减轻的可能,因此,在评价新的治疗方法前应设立对照组进行大量的临床对比分析,确立治疗标准。
[1]高山,黄家星,黄一宁,等.颅内大动脉狭窄的检查方法和流行病学调查[J].中国医学科学院院报,2003,25(2):96-100.
[2]卢宝全,孙泽民,马建国.交界区脑梗塞与脑动脉狭窄或闭塞的关系[J].临床神经病学杂志,2003,16(6):333-335.
[3]王伊龙,王春学,王拥军.颅内动脉粥样硬化性狭窄的流行病学[J].国外医学:脑血管疾病分册,2005,13(6):418-421.
[4]李慎茂,缪中荣,凌锋,等.颈内动脉狭窄83例的血管内支架治疗[J].中华普通外科杂志,2002,17(6):6.
[5]顾东风,吴锡桂.中国成年人高血压患病率、知晓率、治疗和控制状况[J].中华预防医学杂志,2003,37(2):84-89.
[6]刘国荣,李月春,张京芬.缺血性脑血管病颅内动脉狭窄的危险因素[J].中华神经科杂志,2003,36(5):363-365.
[7]姜卫剑.颅内动脉粥样硬化,脑缺血和梗死的病理生理机制[J].BNC频道,2005,3(2):17-19.
[8]华扬.实用颈动脉与颅脑血管超声诊断学[J].北京:科学出版社,2002.



