吴天昊 孙文婷 赵彦伟 徐 林 李军平
0 引言
随着航天科技的发展,临近空间飞行器飞行时间更长、速度更快,这对材料的耐高温性能提出了更高的要求[1]。ZrC具有高熔点、高硬度的性能特点,是超高温陶瓷中具有重要应用的材料之一。采用Solgel法制备ZrC,其粉体可达纳米级别,纯度较高,控制因素易调节。据文献报道,Sol-gel法制备ZrC的锆源主要为正丙醇锆[2-5]和氯氧化锆[6-8]等,碳源主要为酚醛树脂以及蔗糖、果糖等小分子。近年来也出现了诸如乙酰基丙酮酸锆等[9-12]新的锆前驱体。Sol-gel法制备ZrC通常选取一种或几种溶剂,将碳源溶解,并且控制锆源的水解,形成溶胶凝胶,经碳热还原后,ZrC的粒径在50~300 nm。
本文采用正丙醇锆作锆源,蔗糖作碳源,乙酸作为络合剂和溶剂,并且加入一定比例的水以提高溶胶的凝胶时间,对制得的溶胶凝胶及其碳热还原产物进行了表征,为PIP法制备碳化锆基复合材料提供技术支撑。
1 实验
1.1 实验原料
正丙醇锆 Zr(OPr)4,70wt%正丙醇溶液,蔗糖 C12H22O11,分析纯,均为上海阿拉丁生化科技股份有限公司;冰醋酸AcOH分析纯,北京蓝弋化工产品有限责任公司;去离子水H2O自产。
1.2 实验过程
取 50 mL 醋酸与 0、5、10、15、20 mL 去离子水混合组成溶剂。水体积分数(φ)分别为0,10%,20%,30%以及40%。
蔗糖中的碳最终会完全转化为单质碳,正丙醇锆中的锆原子为锆的唯一来源,碳原子和锆原子的摩尔比(C/Zrmol)由此确定。取3 g蔗糖加入40 mL醋酸与XmL去离子水的混合液中,经油浴加热至80℃,连续搅拌至蔗糖完全溶解,得到蔗糖溶液;另取10 mL的醋酸放入小烧杯,称取正丙醇锆加入其中得到正丙醇锆溶液。随后在80℃下将正丙醇锆溶液倒入持续搅拌的蔗糖溶液中并继续油浴加热5 min,自然冷却得到前驱体溶液或湿凝胶。
若得到前驱体溶液,则将其陈化24 h后,置于鼓风干燥箱中在80℃下蒸发掉多余溶剂,得到湿凝胶。在鼓风干燥箱中90℃下加热得到干凝胶。随后对得到的前驱体干凝胶先在氧化铝管式炉中Ar氛围下以5℃/min加热至800℃并保温1 h,待其冷却至室温后,在碳管炉中Ar氛围以5℃/min加热至1 200℃,随后以3℃/min加热至设定温度并保温1 h,得到黑色粉末。
采用DSC-TGA对得到的干凝胶进行热分析,采用X射线衍射对黑色粉末进行物相分析,对得到的溶胶凝胶及黑色粉末的形貌以及粒径大小使用SEM及动态光散射进行观测。
2 结果及讨论
2.1 含水量对前驱体的影响
AcOH可以与Zr(OPr)4发生螯合,形成一种螯合物。首先在正丙醇锆溶液中发生OAc基团取替OPr,反应如下所示:

在式(1)中产生的锆螯合物 Zr(OAc)2(OPr)2接下来有可能会发生以下两种竞争反应:

式中,X为C12H14O3。
反应式中如果水较少,则式(3)反应占据主导,从而较快形成 HO—Zr—[O—X—O—Zr]n—OH 溶胶,胶粒不断长大导致迅速凝胶。反之如果水如果大量存在,则式(4)反应占据主导,Zr无法和蔗糖形成化学键,而是水解形成无机 ZrO2前驱体—O—Zr—O—,当溶液中组份达到一定极限时生成白色沉淀[13]。 而如果水的量适中,则式(3)与式(4)竞争进行,胶体既不会像无机锆前驱体一样迅速水解,也不会像有机锆溶胶一样迅速长大,胶粒尺寸适中即n值大小适中,可以延长其凝胶时间。
设定C/Zrmol=7,实验中发现,凝胶时间随着含水量的增加而提高。当φ=0、10%时,将正丙醇锆溶液倒入持续搅拌的溶液蔗糖中后,体系在1~2 s内迅速凝胶,这是因为(3)反应占据主导、胶粒迅速长大所致;而当φ=20%、30%时,可以得到稳定的、有丁达尔效应的前驱体溶液。φ=20%时,丁达尔效应更为明显,制得的前驱体溶液可以在室温下保存1年以上而不变质。φ=30%时,丁达尔效应较弱,前驱体溶液在存放至100~150 d时失去稳定性,产生了白色沉淀。φ=40%时,体系在2 min内产生白色沉淀。
对得到的溶胶凝胶用SEM观察,结果如图1所示,溶胶凝胶的形态随含水量的不同而发生变化:φ=0时,凝胶呈现胶块状,胶粒很大,且大小不均匀;当φ=10%时,凝胶尺寸较φ=0时小,其线性长大形成三维网状结构导致凝胶;当φ=20%时,溶胶主要以胶粒形式存在,虽然偶有胶体线性长大,但并不会导致体系凝胶;而当φ=30%时,溶胶粒径进一步减小,溶胶粒径均匀,平均粒径为140 nm,并且无胶体的线性长大。
对形成的溶胶与凝胶经稀释分散后,利用动态光散射法(Dynamic Light Scattering,DLS)测定其粒径,结果如图2所示。可以看出,溶胶凝胶的颗粒大小随着含水量的提高先减小;当水进一步增加时,胶粒大小反而增大。


图1 不同含水量溶胶凝胶的SEM照片Fig.1 SEM images of various water contentsol-gel precursor samples
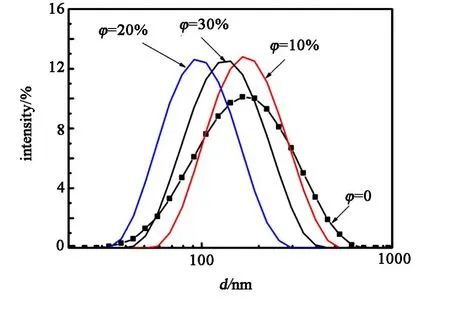
图2 不同含水量溶胶凝胶的粒径动态光散射图谱Fig.2 DLS images of various water content sol-gel precursor samples
对φ=20%、C/Zrmol=7的溶胶,经室温下陈化1 d后,测定其Zeta电位,其测试结果如图3所示,Zeta电位峰主要集中在18.7 mV,对于纳米级微粒,当其Zeta电位的绝对值超过15 mV时,可认为其存在较为稳定。

图3 φ=20%、C/Zrmol=7的溶胶Zeta电位测试结果Fig.3 Zeta potential of sol precursor with φ=20%and C/Zrmol=7
2.2 前驱体热处理分析
选取C/Zrmol=7,φ=20%的干凝胶为例,对其从室温到1 400℃做DSC-TGA测试,结果如图4所示。可以观察到3个主要失重阶段,分别是150~240、240~550和1 150~1 350℃,第一个阶段可能是与锆络合的羧酸等小分子的分解逸散[14]以及前驱体中结合水的完全分解。270~550℃阶段,主要发生的反应是蔗糖的分解。而在 1 150~1 350℃,主要是 C还原ZrO2,放出CO所致。在DSC曲线上也有对应的3个吸热峰,以1 271℃处最为明显,与DTG峰值相互对应。

图4 C/Zrmol=7,φ=20%时,干凝胶的 DSC-TGA 结果Fig.4 DSC-TGA curves of xerogel precursor with C /Zrmol= 7 and φ = 20%
选取φ=20%,C/Zrmol=7的前驱体粉末,分别加热到 1 300、1 400、1 500、1 600、1 700℃热处理并保温1 h,对热处理后的粉末进行XRD衍射分析,其XRD分析结果如图5所示。可以看出,φ=20%,C/Zrmol=7的前驱体在1 300~1 600℃时,粉末中主要存在t-ZrO2(PDF#88-1007)而到 1 700℃时,粉末完全转变为ZrC(PDF#73-0477)。这说明此前驱体粉末中的t-ZrO2在1 700℃时才可以被碳热还原为ZrC。

图 5 φ=20%,C/Zrmol=7的前驱体不同温度处理后的粉末XRD图谱Fig.5 XRD patterns of powder treated under different temperatureswith φ = 20%and C /Zrmol= 7
2.3 碳锆摩尔比对粉末物相组成的影响
取 φ=20%为例,C/Zrmol=5、6、7 时,在1 700℃保温1 h制备的粉体XRD图谱如图6所示。

图6 φ=20%、T=1 700℃时不同碳锆摩尔比的XRD图谱Fig.6 XRD patterns of different C/Zr ratio powder treated under 1700℃ when φ=20%
当C/Zrmol=5和6时,产物组成较为复杂,由ZrC(PDF#73-0477)、m-ZrO2(PDF#83-0939)、t-ZrO2(PDF#88-1007)组成。 当 C/Zrmol=7 时,最终的碳热还原产物为纯相ZrC粉末。制备纯ZrC相的C/Zrmol超过了理论值3。此实验说明在小剂量反应下,碳需要被额外多加[4]。
2.4 加水量对碳热还原产物的影响
选取 C/Zrmol=7,当 φ=0、10%、20%、30%时,将前驱体分别在1 700℃处理1 h,其XRD图谱如图7所示。可知,其碳热还原产物均为 ZrC(PDF#73-0477),加水量不会影响产物的相组成。

图 7 C/Zrmol=7、T=1 700℃时不同含水量的碳热还原产物XRD图谱Fig.7 XRD patterns of powder treated under 1700℃ with different water content while C/Zrmol= 7
对经过热处理的粉末粒径利用SEM观察(图8),并利用动态光散射法测定其粉体粒径,光散射强度与粒径的关系如图9所示。

图8 不同含水量的碳热还原产物的SEM照片Fig.8 SEM images of powder treated under 1700℃ with different water content

图9 1 700℃处理后的粉末动态光散射图谱Fig.9 DLS images of powder treated under 1700℃with different water content
从图8中可以看出,粉末粒径分布均为纳米级,相对粒径大小相差无几。,φ=20%、30%时,其粉末粒径整体较φ=0、10%时较小。φ=0时,其粉体较易发生团聚,导致其在5 000 nm附近出现一个光散射峰。φ=10%、20%、30%时,其平均粒径为240 nm。
3 结论
以正丙醇锆为锆源、蔗糖为碳源、乙酸作为分散剂制备碳化锆前驱体,其结果如下:
(1)当 C/Zrmol=7 时,含水量 φ=20%,体系会保持溶胶状态,Zeta电位约为18.7 mV,此溶胶状态可稳定存放1年以上,并且制得的溶胶胶粒较小,有利于浸渍碳纤维等制备复合材料。加水较少(φ为0或10%)则会迅速凝胶,加水过多(φ=30%)时,虽然其胶粒更小,但是其在室温下保存100 d左右会失稳产生白色沉淀。加入φ=40%水时,体系迅速产生白色沉淀。
(2)当 C/Zrmol=7、T=1 700℃时,前驱体经碳热还原可以制得较纯的纳米级ZrC粉末。
(3)当 C/Zrmol=7、T=1 700℃时,含水量的多少并不会改变制得粉末的物相。最终得到的ZrC粉末粒径随着加水量的增加而减小。当φ=20%时,制得的ZrC平均粉末粒径为240 nm。
参考文献
[1]郭强强,冯志海,周延春.超高温陶瓷的研究进展[J].宇航材料工艺,2015,45(5):1-13.
[2]刘春轩,陈建勋,苏哲安,等.碳化锆陶瓷先驱体裂解机理及PIP法制备C/C-ZrC复合材料[J].中国有色金属学报(英文版), 2014(6):1779-1784.
[3] GHELICH R,MEHDINAVAZ A R,TORKNIK F S,et al.Low temperature carbothermal reduction synthesis of ZrC nano⁃fibers via cyclized electrospun PVP/Zr(OPr)4hybrid[J].Inter⁃national Journal of Applied Ceramic Technology, 2016, 13(2):352-358.
[4] DOLLÉ M, GOSSET D, BOGICEVIC C, et al.Synthe⁃sis of nanosized zirconium carbide by a sol-gel route[J].Journal of the European Ceramic Society, 2007, 27(4):2061-2067.
[5] XIE J, FU Z, WANG Y, et al.Synthesis of nanosized zirconium carbide powders by a combinational method of sol-gel and pulse current heating [J].Journal of the European Ceramic Society, 2014, 34(1):13.e1-13.e7.
[6] XUW, ZHOU Y, HUANG D, et al.Synthesis and py⁃rolysis evolution of glucose-derived hydrothermal precursor for nanosized zirconium carbide[J].Ceramics International, 2016,42(9):10655-10663.
[7] Cao Y, LIF, ZHANG H, et al.Low-temperature prep⁃aration of ZrC powders using a combined sol-gel and microwave carbothermal reduction method [J].Journal-Ceramic Society Ja⁃pan,2016, 124(11):1171-1174.
[8] YAN Y, HUANG Z, LIU X, et al.Carbothermal syn⁃thesis of ultra-fine zirconium carbide powders using inorganic pre⁃cursors via sol-gel method [J].Journal of Sol-Gel Science and Technology, 2007, 44(1):81-85.
[9] CUIX M, NAM Y S, LEE J Y, et al.Fabrication of zir⁃conium carbide(ZrC) ultra-thin fibers by electrospinning [J].Materials Letters, 2008, V62(12-13): 1961-1964.
[10] WU H, ZHANG T, LI Y.Fabrication of biomorphic ZrC/C ceramics by sol-gel and carbothermal reduction processing[J].Ceramics International, 2015, 109(10):480-492.
[11] TAO X, QIU W, LI H, et al.Synthesis of nanosized zirconium carbide from preceramic polymers by the facile one-pot reaction [J].Polymers for Advanced Technologies, 2010, 21(4):300-304.
[12] TAO X, WEI X Y, CHEN Q, et al.Synthesis, char⁃acterization and thermal behaviour of new preceramic polymers for zirconium carbide[J].Advances in Applied Ceramics, 2013, 112(5):301-305.
[13] CLEARFIELD A.The mechanism of hydrolytic poly⁃merization of zirconyl solutions [J].Journal of Materials Re⁃search, 1990, 5(1): 161-162.
[14]杨旭堃,刘辉,迟伟东,等.溶胶-凝胶法制备锆先驱体改性C/C复合材料[J].北京化工大学学报(自然科学版),2012, 39(5):42-48.



