王 萍
伊马替尼治疗新诊断与重组人干扰素α2b治疗失败的慢性髓性白血病患者的效果分析
王萍
【摘要】目的 探索伊马替尼对于新诊断与重组人干扰素α2b治疗失败的慢性随行白血病患者的治疗价值。方法 随机选取在我院收治的慢性髓性白血病患者127例作为本次研究的对象,其中有78例患者为新诊断患者,49例患者为重组人干扰素α2b治疗失败的患者,根据患者的类型分成A组与B组,其中A组患者为新诊断组,B组为重组人干扰素α2b治疗失败组,对两组患者均采用伊马替尼治疗,对比分析治疗效果。结果 治疗6个月和治疗12个月,A组患者的细胞遗传学完全反应率、部分反应率均高于B组。在毒副作用上,A组患者的腹泻、血细胞减少、贫血的发生率均低于B组,差异具有统计学意义,P<0.05。结论 在慢性髓性白血病患者的临床治疗中,重组人干扰素α2b治疗失败患者用伊马替尼治疗的效果低于新诊断患者的治疗效果,且毒副作用发生率更高,临床上对于CML治疗应及早使用伊马替尼治疗,而对于重组人干扰素α2b治疗失败或是出现耐药性的患者应及早采用伊马替尼治疗,控制病情。
【关键词】伊马替尼;慢性髓性白血病;重组人干扰素α2b;毒副作用
作者单位:河南省驻马店市中心医院血液内科,河南 驻马店 463000
慢性髓性白血病(CML)是一种恶性疾病,是起源于造血干细胞、粒细胞过度增殖的一种疾病,大部分患者在慢性期被诊断[1]。伊马替尼的发明为CML的治疗带来新的方向和理念,有效提高了患者的生存质量,不少指南都将伊马替尼作为CML慢性期治疗的一线药物[2]。为分析伊马替尼对于CML治疗的临床价值,我院特开展本次研究,现报道如下。
1 资料与方法
1.1基础资料
随机选取我院2013年1月~2014年12月收治的慢性髓性白血病患者127例作为本研究的对象,其中78例为新诊断患者,设为A组,男43例,女35例,年龄在19~55岁,平均年龄(43.9±12.1)岁;血小板计数为95×109/L~780×109/L,平均血小板计数(478±121)×109/L;49例患者为重组人干扰素α2b治疗失败的患者,设为B组,其中男27例,女22例,年龄22~56岁,平均年龄(44.5±12.3)岁;血小板计数为90×109/L~805×109/L,平均血小板计数(482±118)×109/L;两组患者的基础资料对比,差异无统计学意义,P>0.05,具有可比性。
1.2治疗方法
两组患者均给予伊马替尼(生产企业:Novartis Pharma Stein AG;批准文号:H20100264)治疗,每日口服400 mg,根据患者的病情改善或加重适当调整药物剂量,最大剂量不得超过600 mg/d,当患者的中性粒细胞计数<1×109/L或者血小板计数<30×109/L,则可减药或是暂时停药。治疗期间进行患者肝功能的检测,若发现出现肝脏毒性反应,则停药;若治疗期间发现患者的中性粒细胞计数或是血小板计数持续减少超过30 d,则停药。
1.3观察指标
观察两组患者的细胞遗传学反应以及毒副作用。其中细胞遗传学反应的评估标准:完全反应(CCyR):治疗后患者的Ph染色体阳性细胞全部消失。部分反应(PCyR):Ph染色体阳性细胞所占比例在1%~35%。次要反应(mCyR):Ph染色体阳性细胞占36%~65%。微小反应(miniCyR):Ph染色体阳性细胞所占比例在66%~95%。无反应(NCyR):治疗后Ph染色体阳性细胞所占比例在95%~100%。
1.4统计分析
采用SPSS 19.0软件对本研究中的相关数据资料进行对比分析处理,对计数资料对比采用χ2检验,P<0.05表示具有统计学意义。
2 结果
2.1两组患者的细胞遗传学反应对比
治疗6个月后的细胞遗传学反应见表1所示,在完全反应和部分反应上,A组所占比例均高于B组,P<0.05;在治疗12个月后,A组患者的完全反应率、部分反应率依然均高于B组,P <0.05,见表2。
2.2两组患者的毒副作用对比
从表3中可知,治疗期间,在腹泻、血细胞减少、贫血发生率上,A组患者的发生率低于B组,P<0.05。
3 讨论
慢性髓性白血病(CML)是一种恶性骨髓增殖性肿瘤,其基本特点就是骨髓中性粒系的恶性克隆衍生,直接影响到骨髓的正常造血功能,并且会在血液中累积。该病最早是1960年Nowell和Hungerford报道,他们发现CML患者体内的一个小于g组的染色体,并将其命名为费城染色体[3]。随着研究的深入,医学界发现95%以上的CML患者体内Ph染色体为阳性,故而临床上讲Ph染色体阳性作为CML的重要诊断标准之一[4]。
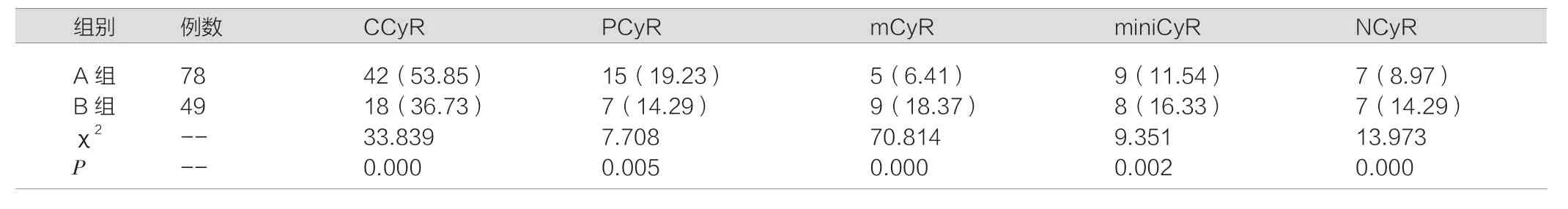
表1 两组患者治疗6个月后的细胞遗传学反应结果对比[n(%)]
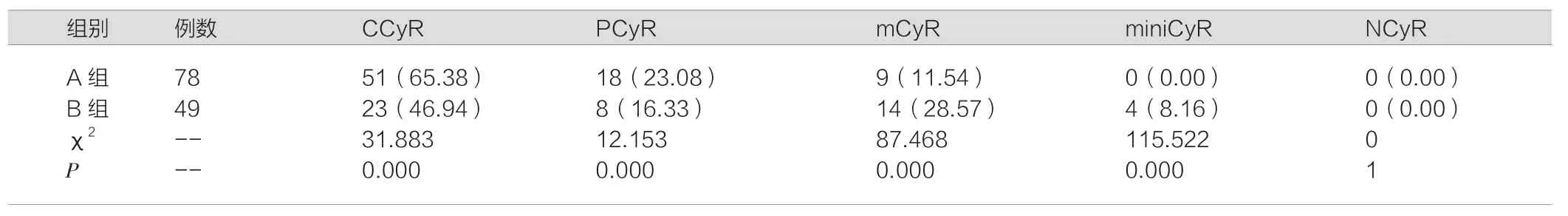
表2 两组患者治疗12个月后的细胞遗传学反应结果对比[n(%)]
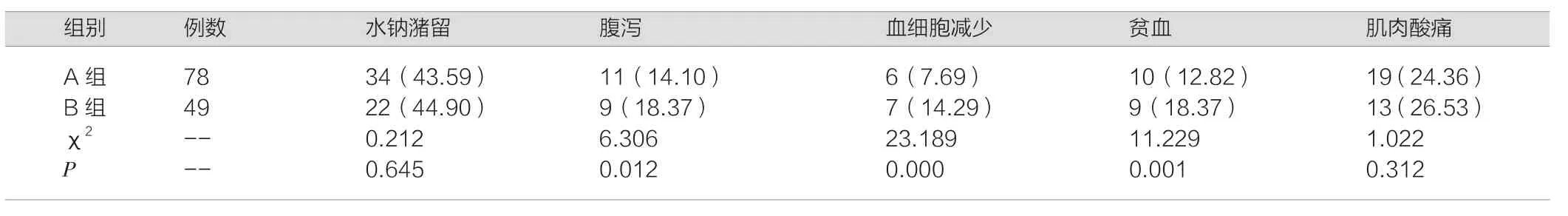
表3 两组患者的毒副作用发生情况对比[n(%)]
在临床治疗中,过去常通过口服化疗、脾区放疗、干扰素单药治疗、干扰素联合小剂量化疗、造血干细胞移植等方法治疗。有学者在1970年提出对淋巴瘤小鼠用干扰素治疗效果确切,此后干扰素在肿瘤的治疗中逐渐得到应用。在CML治疗中,干扰素是一线治疗药物,其通过与细胞膜上的受体结合而发挥作用,促进蛋白质的生成,并对某些酶产生诱导作用,抑制生长因子,减少肿瘤细胞的基因表达,抑制感染细胞中的病毒复制以及细胞增殖,起到显着的抗肿瘤效果[5]。但是,干扰素的毒副作用大,影响治疗效果。不少学者研究发现,对CML患者应用干扰素α2b治疗,其中大部分患者因耐药、无法耐受药物毒副作用而终止治疗,仅有少数患者能坚持治疗12个月。在本研究中的B组49例患者为使用干扰素α2b治疗失败而转而使用伊马替尼治疗。
BCR-ABL融合基因是一种能够编码以及表达酪氨酸蛋白激酶的基因,其能作用于细胞信号传导途径,从而促使细胞的恶性增生、细胞凋亡的减少以及骨髓基质细胞粘附性降低[6]。该融合基因蛋白中ABL的SH1结构域TK活性异常,其会与ATP结合,进而使得与ABL结合的信号传导蛋白出现磷酸反应而被激活。95% 的CML患者存在Ph1染色体的变异现象,22号染色体q11断裂点可以分成三种:M-BCR、m-BCR、u-BCR,而与ABL融合后产生的融合基因又会产生出P210、P190、P230蛋白,其中最为常见的蛋白是P210[7]。伊马替尼是一种靶向治疗CML的苯胺嘧啶衍生物,是一种高度选择性的与BCR-ABL酪氨酸激酶结合,有效阻止BCR-ABL与ATP结合,抑制蛋白酪氨酸激酶的活性[8]。有体外研究发现:伊马替尼能抑制v-abl的表达,阻止BCR-ABL细胞增殖。所以,伊马替尼的研发成功标志着慢性髓性白血病的治疗药物有了质的飞跃,使得CML开始逐渐向慢性病转化,有效延长患者的生存期[9]。有学者曾对接受伊马替尼治疗等CML患者进行回顾性分析,发现治疗12个月时累积获得的CHR率高达69%,在60个月则达到87%,预计5年生存率可达89%。由此,NCCN将伊马替尼列为慢性髓性白血病临床治疗的一线药物。在本研究中,对新诊断CML患者、重组人干扰素α2b治疗失败的CML患者均采用伊马替尼治疗,在细胞遗传学反应结果上,在治疗6个月和治疗12个月,新诊断CML的A组患者完全反应、部分反应占比均高于重组人干扰素α2b治疗失败的B组患者,P<0.05;证明重组人干扰素α2b治疗失败的CML患者应用伊马替尼治疗无法达到最佳反应效果,治疗效果较新诊断CML患者差。在临床治疗中,慢性髓性白血病患者应早期使用伊马替尼治疗,以早期获得细胞遗传学反应,尽量达到彻底反应,从而有效提高生存期,提高临床治疗效果。
在伊马替尼治疗的毒副作用上,本研究结果显示A组患者在腹泻、贫血、血细胞减少毒副作用上的发生率均低于B组,P<0.05,但是A组患者的毒副作用发生率依然较高。有学者指出对于无法耐受伊马替尼或是对伊马替尼耐药的患者可联合使用干扰素治疗,在使用伊马替尼治疗获得CCyR后应用干扰素进行维持治疗,利用干扰素改善对伊马替尼耐药以及毒副作用情况,提高治疗效果。今后临床研究还应深入讨论如何充分发挥伊马替尼的重要作用,并减少毒副作用发生率,提高患者生存率。
参考文献
[1]中华医学会血液学分会. 中国慢性髓性白血病诊断与治疗指南(2013年版)[J]. 中华血液学杂志,2013,34(5):426-432.
[2]吴圣豪,郑翠苹,徐杰,等. 伊马替尼联合干扰素-α治疗慢性髓性白血病的回顾性研究[J]. 中华血液学杂志,2012,33(4):311-315.
[3]黄晓军,胡建达,李建勇,等. 达沙替尼对中国慢性髓性白血病伊马替尼耐药或不耐受患者疗效及安全性研究[J]. 中华血液学杂志,2012,33(11):889-895.
[4]周励,王建祥,黄晓军,等. 达沙替尼与伊马替尼治疗初发慢性髓性 白血病的疗效及安全性初步比较[J]. 中华血液学杂志,2013,34(2):93-97.
[5]李梦琪,张鸣,廖爱军,等. 伊马替尼联合干扰素治疗慢性髓性白血病慢性期疗效的Meta分析[J]. 中华血液学杂志,2013,34(8):685-690.
[6]刘爱琴,苏智祥. 联合应用伊马替尼和IFN-α治疗慢性髓性白血病的临床效果观察[J].临床和实验医学杂志,2013,12(21):1763-1765.
[7]周敏,沙信山,仇惠英,等. 伊马替尼与异基因造血干细胞移植治疗慢性髓性白血病回顾性分析[J]. 中华血液学杂志,2014,35 (2):126-128.
[8]周敏,仇惠英,何广胜,等. 伊马替尼治疗慢性髓性白血病过程中发生耐药的多因素分析[J]. 中华血液学杂志,2013,34(5):395-398.
[9]董学斌,赵秀荣,陈萍,等. 伊马替尼对慢性髓性白血病患者体内激素的影响[J]. 中国综合临床,2014,30(10):1074-1076.
Analysis on Efficacy of Imatinib for New diagnostic and Treatment Failure in Human Recombinant Interferon α2b in the Treatment of Patients With Chronic Myeloid Leukemia
WANG Ping, Hematology Department, The Center of Hematology Hospital,Zhumadian He'nan, 463000, China
[Abstract]Objective To explore the value of imatinib for new diagnostic and treatment failure in human recombinant interferon α2b in the treatment of patients with chronic with leukemia. Methods 127 cases of patients with chronic myelogenous leukemia in our hospital were randomly selected as the object of this study and were divided into group A and group B, 78 patients were newly diagnosed patients, 49 patients have failed the treatment of recombinant human interferon α2b. according to the type of patients,group A was newly diagnosed group, group B was the group of treatment failure in a recombinant human interferon α2b, Two groups of patients were treated with imatinib, to compare and analyze the curative effect. Results After 6 months and 12 months of treatment, the cell genetic response rate,partial response rate of group A was higher than those of group B. In the side effect, the diarrhea, blood cell reduction and the incidence rate of anemia of group A were lower than those of B group, P>0.05. Conclusion In the clinical treatment of patients with chronic myeloid leukemia, the curative effect of imatinib for patients with the treatment failure in human recombinant interferon α2b was lower than that for patients with newly diagnosed, which was higher incidence rate of side effects. The clinical management in CML should use imatinib therapy as early as possible,and the patients of failure or resistant of treatment in human recombinant interferon α2b should use imatinib therapy as early as possible to control the condition.
[Key words]Imatinib, Chronic Myelogenous Leukemia, Human Recombinant Interferon α2b, Side Effects
【中图分类号】R552
【文献标识码】A
【文章编号】1674-9308(2016)11-0185-03
doi:10.3969/j.issn.1674-9308.2016.11.125



