何勇,裴莹莹,张彬,邵薇娜,朱云娜,冯波,刘玉新
标准化尘螨变应原制剂治疗变应性鼻炎的疗效及对血清免疫学指标的影响
何勇,裴莹莹,张彬,邵薇娜,朱云娜,冯波,刘玉新
目的 探讨标准化尘螨变应原制剂治疗变应性鼻炎(AR)的疗效及对血清免疫学指标的影响。方法 40例AR患者按照治疗方法的不同分为对照组及观察组,各20例。观察组采用标准化特异性免疫治疗,对照组采用常规对症药物治疗。记录两组治疗前及治疗12个月时的症状评分(V AS)、血清免疫学指标水平(血清总IgE、sIgE和sIgG4)。、眼结膜激发试验及不良反应情况。结果 观察组19例完成为期12个月的治疗,依从率为95%;对照组均完成12个月的治疗,依从率为100%;两组间依从率差异无统计学意义(>0.05)。两组治疗前总V AS差异无统计学意义(>0.05),治疗12个月后与治疗前均明显降低,差异均有统计学意义(均<0.05),治疗12个月后观察组总VAS明显低于对照组(<0.05)。治疗前两组患者血清免疫学指标差异均无统计学意义(≥0.29),治疗12个月后,对照组各指标水平与治疗前差异均无统计学意义(≥0.18),观察组sIgE水平较治疗前差异无统计学意义(=0.20),总IgE和sIgG4水平明显升高,差异均有统计学意义(<0.01)。两组治疗后眼结膜激发试验阳性例数相似,差异无统计学意义(>0.05),两组不良反应发生率差异无统计学意义(>0.05)。结论 标准化特异性免疫治疗AR是一种安全有效的治疗方法。
变应性鼻炎;尘螨;免疫治疗;免疫学指标
变应性鼻炎(AR)临床常见,且发病率逐年上升,70%以上患者是由尘螨引起。标准化特异性免疫治疗(SIT)是目前临床针对AR病因的“治本”方法,其可避免患者由对单一变应原过敏发展为对多种变应原过敏,由上气道疾病的变应性鼻炎发展为下气道疾病哮喘的进程。本研究拟观察SIT治疗AR的疗效及对血清免疫学指标的影响,报道如下。
1 资料与方法
1.1 一般资料 收集2013年7月至2014年12月宁波大学医学院附属医院收治的AR患者40例,均符合2009年《变应性鼻炎诊断和治疗指南》中的AR诊断标准[1]。其中男27例,女13例;年龄7~45岁,平均(21.5±11.4)岁。行皮肤过敏原点刺试验(SPT)屋尘螨均呈阳性,试验采用丹麦ALK公司提供的14种变应原液点刺皮肤,15 min后观察结果,SI值为变应原风团直径/组胺风团直径值(SI=0为阴性,SI<0.5为+,0.5≤SI<1.0为2+,1.0≤SI<2.0为3+,SI≥2.0为4+),本组患者SI值≥2+。按照治疗方法的不同将40例患者分为对照组及观察组,各20例。两组一般情况差异无统计学意义(>0.05),有可比性;观察组采用SIT治疗,对照组采用常规对症药物治疗。
1.2 治疗方法 观察组:使用丹麦ALK公司提供的SIT正规治疗,分为两个阶段:(1)起始阶段(3~4个月),每周注射屋尘螨变应原制剂(商品名:安脱达);(2)维持阶段,每6周注射1次。免疫治疗期间初期,为控制AR症状,使用糠酸莫米松喷鼻剂(内舒拿)正规剂量(12岁以上每天每侧鼻腔100 g,7~11岁每天每侧鼻腔50 g)4周+联合氯雷他定片(开瑞坦)或开瑞坦糖浆正规剂量(12岁以上或体质量大于30kg的儿童10mg,1次/d;7~12岁儿童5mg,1次/d)2周。在症状控制后药物减量,以后门诊复查根据症状程度按需给药。
对照组:使用糠酸莫米松喷鼻剂(内舒拿)正规剂量4周+联合氯雷他定片(开瑞坦)或开瑞坦糖浆正规剂量2周(使用方法同观察组)。在症状控制后药物减量,以后门诊复查根据症状程度按需给药。
1.3 观察指标 (1)记录两组治疗前及治疗12个月后的AR症状评分,采用视觉模拟量表(VAS)进行评估,针对4项主要症状鼻痒、喷嚏、鼻涕及鼻塞进行评分。(2)治疗前及治疗12个月后测定及比较两组患者血清免疫学指标水平(血清总 IgE、sIgE和sIgG4),总IgE由本院检验科检测,sIgE和sIgG4均由ALK公司-广州呼吸病研究所联合实验室提供协助,采用Bayer公司的Centaur变应原自动检测系统。(3)观察两组治疗后眼结膜激发试验阳性例数(。4)观察两组不良反应情况。不良反应可分为局部反应和全身反应,全身反应分0~4级[1]。
1.4 统计方法 数据采用SPSS18.0统计软件分析,计量资料采用均数±标准差表示,采用 检验;率的比较采用2检验。<0.05为差异有统计学意义。
2 结果
2.1 依从性分析 观察组20例患者中19例完成为期12个月的SIT治疗,依从率为95%;对照组20例患者均完成12个月的治疗,依从率为100%。两组间依从率差异无统计学意义(2=1.02,>0.05)。
2.2 总 VAS比较 观察组治疗前总VAS为(25.13±6.15)分,治疗12个月后为(13.27±2.87)分;对照组分别为(24.32 ±5.82)及(17.56±3.92)分;两组治疗前总VAS差异无统计学意义(i=0.42,>0.05),治疗12个月后与治疗前均明显降低,差异均有统计学意义(=7.82、4.31,均<0.05),治疗12个月后观察组总VAS明显低于对照组(i=3.88,<0.05)。
2.3 血清免疫学指标水平比较 治疗前两组患者各项指标差异均无统计学意义(≥0.29)。治疗12个月后,对照组各指标水平与治疗前差异均无统计学意义(≥0.18),观察组sIgE水平较治疗差异无统计学意义(=0.20),总IgE和sIgG4水平明显升高,差异均有统计学意义(<0.01)。见表1。
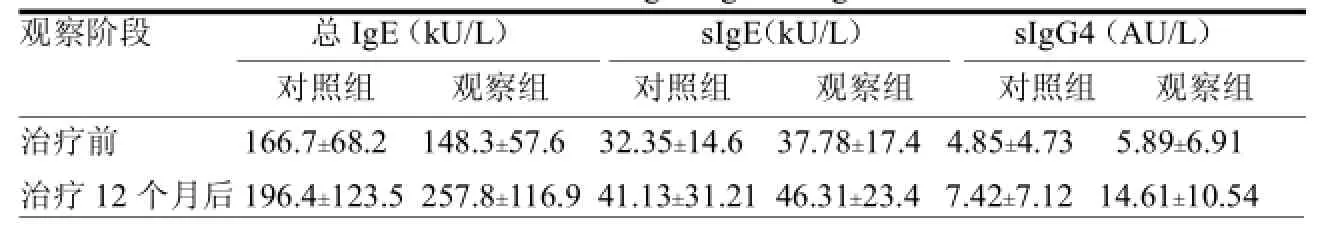
表1 两组治疗前后总IgE、sIgE和sIgG4水平比较
2.4 眼结膜激发试验及不良反应情况两组治疗后眼结膜激发试验阳性例数相似。两组患者均无2级及以上全身不良反应,对照组5例出现轻度全身不良反应,发生率为25%;观察组7例出现轻度全身不良反应,其中1例因患者自身不能坚持原因放弃治疗,不良反应发生率为35%。两组不良反应发生率差异无统计学意义(2=0.02,>0.05)。大多不良反应发生在剂量递增阶段中后期及维持治疗阶段的早期,且在对症处理后不良反应症状均得到缓解或消失,并可继续接受下一阶段的治疗。
3 讨论
临床中鼻炎患者中有超过80%的患者属于AR,在我国华东沿海地区呼吸道过敏诱发鼻炎或哮喘的患者中70%以上主要是由尘螨引起[2]。这些尘螨主要致敏原蛋白的种类是屋尘螨和粉尘螨,也就是说针对尘螨致敏原进行治疗能够解决近60%鼻炎患者的问题。目前国内外临床上常规使用的AR对症药物主要是口服抗组胺药物和鼻喷激素两类,一般使用后效果明显,但持续时间短暂,患者需要长时间持续用药以保持良好状态,但是长时间用药会产生诸多问题。譬如生活不便、医疗费用增加、产生耐药性以及长时间占用政府医疗卫生资源等,并且药物不能够有效预防AR向哮喘症状的发展及改变疾病的进程[3-4]。
SIT简称脱敏治疗,是一种原理与疫苗类似的治疗手段,以标准化的过敏原制剂持续刺激机体,使之自身产生高度耐受性,从而达到阻止症状产生和改变疾病进程的目的。标准化SIT在欧美发达地区已经开展了近30年,目前制剂和操作标准化程度最高,以及疗效最确切的是皮下注射脱敏治疗SCIT,被证明具有减轻症状、减少用药、预防哮喘、免疫调节的作用[5]。标准化SIT被引进国内已经进十年,在国内相当多的城市和地区开展,并且在项目管理和操作规范上努力与国际接轨,所以在临床上取得了很好的效果与反馈。但是目前国内外都面临着同样的一个问题:如何客观评价治疗效果?以往的经验主要以患者的主观感受作为疗效的评价。因此,建立一种由客观检测数据作为判断依据的患者治疗评价体系就显得格外必要。以往研究中多采用VAS进行症状评分,该评分是基于精神物理学和生理学研究人体对生理现象和疾病痛苦的感性指标。本研究发现两组患者治疗12个月后与治疗前比较VAS值明显降低,差异具有统计学意义(<0.01),观察组与对照组相比VAS值较低(<0.01)。
检测 sIgE能够获知患者对何种过敏原过敏、过敏的程度等级以及具体的浓度数值。sIgG4是目前实验室检测的一蛋白指标,其与sIgE竞争结合肥大细胞表面的特异性受体,从而阻止过敏反应免疫路径的传递,阻止症状的产生。SIT是对IgE介导的I型变态反应性疾病唯一的对因治疗,亦是唯一有可能达到根治的疗法[6-7]。本研究发现,在治疗12个月后,对照组各指标水平与治疗前差异均无统计学意义(≥0.18),观察组sIgE水平较治疗差异无统计学意义(=0.20),总IgE 和sIgG4水平明显升高,差异均有统计学意义(<0.01)。有研究对变应性哮喘及AR患者免疫治疗时,把SPT、眼结膜激发试验(CPT),血清sIgE、IgG1及IgG4等均纳入疗效观察指标,发现 CPT与血清SIgE、IgG1、IgG4变化水平相关。该研究提示,只要选择适当的变应原,CPT可作为支气管激发试验(BPT)较安全、可行的替代检查方法,并可较好地反映气道敏感性及气道炎症介质的变化水平,可作为SIT疗效判断的指标之一;IgG4同样是一个特异性免疫治疗的关键指标,在最新国际文献中被重点研究[8]。两组治疗后眼结膜激发试验阳性例数相似,差异无统计学意义(>0.05)。本研究中发现观察组7例发生较轻度全身反应,通过对症处理患者的不良反应均得到缓解,可继续下一疗程的治疗。
[1]中华耳鼻咽喉头颈外科杂志编委会鼻科组.变应性鼻炎诊断和治疗指南(2009年,武夷山)[J].中华耳鼻咽喉头颈外科杂志, 2009,44(12):977-978.
[2] 周洁;何源萍;曾旭东,等.屋尘螨变应原制剂治疗变应性鼻炎的临床疗效观察[J].临床耳鼻咽喉头颈外科杂志,2012,26(11):487-489.
[3] Bouousquet J,Schunemann HJ,Samolin-ski B,et al.Allergic Rhinitis and its Impact on Asthma(ARIA):Achievements in 10 years and future needs[J].Journal of Allergy and Clinical Immunology,2012, 130(5):1049-1062.
[4] Eli OM,Don AB.The economic impact of allergic rhinitis and current guidelines for treatment[J].Annals of Allergy,Asthma&Immunology,2011,106(2):12-16.
[5] Petalas K,Durham SR.Allergen immu-notherapy for allergic rhinitis[J].Rhinology,2013,51(2):99-110.
[6] Klimek L,Schendzielorz P,Mueller P,et al.Immunotherapy of allergic rhinitis: New therapeutic opportunities with viruslike particles filled with CpG motifs[J]. American Journal of Rhinology&Allergy, 2013,27(3),206-212.
[7] Lai X,Li J,Xiao X,et al.Specific IgG4 production during house dust mite immu-notherapy among age,gender and allergic disease populations[J].International Archives of Allergy and Immunology,2013, 160(1):37-46.
[8] Louisa K,James HB,Rosaleen AC,et al. Allergen specificity of IgG4-expressing B cells in patients with grass pollen allergy undergoing immunotherapy[J]Journal of Allergy and Clinical Immunology,2012, 130(3):663-670.
10.3969/j.issn.1671-0800.2016.01.053
R765.21
A
1671-0800(2016)01-0099-03
2015-11-14(本文编辑:钟美春)
宁波市科技计划社会发展项目(2012C50036)
315020宁波,宁波大学医学院附属医院(何勇、裴莹莹、张彬、邵薇娜、朱云娜、冯波);宁波大学医学院(刘玉新)
何勇,Email:nbhy195@sina.com



