解正军
(四川康西铜业有限责任公司,四川 西昌 615013)
0 前言
碘法的终点常用淀粉指示剂来确定。 在有少量I 存在下,I2与淀粉反应形成蓝色吸附包合物,根据蓝色的出现或消失来指示终点。 碘法中所用的淀粉是多糖类(C6H10O5)的一种,高等学校《有机化学实验》教材也指出:“淀粉在百万分之几时仍能给出碘试验的正性结果”。因此,在生化领域的生产和检验中,都广泛地利用淀粉和碘化钾组成的混合液作为氧化还原反应一类滴定的指示剂,或用碘来证实淀粉的存在。 但在实际分析操作中,往往会出现市售可溶性淀粉配制成的淀粉溶液在遇一定量碘时不一定显蓝色的现象。为了确保分析结果的准确性,需要我们对所用淀粉作一些对比分析,选择质量好的淀粉作为指示剂来使用。
1 实验部分
淀粉溶液的准备:5g/L
将市售A、B、C、D、E 五个不同厂家生产的可溶性淀粉分别称取0.5 克,调成糊状后分别配入已烧沸的五杯蒸馏水中,煮沸搅拌直至淀粉溶解完全,冷却稀释至100 mL 备用。
方法(一):标样法
每种淀粉溶液随机滴定两杯标样。
参照GB/T 3884.1-2012《铜精矿化学分析方法 第1 部分 铜量的测定 碘量法》,将已知铜含量为20.17%的硫化铜精矿标准样品,分别称量0.2000 克于10 个500mL 锥形烧杯中,用少量水润湿,加入10mL盐酸(ρ1.19g/mL),置于电热板上低温加热 3~5 分钟,取下稍冷,加入5mL 硝酸(ρ1.42g/mL)和 0.5~1 mL 溴,盖上表皿,混匀,低温加热;待试料完全分解后,取下稍冷,用少量水洗涤表皿,继续加热蒸至近干,冷却。 用蒸馏水30mL 冲洗表皿及杯壁,盖上表皿,置于电热板上煮沸,使可溶性盐类完全溶解,取下冷至室温。
滴加乙酸铵(300g/L)溶液至红色不再加深并过量3~5mL,然后滴加氟化氢铵饱和溶液至红色消失并过量1mL,混匀。 加入10mL(40%)片状固体碘化钾溶液摇匀,立即用硫代硫酸钠标准溶液(C=0.04mol/L,按国标方法标定好滴定度)滴定到浅黄色,加入2mL 淀粉溶液,继续滴定至浅蓝色,加入5mL 硫氰酸钾(100g/L)溶液,激烈摇振至蓝色加深。 再滴定至蓝色刚好消失即为终点。
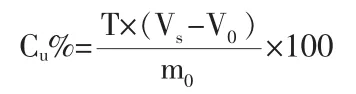
式中:T——硫代硫酸钠标准滴定溶液的滴定度,g/mL;
Vs——测定时,滴定试料溶液所消耗的硫代硫酸钠标准滴定溶液的体积,mL;
V0——测定时,滴定空白试料溶液所消耗的硫代硫酸钠标准滴定溶液的体积,mL;
m0——试料的质量,g;
方法(二):铜标准法
将纯度99.999%以上的铜片按GB/T 3884.1——2012 进行预处理,称取1.0000 克,按操作规程配制成1mg/mL 的铜标准溶液备用。
需要时, 吸取一定量铜标准溶液于洁净的烧杯中, 按GB/T 3884.1——2012 中方法2 调节酸度,加入试剂,直至加入淀粉,观察显色情况,以确定淀粉质量。
注:此方法简单、快捷,能快速辨别淀粉质量,也可对比评估淀粉影响分析结果的情况,在此略过。
2 结果与讨论
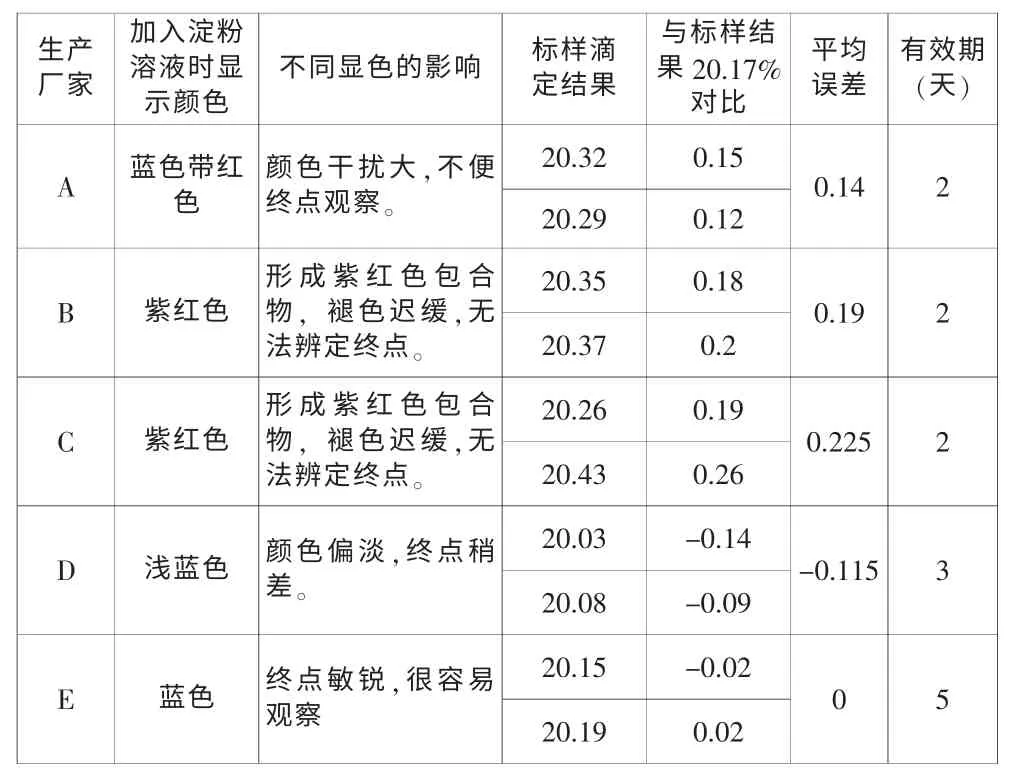
表1
就以上结果显示显浅蓝色的淀粉滴定结果略偏低,蓝带红或紫红色的容易导致结果波动,通常达0.1%以上,尤其紫红色的褪色很难观察,根本不能用来指示终点。只有显蓝色的滴定结果很稳定。在随后分析成批样品对比时也证明了此种结论。
随后几天观察所配淀粉溶液,显蓝色的最多可用近一周,但其它几种只能用2~3 天,就出现悬糊丝状物,出现腐败、变质现象,显色时明显失真。
结合所学知识并查阅相关资料显示:
淀粉是白色无定形的粉末,从结构上可分为直链和支链两种。 淀粉跟碘生成的包合物的颜色, 跟淀粉的聚合度或相对分子质量有关。在一定的聚合度或相对分子质量范围内,随聚合度或相对分子质量的增加,包合物的颜色的变化由无色、橙色、淡红、紫色到蓝色。
碘量法中应用最多的是淀粉指示剂。 通常淀粉溶液遇I2显深蓝色,反应可逆并极灵敏,在I2浓度为10-5~10-6mol/L 时亦能观察到溶液的蓝色。 含直链成份多的淀粉与I2(或I3)作用形成深蓝色,反应可逆并极灵敏,在室温条件下,可检出约10mol/L 的碘溶液;含支链成份的淀粉,只能松动地吸附I,形成一种红紫色产物,灵敏度低,不能作为碘量法的终点指示剂。
天然淀粉中含有油脂,且不同的植物,其淀粉中油脂的含量有所不同。 我们知道,油脂是有碘值的(即能与碘反应褪色),碘溶于油脂中,会使得液体呈现红至橙红色。 淀粉分子末端单糖所含有的醛基也可被碘水氧化,使碘水褪色。 (参照处理方法:可用市售的可溶性淀粉(55℃~65℃),最好是在55℃左右提取的可溶性淀粉干燥后,用CCL4在40℃~65℃下浸泡半小时,过滤,并用CCL4多次洗涤,进行脱脂处理。 将上述提取的淀粉干燥后, 用3%的H2O2浸泡二十分钟以上,过滤,并用蒸馏水反复洗涤,除去淀粉分子末端单糖的醛基。经上述处理过的淀粉,试验时可使产生的蓝色较为准确,也观察不到颜色的消褪现象,可以避免指示剂引入误差,使检验结果更准确。 )
淀粉跟碘生成的包合物在pH=4 时最稳定,所以它的显色反应在微酸性溶液里最明显,实际操作时应控制好滴定溶液的酸度,并在室温下进行操作,同时在滴定时应注意以淀粉作指示剂的加入时刻。 直接碘量法,在酸度不高的情况下,可滴定前加入;间接碘量法时,应先以硫代硫酸钠溶液滴定到溶液呈浅蓝色(此时大部分I2 已作用),然后加淀粉溶液,再用硫代硫酸钠标液滴定至蓝色恰好消失,即为终点。淀粉加入不能太早,因滴定反应中产生大量的CuI 沉淀,大量的I2 与淀粉过早形成蓝色包合物(也即淀粉凝聚,而且吸附在淀粉表面上的I2 不易释出),大量I3 被吸附,终点颜色呈较深的灰色,终点“迟纯”,不好观察。
淀粉溶液易于变质、腐败,最好临用前配制,若放置过久,则与I2形成的包合物呈紫或红色而非蓝色。这种红紫色吸附包合物在用硫代硫酸钠溶液滴定时褪色慢,终点不敏锐。
3 结论
我们在实际使用淀粉作为碘量法的指示剂时, 可参照方法一或二,及时试验对比所购淀粉质量,选择显色最好的淀粉来使用,同时严格按淀粉使用的注意事项进行现配现用,以免造成数据不稳定,引起供需双方较大的争议,甚至给企业带来重大损失。
[1]碘遇淀粉真的都显蓝色吗[OL].http://dxchong.bokee.com/5677522.html.
[2]指示剂[OL].http://class.ibucm.com/fxhx/6/right4_3.htm.
[3]中华人民共和国国家质量技术监督检验检疫总局、中国国家标准化管理委员会发布.GB/T 3884.1-2012 铜精矿化学分析方法 第1 部分 铜量的测定 碘量法[S].中华人民共和国国家标准,北京:中国标准出版社.2013,5.
[4]武汉大学,主编.分析化学[M].3 版.高等教育出版社,1995,5.
[5]胥朝,主编.分析工[M].化学工业出版社,1997,5.
[6]刘珍,编.化验员读本(上册):化学分析[M].4 版.化学工业出版社,2004,1.
[7]淀粉遇到碘变成蓝色,为什幺[OL].http://iask.sina.com.cn/b/3837660.html.



