刘明
(长春理工大学,吉林 长春 130022)
1 概述
葡萄糖作为一种常见单糖,被广泛用于食品加工中,如饮料、糖果、奶粉等制备,已成为判断食物质量是否合格的重要指标,因此。葡萄糖浓度检测对食品安全以及人类健康至关重要。在诸多检测手段中,电化学传感器因其高灵敏性、稳定性、可自动化检测等优点,得到广泛关注和研究。最早电化学葡萄糖传感器是基于酶修饰的电极作为检测原件,Clark[1]等首次提出葡萄糖酶电极并对其反应机理做出解释,指出是利用酶覆盖的氧电极通过对溶液中氧的消耗量的测定,间接达到对葡萄糖检测。虽然目前葡萄糖传感器主要是基于酶构建的传感器,对葡萄糖具有极高的专一性、选择性。但酶电极搭建成本高、酶固定技术不成熟、稳定性差并且不能长期储存使用等限制了其在实际生活中的应用。
为解决以上存在的问题,非酶葡萄糖传感器渐渐崛起,因具有出色的重复性、稳定性而备受关注,然而,要想获得高质量的葡萄糖传感器,电极材料在传感性能中起着决定性的作用。在过去电化学传感器发展的10 年里,基于贵金属(如Au、Ag、Pd)、金属合金(如Pt-Pd、Pt-Au)等饰的电极对葡萄糖具有很好的电催化性能,被广泛用作非酶葡萄糖传感器的电极材料[2-4]。但其材料价格贵、成本高、不适用于大规模使用,且易被葡萄糖反应过程中生成的中间体和氯离子毒化,使得基于贵金属构建的电极存在一些不足,例如选择性差、灵敏度低以及检测范围比较狭窄等缺点。近年来,发现相比于贵金属,过渡金属具有成本低、种类多、存储量丰富等优点,并且对葡萄糖具有很高的敏感性,是非常理想的电极材料。纳米MoS2是一种典型的过渡金属硫化物材料,单层MoS2是由共价键结合的S-Mo-S 三层组成的“三明治”层状结构,有着独特的电学、光学、物理性质,因其摩擦系数低、边缘活性强以及比表面积大,可提供足够多的活性位点,在润滑剂、催化、电池、传感器等方面有着很好的应用前景。然而,MoS2虽因具有良好的导电性、生物相容性而在生物传感方面具有极大的应用潜能,但其导电性要远远低于具有相似结构的石墨烯,为提高MoS2的导电性能,目前主要是通过与金属颗粒、石墨烯等具有超高导电性的材料复合,来使其导电性得到提高。Huang[5]等利用化学还原法将Cu 纳米粒子均匀的还原在二维MoS2纳米片上,得到Cu-MoS2复合结构并用于建立非酶葡萄糖传感器。Su[6]等通过微波辅助水热法合成出AuNPs@MoS2复合结构,并利用该复合结构建电化学传感器实现对DA 的检测。其中金纳米材料具有良好的导电性,对葡萄糖分子有着很高的电催化活性,而MoS2又是一种稳定金属纳米粒子的支持材料,所以我们选择基于Au@MoS2复合材料作为电极实现葡萄糖分子检测。
本文采用化学法成功合成出Au 纳米颗粒修饰的MoS2复合材料(Au@MoS2),利用循环伏安法(CV)和电化学交流阻抗(EIS)对所设计的电极进行电化学性能测试,并对葡萄糖进行电化学检测。
2 实验部分
2.1 材料
硫脲(CH4N2S),钼酸钠(Na2MoO4),十六烷基三甲基溴化铵(CTAB),四氯金酸(HAuCl4·H2O),氢氧化钠(NaOH),盐酸(HCl),磷酸二氢钾(KH2PO4),磷酸氢二钾(K2HPO4·3H2O),亚铁氰化钾(K4Fe(CN)6·3H2O),铁氰化钾(K3[Fe (CN)6]),N-甲基吡咯烷酮(NMP),葡萄糖(C6H12O6·H2O)等均为分析纯。
2.2 仪器
采用冷场发射扫描电子显微镜(SEM,Regulus8100)、投射电子显微镜(TEM,FEI Tecnai)对样品进行微观形貌、能谱分析,检测材料组成成分;采用X 射线衍射仪(XRD,Rigaku-D-max2550)对样品进行结构分析;采用拉曼光谱仪(Raman,LabRAM HR E)对样品进行拉曼表征分析;电化学工作站(CS350)。
2.3 Au@MoS2 复合材料的制备
先依次称量1.0gNa2MoO4、1.4gCH4N2S 倒入45mL 的去离子水中,将溶液搅拌均匀后加入0.5gCTAB,待溶液充分混匀后,用HCl 或NaOH 将溶液pH 调至弱碱性(pH 8),然后将混合后的溶液倒进反应釜中,之后放入鼓风干燥箱中进行高温反应,在240℃温度下反应48h。待反应结束,干燥箱温度降到50℃后取出反应釜放置室温待其冷却,使用去离子水、无水乙醇对溶液进行洗涤,通过离心收集样品并放进40℃的干燥箱中将其干燥,获得样品MoS2粉末。
将浓度为6.5×10-4M 的MoS2加入到沸腾的HAuCl4·3H2O 溶液中,持续搅拌至混合溶液再次沸腾,沸腾10min 后停止搅拌加热并自然冷却,之后利用胶头滴管将沉淀物取出,使用去离子水、无水乙醇对沉淀物洗涤两次,最后通过离心收集沉淀物并放进40℃的干燥箱中进行烘干,最终得到Au@MoS2样品。
2.4 电极制备及电化学测试
电极制备:将聚偏二氟乙烯、乙炔黑、石墨粉和Au@MoS2以6:10:10:74 的质量比与NMP 溶剂混合得到均匀泥浆并涂抹到泡沫Ni 上,然后放在50℃下干燥,最终得到Au@MoS2电极。通过电化学工作站进行循环伏安(CV)和交流阻抗(EIS)测试。电化学测试在电解液为含有30mMK4Fe(CN)6·3H2O 和30mMK3[Fe(CN)6]的0.1M磷酸盐缓冲液中进行,参比电极为Ag/AgCl,对电极为Pt,工作电极为Au@MoS2。
3 结果与讨论
3.1 形貌表征
利用扫描电镜、透射电镜观察研究样品的形貌特征。图1(a)显示了Au@MoS2的SEM 图,由图可知,MoS2为均匀花状结构,由多个纳米片自组装形成,尺寸约为2μm,Au 纳米颗粒附着在MoS2表面。为了能获取更多样品Au@MoS2的细节信息,利用TEM 对样品的微观结构进行观察。可以看出,平均直径为5nm 的Au 纳米颗粒被还原在MoS2花瓣表面,这表明Au 颗粒成功修饰在MoS2纳米片上。插图为Au@MoS2的EDS 图谱,从中可以看出样品Au@MoS2仅由Au、Mo、S 元素组成,无其他元素出现。

图1 Au@MoS2 复合材料的SEM 图(a)、TEM 图(b)及EDS 图谱
3.2 XRD 表征
利用X 射线衍射对样品的晶体结构、纯度进行表征,Au@MoS2的XRD 图谱如图2 所示,从图可以看出,Au@MoS2位于(002)、(111)、(110)三个晶面衍射峰的位置与MoS2的标准卡(PDF#75-1539)基本相符。而另外出现的四个衍射峰分别属于Au 的(111)、(200)、(220)、(311)晶面。整个XRD 图谱中,未有其它元素杂峰显示,说明我们所制备的样品纯度较高。

图2 Au@MoS2 复合材料的XRD 图
3.3 交流阻抗测试
为了考察Au@MoS2电极的电子传递性能,我们在测试频率为0.01Hz~100kHz 范围内,对Au@MoS2电极进行交流阻抗检测。由图3 所示,两电极的阻抗曲线均由半圆和直线组成,高频区域中的半圆对应电极反应的一个动态过程,低频区域中的直线对应扩散过程。半圆的直径表示电阻传递阻抗(Rct),直径越小表明该电极电子传递的阻力越小。实验结果显示,Au 纳米颗粒修饰的MoS2电极其Rct很小,在电极界面很容易发生电子传递过程[7]。

图3 Au@MoS2 电极的交流阻抗图谱

图4 Au@MoS2 电极的循环伏安曲线(a)及电流与v1/2 的线性拟合图(b)(5mV·s-1~25mV·s-1)
3.4 循环伏安特性
为考察扫描速率对Au@MoS2电极性能的影响,Au@MoS2电极分别在扫速为5mV·s-1、10mV·s-1、15mV·s-1、20mV·s-1、25mV·s-1下进行CV 测试,如图5(a)所示,随着扫描速率增加,峰电流强度不断增加,阴极峰的电位向负电位方向移动,阳极峰的电位向正电位方向移动。这是由于扫描速率变快会使电极界面电子传递速率加快、电催化反应加快,从而使峰电流值变大。而电位发生偏移,是由于相对较慢的扩散速度又限制了电催化反应,发生强极化作用所导致的。图5(b)所示,电流与扫速的平方根具有良好的线性关系,线性方程为:

这表明在电极表面发生的电化学反应是受扩散控制的过程,并且由回归方程的斜率可已看出,Au@MoS2适合用作生物传感器的电极制备。
3.5 葡萄糖检测
图5 为添加葡萄糖前后Au@MoS2电极在PBS 溶液中的循环伏安曲线,a 为Au@MoS2电极在电解液PBS 中的伏安曲线,b 为Au@MoS2电极在含有15mM 葡萄糖的电解液PBS 中的伏安曲线。由图可知,在同一扫速下,均出现一对几乎对称、稳定的氧化还原峰,表明该反应过程是可逆的。Au@MoS2电极a、b 曲线的阳极峰电位分别为0.76V、0.92V,阴极峰电位分别为-0.22V、-0.27V,电位差分别为0.98V、1.19V,呈递增趋势。且加入葡萄糖后Au@MoS2电极的积分面积和峰电流强度要远高于未加入葡萄糖的,这表明Au@MoS2电极对葡萄糖具有电催化活性,可以用于非酶葡萄糖传感器的构建[8]。
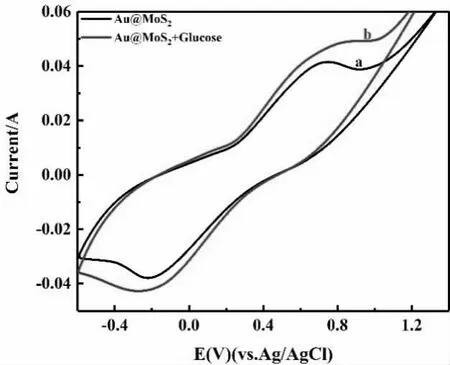
图5 未加葡萄糖的Au@MoS2 电极在电解液PBS 中的循环伏安曲线(a)和加入15mM 葡萄糖后的Au@MoS2电极在电解液PBS 中的循环伏安曲线(b)(扫速15mV·s-1)
4 结论
本文通过热还原法成功合成出Au@MoS2复合材料,经SEM、TEM 以及XRD 的表征和电化学测试显示,我们成功合成出具有高度结晶的Au@MoS2复合材料,Au@MoS2电极具有较高的导电性和较强的电催化活性,可以高效电催化氧化葡萄糖,实现快速检测。



