董秋霞 宋岩 王兴元 王玺 黄镜
中国医学科学院肿瘤医院内科,北京100021
伊立替康和奥沙利铂联合氟尿嘧啶类药物一线治疗晚期结直肠癌的临床观察
董秋霞宋岩王兴元王玺黄镜#
中国医学科学院肿瘤医院内科,北京100021
目的观察伊立替康(IRI)和奥沙利铂(OXA)联合氟尿嘧啶类药物(5-FU/替吉奥胶囊/卡培他滨)一线治疗晚期结直肠癌的疗效和不良反应。方法选取有可测量指标的晚期结直肠癌患者35例,第1天应用IRI 130~l60 mg/m2静脉滴注,同时予亚叶酸钙(CF)200 mg/m2静脉滴注后5-FU 400 mg/m2静脉推注,之后5-FU 2400 mg/m2持续泵注44 h;或替吉奥胶囊每次40~60 mg(根据体表面积确定),卡培他滨每次1000 mg/m2,早晚饭后各1次,连续服用10 d,停药4 d;第2天奥沙利铂85~100 mg/m2静脉滴注;14 d为1个周期。每3个周期评价疗效及相关毒性反应。结果全组35例可评价疗效,中位化疗为4个周期(3~11)。客观有效率(ORR)为54.3%(19/ 35),其中完全缓解(CR)1例,部分缓解(PR)18例。化疗后接受手术的25例患者中,20例患者达到R0切除(57.1%),其中18例患者系初始局部晚期,2例患者初始伴肝转移。所有35例患者在治疗期间,未出现治疗相关性死亡,3级不良反应发生率为54.3%(19/35),其中粒细胞下降发生率为20.0%(7/35),恶心发生率为17.1%(6/ 35),呕吐发生率为14.3%(5/35),腹泻发生率40.0%(14/35)。4级不良反应主要为粒细胞下降发生率,发生率为17.1%(6/35)。结论三药联合方案一线治疗晚期结直肠癌近期疗效高,毒性反应可以耐受。
结直肠癌;伊立替康;奥沙利铂;5氟尿嘧啶;替吉奥;卡培他滨;疗效
Oncol Prog,2016,14(2)
结直肠癌是常见恶性肿瘤,其发病率与病死率已分别占我国恶性肿瘤的第六位和第五位[1]。对于晚期转移性结直肠癌患者,主要的治疗手段是全身化疗。美国国立综合癌症网络指南(NCCN)推荐奥沙利铂(OXA)和/或伊立替康(IRI)联合5-氟尿嘧啶(5-FU)的方案,以是否联合靶向药物作为转移性结直肠癌一线治疗方案。但靶向药物价格昂贵,药效经济学上并不理想[2]。临床研究已经证实三药FOLFOXIRI强化治疗与传统两药方案相比,显着增加了疗效并延长患者生存,但毒性明显增加[3-8]。如何在提高疗效的前提下尽量减少不良反应成为强化治疗的关键。为进一步探索三药联合方案在临床中应用更加安全可行,回顾性分析35例经氟尿嘧啶类药物联合OXA、IRI一线治疗的晚期结直肠癌患者的疗效和不良反应,并报道如下。
1 对象与方法
1.1研究对象
选取中国医学科学院肿瘤医院肿瘤内科2013年3月至2014年10月收治的35例有可测量指标的结直肠癌患者。入选标准:经病理学证实的初治晚期结直肠癌;有可经影像学评估测量的病灶;年龄18~75岁;WHO体能状况评分≤2分;预计生存期>3个月;签署知情同意书。排除标准:骨髓造血功能异常;既往有慢性腹泻、肠道炎性疾病或肠梗阻(完全性或不完全性)史;有影响认知能力的神经或精神异常,包括肿瘤中枢神经系统转移;其他严重疾患病史,如不能控制的活动性感染、1年内心肌梗死、未控制的高血压、未控制的高危心律失常或不稳定型心绞痛;妊娠或哺乳患者,有生育能力而未采取充分避孕措施者。其中男性25例,女性10例;年龄28~72岁,中位年龄55岁。肿瘤原发于直肠的患者6例,结肠患者29例;合并肝转移11例,肺转移1例,其他部位转移5例,一个以上多脏器转移(肝、肺、骨等)2例。35例病理类型均为腺癌,其中中分化腺癌19例,低分化腺癌7例,分化程度不明确的腺癌9例。局部晚期19例,远处转移16例。(表1)
1.2治疗方法
第一天将IRI 130~160 mg/m2溶于250 ml 0.9%氯化钠溶液静脉输注90 min;同时将亚叶酸钙(CF)200 mg/m2溶于100 ml 0.9%氯化钠溶液静脉输注30 min,随后立即静脉推注5-FU 400 mg/m2,继而持续静脉泵注5-FU 2400 mg/m244 h。第二天OXA 85~100 mg/m2溶于500 ml 5%葡萄糖溶液中静脉输注2 h。或口服替吉奥胶囊(根据体表面积确定初始剂量):体表面积<1.25 m2,(按替加氟计)每次40 mg;体表面积1.25~1.50 m2,每次50 mg;体表面积>1.50 m2,每次60 mg,早晚饭后各1次,连续服用10 d,停药4 d。或口服希罗达每次1000 mg/m2,每日2次,连续服用10 d,停药4 d。治疗每两周重复一次,可手术切除的患者截至手术,无法手术的患者直至疾病进展或无法耐受化疗。
1.3疗效和不良反应评估
疗效评定根据实体瘤的客观疗效评价(RECIST 1.1)标准分为完全缓解(CR):所有目标病灶消失;部分缓解(PR):基线病灶长径总和缩小≥30%;病情进展(PD):基线病灶长径总和增加≥20%或出现新病灶;病情稳定(SD):基线病灶长径总和有缩小但未达PR或有增加但未达PD。客观有效率(ORR)为CR+PR病例占可评价病例的百分数,CR或PR患者需经4周后再证实。按毒性评估标准(NCI-CTCAE)4.0将常见不良反应分为4级。另外神经系统不良反应根据L-OHP神经系统不良反应专用分级标准分为3级:I度:短时间的感觉异常和感觉麻木;Ⅱ度:治疗周期间持续存在的感觉异常和感觉麻木;Ⅲ度:感觉异常和感觉麻木引起功能障碍。
1.4统计学方法
采用SPSS 19.0统计软件进行数据分析。计数资料采用率(%)表示。
2 结果
2.1近期疗效
全组35例患者共完成156个周期的化疗,中位化疗周期为4个(3~11)。其中延迟治疗28个周期(28/156),药物减量37个周期(37/156);延迟治疗患者9例(9/35),药物减量患者13例(13/35)。所有35例患者均可进行疗效评价。其中CR 1例,PR 18例,SD 16例,ORR 54.3%(19/35)。氟尿嘧啶组6例,其中PR 2例,SD 4例;替吉奥组15例,其中CR 1例,PR 6例,SD 8例;希罗达组14例,PR 10例,SD 4例。IRI 130~140 mg/m2剂量组10例,其中PR 7例,SD 3例;IRI 150~160 mg/m2剂量组25例,其中CR 1例,PR 10例,SD 14例;OXA 85~90 mg/m2剂量组26例,其中CR 1例,PR 13例,SD 12例;OXA 91~100 mg/m2剂量组9例,其中PR 5例,SD 4例。25例患者接受了原发灶或转移灶切除手术,R0切除患者为20例(57.1%),其中18例为初始局部晚期(17例为结肠癌,1例为直肠癌),2例为初始伴肝转移患者(2例均为结肠癌)。5例患者仅接受姑息性原发灶切除手术。

表1 35例患者基线特征比较
2.2生存状况
截至2015年12月1日,中位随访时间为19个月,无病例失访,2例死亡,与肿瘤进展有关。33例存活,其中18例R0切除患者未见肿瘤复发。患者的远期生存情况尚在随访中。
2.3不良反应
35例患者在治疗中的主要不良反应为骨髓抑制及消化道反应。最常见的血液毒性为白细胞减少、中性粒细胞减少和血小板减少;最常见的非血液毒性为乏力、恶心、呕吐、腹泻和外周神经毒性。未出现治疗相关性死亡。外周神经毒性均为轻度,Ⅰ~Ⅱ度发生率为25.7%(9/35),其他相关不良反应见表2。
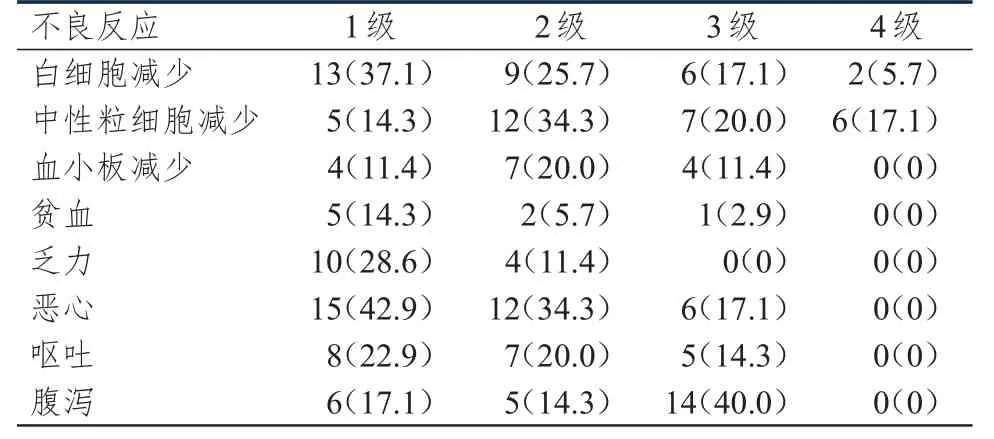
表2 FOLFOXIRI方案治疗晚期结直肠癌的不良反应[n(%)
3 讨论
随着基因检测水平及分子靶向药物研究的飞速发展,西妥昔单抗、贝伐单抗、帕尼单抗联合化疗均被NCCN指南推荐作为转移性结直肠癌的一线治疗选择[9]。本组资料显示,三药联合方案一线治疗晚期结直肠癌的ORR为54.3%(19/35),其中CR 1例,PR 18例。25例患者接受了原发灶或转移灶切除手术,20例患者达到R0切除(57.1%),其中18例为初始局部晚期,2例为初始远处转移。临床疗效显着,与国外文献报道一致。2007年GONO大型Ⅲ期随机对照临床研究,直接头对头比较了FOLFOXIRI与FOLFIRI方案在晚期转移性结直肠癌患者中的疗效,ORR:60%vs 34%(P<0.001);PFS:9.8个月vs 6.9个月(P=0.006);OS:22.6个月vs 16.7个月(P=0.032),证实三药联合相比传统两药化疗显着增加了疗效及改善了生存[8]。
2015年NCCN指南已推荐FOLFOXIRI用于进展期/转移性结直肠癌患者的一线治疗,但由于三药联合的高毒性限制了该方案的应用,指南仅推荐用于可耐受强化治疗的患者。因此如何对药物剂量进行优化,用口服氟尿嘧啶类药物替代传统5-FU是否可以提高患者的耐受性值得进一步探索。作为口服的氟尿嘧啶类药物,卡培他滨和替吉奥不但能维持较高的血药浓度并提高抗癌活性,还明显减少毒性,口服制剂还避免了因持续静脉给药产生静脉炎及中心静脉置管相关并发症。已有研究证实,口服替吉奥胶囊联合伊立替康或奥沙利铂治疗转移性结直肠癌疗效并不劣于传统FOLFIRI、FOLFOX或XELOX方案,且不良反应可以接受[10-11]。Bajetta等[12]应用卡培他滨联合伊立替康和奥沙利铂治疗转移性结直肠癌患者,ORR达到63%,化疗后手术的患者肝转移病灶R0切除率62.5%。而Vasile等[13]应用相同的三药治疗36例不可切除的转移性结直肠癌患者,ORR高达67%。笔者以卡培他滨或替吉奥胶囊代替传统5-FU,ORR为58.6%,临床疗效同样显着,这与之前的研究结果一致。
不可否认,三药联合方案很大的缺点是化疗相关不良反应,尤其3~4级不良事件均增加[3-8]。本研究最常见的血液毒性为白细胞减少、中性粒细胞减少和血小板减少;最常见的非血液毒性为乏力、恶心、呕吐、腹泻和外周神经毒性,但多为1~2级。发生外周神经毒性者,大多数为轻度,均能耐受。其中7例出现3级中性粒细胞减少(20.0%),6例出现4级中性粒细胞减少(17.1%),未出现粒细胞缺乏性发热。11例患者出现1~2级度血小板减少(31.4%),4例出现3级血小板减少(11.4%),注射白细胞介素-11后好转。14例患者在用药后出现3级腹泻(40.0%),患者经口服洛哌丁胺、补液、使用广谱抗生素及生长抑素治疗后均很快好转,未出现治疗相关性死亡事件。相对于GONO研究中患者中位年龄62岁及ECOG评分0~2分,我们选择的患者中位年龄55岁,ECOG评分0~1分,患者更年轻,体力状况更好,化疗相关耐受性更好[8]。这说明三药联合的强化方案可以成为一般状况良好患者的一线治疗选择。
另外,从用药剂量强度上看,国外报道提示三药联合方案由于化疗相关不良反应明显,导致实际剂量强度只达到目标强度的77%~91%[3-8,12-13]。随着对伊立替康毒性的深入研究表明UGT1A1*28或UGT1A1*28*6纯合突变与伊立替康不良反应具有统计学相关性[14],通过UGT1A1*28或UGT1A1* 28*6基因检测来预测伊立替康的不良反应,有助于伊立替康剂量的确定。本研究伊立替康剂量强度为130~160 mg/m2,低于国外研究,这可能也是相关不良反应发生率及疗效略低的原因。但通过伊立替康不同剂量组内的比较,适当下调化疗剂量会显着提高患者的耐受性。另外,82.58%(29/ 35)的患者口服氟尿嘧啶类药物,明显减少了静脉输注5-FU相关的并发症。
本研究再次证实了三药联合化疗在晚期转移性结直肠癌中的良好疗效并且不良反应可耐受。对于体力状况良好,伴有边界性可切除转移病灶的患者应用联合方案可明显提高R0切除率,进而转化为生存获益,所以三药联合方案应该是最优先选择之一[15]。同时我们通过口服氟尿嘧啶类药物及减少化疗药物剂量,在不影响疗效的同时降低了相关不良反应发生率,优化了给药方案,使其在临床应用中更加安全可行,值得进一步实践探索。
[1]Chen W,Zheng R,Zhang S,et al.Annual report on status of cancer in China,2010[J].Chin J Cancer Res,2014,26(1):48-58.
[2]Carter HE,Zannino D,John Simes R,et al.The cost effectiveness of bevacizumab when added to capecitabine,with or without mitomycin-C,in first-line treatment of metastatic colorectal cancer:results from the Australasian phase III MAX study[J].Eur J Cancer,2014,50(3):535-543.
[3]Masi G,Allegrini G,Cupini S,et al.First-line treatment of metastatic colorectal cancer with irinotecan,oxaliplatin and 5-fluorouracil/leucovorin(FOLFOXIRI):results of a phase II study with a simplified biweekly schedule[J].Ann Oncol,2004,15(12):1766-1772.
[4]Ychou M,Viret F,Kramar A,et al.Tritherapy with fluorouracil/leucovorin,irinotecan and oxaliplatin(FOLFIRINOX):a phase II study in colorectal cancer patients with non-resectable liver metastases[J].Cancer Chemother Pharmacol,2008,62(2):195-201.
[5]Morelli MF,Santomaggio A,Ricevuto E,et al.Triplet schedule of weekly 5-fluorouracil and alternating irinotecan or oxaliplatin in advanced colorectal cancer:a dose-finding and phase II study[J].Oncol Rep,2010,23(6):1635-1640.
[6]Köhne CH,Wils J,Lorenz M,et al.Randomized phase III study of high-dose fluorouracil given as a weekly 24-hour infusion with or without leucovorin versus bolus fluorouracil plus leucovorin in advanced colorectal cancer:European Organization of Research and Treatment of Cancer Gastrointestinal Group Study 40952[J].J Clin Oncol,2003,21(20):3721-3728.
[7]Goldberg RM,Sargent DJ,Morton RF,et al.A randomized controlled trial of fluorouracil plus leucovorin,irinotecan,and oxaliplatin combinations in patients with previously untreated metastatic colorectal cancer[J].J Clin Oncol,2004,22(1):23-30.
[8]Falcone A,Ricci S,Brunetti I,et al.Phase III trial of infusional fluorouracil,leucovorin,oxaliplatin,and irinotecan(FOLFOXIRI)compared with infusional fluorouracil,leucovorin,and irinotecan(FOLFIRI)as flrst-line treatment for metastatic colorectal cancer:the Gruppo Oncologico Nord Ovest[J].J Clin Oncol,2007,25(13):1670-1676.
[9]Bekaii-Saab T,Wu C.Seeing the forest through the trees:a systematic review of the safety and efficacy of combinationchemotherapies used in the treatment of metastatic colorectal cancer[J].Crit Rev Oncol Hematol,2014,91(1):9-34.
[10]Hong YS,Park YS,Lim HY,et al.S-1 plus oxaliplatin versus capecitabine plus oxaliplatin for first-line treatment of patients with metastatic colorectal cancer:a randomised,non-inferiority phase 3 trial[J].Lancet Oncol,2012,13(11):1125-1132.
[11]Komatsu Y,Yuki S,Sogabe S,et a1.Phase II study of combination treatment with irinotecan and S-l(IRIS)in patients with inoperable or recurrent advanced colorectal cancer(HGCSG0302)[J].Oncology,2011,80(1-2):70-75.
[12]Bajetta E,Celio L,Ferrario E,et al.Capecitabine plus oxaliplatin and irinotecan regimen every other week:a phase I/II study in first-line treatment of metastatic colorectal cancer[J].Ann Oncol,2007,18(11):1810-1816.
[13]Vasile E,Masi G,Fornaro L,et al.A multicenter phase II study of the combination of oxaliplatin,irinotecan and capecitabineinthefirst-linetreatmentofmetastaticcolorectalcancer[J].BrJCancer,2009,100(11):1720-1724.
[14]McLeod HL,Sargent DJ,Marsh S,et al.Pharmacogenetic predictors of adverse events and response to chemotherapy in metastatic colorectal cancer:results from North American Gastrointestinal Intergroup Trial N9741[J].J Clin Oncol,2010,28(20):3227-3233.
[15]Masi G,Vasile E,Loupakis F,et al.Randomized trial of two induction chemotherapy regimens in metastatic colorectal cancer:an updated analysis[J].J Natl Cancer Inst,2011,103(1):21-30.
The clinical observation of combined chemotherapy of irinotecan,oxaliplatin and fluoropyrimidines medication as first-line treatment in advanced colorectal cancer
DONG Qiu-xia SONG Yan WANG Xing-yuan WANG Xi HUANG Jing#
Department of Medical Oncology,Cancer Iinstitute and Hospital,Chinese Academy of Medical Sciences and Peking Union Medical College,Beijing 100021,China
ObjectiveTo evaluate the efficacy and safety of combined chemotherapy of irinotecan(IRI),oxaliplatin(OXA)and fluoropyrimidines(5-FU/S-1/capecitabine)as first-line treatment in advanced colorectal cancer.Method A total of 35 cases of advanced measurable colorectal cancer were enrolled,and the following regimen was administered:For day 1,IRI 130-l60 mg/m2,Ⅳ,plus leucovorin(CF)200 mg/m2,Ⅳ,followed by 5-FU 400 mg/m2Ⅳbolus,Ⅳ,then 5-FU 2400 mg/m2continuous infusion for 44 hours;or S-1 40-60 mg(based on body surface area)or capecitabine 1000 mg/m2,bid,PO,for 10 consecutive days,and then discontinue for 4 days;For day 2,oxaliplatin 85-100 mg/m2,Ⅳ,with 14 days as a cycle.The efficacy and safety were assessed every 3 cycles.ResultOf the 35 evaluable patients,the median number of chemotherapy cycles was 4(3-11).The objective response(ORR)was 54.3%(19/35).Complete response(CR)was observed in 1 case,with a partial response(PR)in 18 cases.25 patients underwent surgery,and 20 patients achieved R0 resection(57.1%),including 18 cases having local advancement and 2 cases with hepatic metastases.No treatment-related death was observed in all the 35 patients.The incidence of grade 3 adverse events was 54.3%(19/35),including neutropenia(20.0%,7/35),nausea(17.1%,6/35),vomiting(14.3%,5/35)and diarrhea(40.0%,14/35).The incidence of grade 4 adverse events was 17.1%(6/35),mainly neutropenia.ConclusionThe triple combination therapy as first-line treatment for advanced colorectal cancer was associated with good short-term efficacy and tolerable toxicity.
colorectal cancer;irinotecan;oxaliplatin;5-fluorouracil;S-1;capecitabine;efficacy
R735.3
A
10.11877/j.issn.1672-1535.2016.14.02.16
2015-12-11)
(corresponding author),邮箱:huangjingwg@163.com



