刘绪林,刘桂举
河南中医药大学第五临床医学院(郑州人民医院)1药学部,2肿瘤科,郑州 450000
胰腺癌是消化系统恶性程度较高的肿瘤,发病率不断升高,严重威胁患者的生命健康[1]。早期胰腺癌患者就可能有局部浸润及远处转移等现象,该病隐匿性较高,诊断难度较大,多数患者确诊时已经进入中晚期,病死率明显升高,因此,早发现、早治疗是降低胰腺癌患者病死率的重要基础。血清细胞迁移诱导透明质酸结合蛋白(cell migration inducing hyaluronidase 1,CEMIP)、Klotho 是临床新发现的可对胰腺癌病情进行诊断的血清因子,相关研究指出,其水平变化可反映患者的病情严重程度,是评估患者治疗效果的有效指标,但目前相关研究尚少[2-3]。胰腺癌主要采用胰头十二指肠切除术治疗,有一定疗效,但预后并不理想,需在术后辅助化疗,以提高患者的生存率,改善生活质量。替吉奥属于生物利用度较高的一种抗肿瘤药物,可在一定程度上改善手术患者的预后,但其与常见化疗药物吉西他滨联合使用治疗胰腺癌的研究较少[4]。本研究探讨吉西他滨联合替吉奥术后辅助治疗对胰腺癌患者免疫功能及血清CEMIP、Klotho 水平的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2018 年2 月至2021 年10 月河南中医药大学第五临床医学院(郑州人民医院)收治的胰腺癌患者。纳入标准:①符合《2017 美国国立综合癌症网络胰腺癌诊断与治疗指南(V1 版)更新解读》[5]中关于胰腺癌的诊断标准;②病历资料完整;③病灶直径2~5 cm;④接受胰头十二指肠切除术治疗;⑤无放化疗史。排除标准:①对治疗药物不耐受;②合并重要脏器严重疾病;③合并认知功能障碍。依据纳入和排除标准,本研究共纳入80 例胰腺癌患者,依据治疗方法的不同分为观察组和对照组,每组40 例,对照组患者给予吉西他滨治疗,观察组患者给予吉西他滨联合替吉奥治疗。观察组中,男22 例,女18 例;年龄(70.25±2.21)岁;肿瘤直径(4.12±0.59)cm;卡氏功能状态(Karnofsky performance status,KPS)评分为(66.49±4.16)分;肿瘤位置:胰头12 例,胰颈15 例,胰尾13 例。对照组中,男24 例,女16 例;年龄(70.31±2.09)岁;肿瘤直径(4.15±0.57)cm;KPS 评分为(66.79±4.25)分;肿瘤位置:胰头12 例,胰颈16 例,胰尾12 例。两组患者性别、年龄、肿瘤直径、KPS 评分、肿瘤位置比较,差异均无统计学意义(P>0.05)。本研究经医院伦理委员会批准通过,所有患者均知情同意。
1.2 治疗方法
两组患者均给予胰头十二指肠切除术治疗,并于术后第6 周开始进行辅助化疗。对照组患者给予吉西他滨治疗,注射用吉西他滨1000 mg/m2与250 ml 氯化钠注射液混合静脉滴注,每周1 次,持续治疗6 周。观察组患者给予吉西他滨联合替吉奥治疗,吉西他滨使用方法同对照组,替吉奥40~60 mg 口服,每天2 次,连续治疗2 周后停药1 周,持续治疗6 周。
1.3 观察指标和评价标准
①采用实体瘤疗效评价标准评估两组患者的临床疗效:完全缓解,肿瘤病灶基本消失,且持续时间超过1 个月;部分缓解,目标病灶直径总和与基线相比缩小≥30%,且持续时间超过1 个月;疾病稳定,目标病灶直径总和与基线相比缩小<30%或增大>20%;疾病进展,目标病灶直径总和与基线相比增大≥20%或出现新病灶。疾病控制率=(完全缓解+部分缓解+疾病稳定)例数/总例数×100%。②治疗前后,抽取两组患者外周空腹静脉血5 ml,3000 r/min 离心10 min 分离血清,离心半径16 cm,采用电化学发光法检测两组患者血清癌胚抗原(carcinoembryonic antigen,CEA)、糖类抗原125(carbohydrate antigen 125,CA125)水平,酶联免疫吸附测定检测两组患者血清CEMIP 水平;采用酶联免疫吸附测定检测仪测定450 nm 处Klotho 的光密度值,若光密度值大于阴性对照的2.1 倍,即判定为阳性。③治疗前后,采用流式细胞术检测两组患者T 淋巴细胞亚群水平,包括CD3+、CD4+、CD8+。④比较治疗期间两组患者的不良反应发生情况,包括乏力、恶心、皮疹、黏膜炎。
1.4 统计学方法
采用SPSS 22.0 软件对所有数据进行统计分析,计数资料以例数和率(%)表示,组间比较采用χ2检验;计量资料以均数±标准差(±s)表示,组间比较采用t检验;以P<0.05 为差异有统计学意义。
2 结果
2.1 临床疗效的比较
观察组患者的疾病控制率为85.00%(34/40),高于对照组患者的65.00%(26/40),差异有统计学意义(χ2=4.267,P=0.039)。(表1)

表1 两组患者的临床疗效[n(%)]
2.2 血清肿瘤标志物的比较
治疗前,两组患者CEA、CEMIP、CA125 水平和Klotho 阳性表达率比较,差异均无统计学意义(P>0.05)。治疗后,两组患者CEA、CEMIP、CA125 水平均低于本组治疗前,Klotho 阳性表达率均高于本组治疗前,且观察组患者血清CEA、CEMIP、CA125 水平均低于对照组,Klotho 阳性表达率高于对照组,差异均有统计学意义(P<0.05)。(表2)
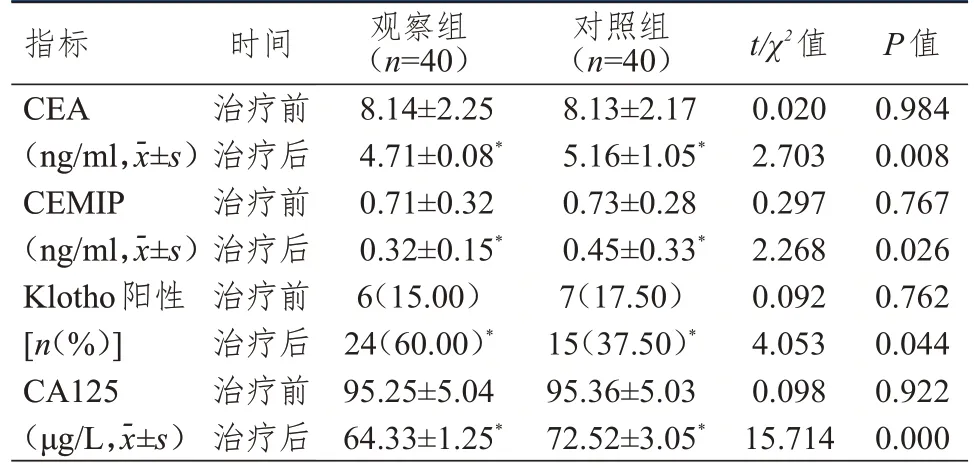
表2 治疗前后两组患者血清肿瘤标志物的比较
2.3 T 淋巴细胞亚群水平的比较
治疗前,两组患者CD3+、CD4+、CD8+水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者CD3+、CD4+水平均高于本组治疗前,CD8+水平均低于本组治疗前,且观察组患者CD3+、CD4+水平均高于对照组,CD8+水平低于对照组,差异均有统计学意义(P<0.05)。(表3)
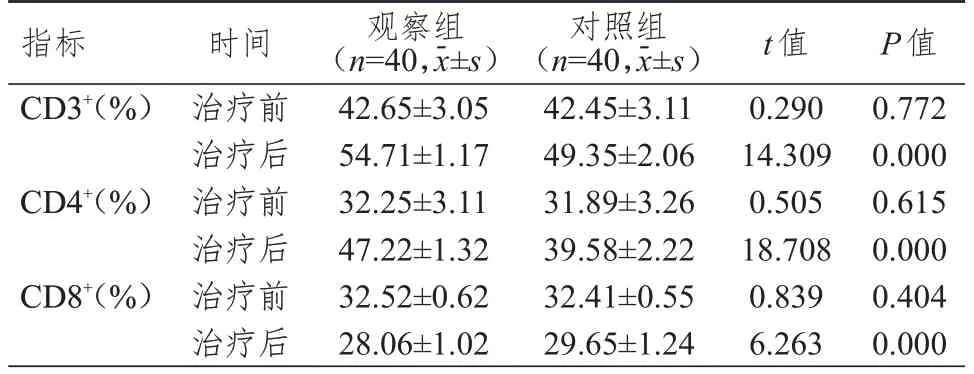
表3 治疗前后两组患者T 淋巴细胞亚群的比较
2.4 不良反应发生情况的比较
两组患者乏力、恶心、皮疹、黏膜炎发生率比较,差异均无统计学意义(P>0.05)。(表4)

表4 两组患者的不良反应发生情况[n(%)]
3 讨论
胰腺癌发病突然且进展迅速,短时间内就可出现远处转移,并发症较重,严重威胁患者的生命健康,手术切除是有效延长胰腺癌患者生存期的主要方式,其中经典术式就是胰头十二指肠切除术,但患者术后的生存率不高,且复发率较高。为改善患者的预后,需要采取术后辅助化疗提高患者的生活质量[6]。
吉西他滨作为临床二氟核苷类药物,是常见的抗肿瘤药物,可抑制肿瘤细胞增殖,促进肿瘤细胞凋亡[7-9]。替吉奥则是一种复合药物,包括奥替拉西、替加氟等,生物利用度较高,可选择性拮抗乳清酸磷酸核糖基转移酶,并可转化为5-氟尿嘧啶,发挥抗肿瘤作用[10-11]。本研究结果显示,治疗后,两组患者CD3+、CD4+水平均高于本组治疗前,CD8+水平均低于本组治疗前,且观察组患者CD3+、CD4+水平均高于对照组,CD8+水平低于对照组,差异均有统计学意义(P<0.05)。表明吉西他滨联合替吉奥可改善T 淋巴细胞亚群水平,促进患者免疫功能恢复。这可能是因为吉西他滨进入体内后会转化为活性三磷酸盐,与肿瘤细胞内脱氧胞苷三磷酸(deoxycytidine triphosphate,dCTP)进行竞争,从而进入胰腺癌内核细胞DNA 之中,导致其无法清除三磷酸盐,抑制胰腺癌细胞残缺DNA 修复,从而减少胰腺癌细胞,提高CD3+、CD4+水平,降低CD8+水平,改善T 淋巴细胞亚群水平[12-13]。替吉奥进入体内后可生成5-氟尿嘧啶,产生脱氧尿苷酸(deoxyuridine monophosphate,dUMP)等活性代谢物,与还原性叶酸反应形成三聚体,抑制胰腺癌细胞中合成酶活性,抑制肿瘤细胞DNA 合成,减少胰腺癌细胞,缓解相关症状,促使患者免疫功能恢复[14]。
本研究结果显示,治疗后,两组患者CEA、CEMIP、CA125 水平均低于本组治疗前,Klotho 阳性表达率均高于本组治疗前,且观察组患者血清CEA、CEMIP、CA125 水平均低于对照组,Klotho 阳性表达率高于对照组,差异均有统计学意义(P<0.05)。表明吉西他滨联合替吉奥可改善患者血清肿瘤标志物水平,促进患者恢复。CEA、CA125 均属于临床常见血清肿瘤标志物,CEA 为酸性糖蛋白,具有人类胚胎抗原特性,是内胚层肿瘤细胞分泌的一种结构蛋白质,经过细胞膜向周围体液分泌,并对其他细胞组织进行感染,最终使得机体内肿瘤标志物水平升高,加重胰腺癌患者病情。CEMIP、Klotho 是临床新型血清肿瘤标志物,与患者病情变化存在一定相关性[15-16]。CEMIP 是一种人体内的基因编码蛋白质,有研究发现,随着患者CEMIP 水平升高,患者的病情逐渐加重。Klotho基因编码为长单程跨膜蛋白,氨基酸共1012 个,是成纤维细胞生长因子23 及受体进行结合的重要辅助因子,可有效抑制胰岛素样生长因子-1 的表达,Klotho 表达缺失会导致肿瘤发生发展[17-18]。因此,本研究检测患者CEMIP、Klotho 表达情况,结果显示,治疗后,CEMIP 表达下调、Klotho 表达上调,可作为病情监测的指标。吉西他滨可促使肿瘤细胞出现碎片样改变,抑制肿瘤细胞代谢,促使肿瘤细胞凋亡;吉西他滨在核苷激酶的转化下可形成活性二磷酸盐,抑制肿瘤组织中还原酶活性,减少肿瘤细胞,从而改善血清肿瘤标志物水平[19-21]。替吉奥中替加氟可向5-氟尿嘧啶转化,干扰胰腺癌细胞内DNA 的结合,破坏细胞核结构,从而改善血清肿瘤标志物水平[22]。
本研究结果显示,观察组患者的疾病控制率为85.00%,高于对照组患者的65.00%,差异有统计学意义(P<0.05);两组患者乏力、恶心、皮疹、黏膜炎发生率比较,差异均无统计学意义(P>0.05)。表明吉西他滨联合替吉奥可改善患者的临床疗效,且安全性较高。
综上所述,胰腺癌患者术后给予吉西他滨联合替吉奥辅助化疗,可提高临床疗效,改善患者免疫功能和血清肿瘤标志物水平,安全性较高。



