欧明春,朱洁云,吉 攀,李红园,何翠影,张剑锋,庞杰龙△
1.广西壮族自治区百色市人民医院药学部,广西百色 533000;2.广西医科大学第二附属医院急诊科,广西南宁 530007
脓毒症是由感染引起的宿主反应失调导致的危及生命的全身炎性反应[1-3]。全球每年脓毒症患病人数超过3 000万,每年以9%~13%的速度增长,病死率为33%~35%[4-6]。脓毒症合并严重的循环和代谢功能紊乱时则发展为脓毒性休克,其病死率大于40%[1],是危重症患者的主要死因之一。脓毒性休克患者一般具有持续性心率加快与顽固性低血压的特点,心率过快可增加心肌耗氧量,且心脏舒张期缩短导致冠状动脉供血不足等,均可导致心肌受损,影响预后[7]。临床研究表明,静息心率是心脏病患者或无心脏病患者全因死亡风险的独立危险因素[8-9],因此降低心率具有重要的临床意义[10]。目前,临床上常用的降心率的药物主要为β-受体阻滞剂,且有研究表明β1-受体阻滞剂可以抑制脓毒症大鼠的心肌炎性反应,减轻脓毒症心肌损伤[11],但因β-受体阻滞剂内在的负性肌力及对血流动力学的影响,使其在脓毒性休克上的应用备受争议[12]。
艾司洛尔是一种超短效的β1-受体阻滞剂,其具有起效快、半衰期短、高选择性的特点,停药10~20 min药效即消失,在体内无蓄积,故适用于重症患者[7]。近年来国内外已有众多文献报道了艾司洛尔能够改善脓毒症或脓毒性休克患者的预后,但单个临床研究样本量较小、纳入标准和干预时间等因素不统一,且报道的结果也不完全一致。虽然近年来也有Meta分析结果表明艾司洛尔能够降低脓毒症或脓毒性休克患者的病死率,同时不影响血流动力学[13-14],但先前的 Meta分析纳入研究较少,且纳入研究的对象未限定为脓毒性休克患者。因此,本研究通过Meta分析的方法来评价艾司洛尔治疗脓毒性休克的疗效和安全性,为临床实践提供参考。
1 资料与方法
1.1纳入与排除标准
1.1.1研究类型 纳入研究的研究类型为随机对照试验(RCT)。
1.1.3干预措施 对照组给予液体复苏、营养支持、抗感染等常规脓毒性休克的治疗,或在常规治疗基础上加用安慰剂;试验组在常规治疗基础上加用艾司洛尔,疗程≥1周。
1.1.4结局指标 (1)28 d病死率;(2)心率、MAP、中心静脉压(CVP)、乳酸,由干预前和干预后的数值计算出干预前后的差值进行分析。
1.1.5排除标准 (1)非中、英文的文献;(2)同一项研究数据重复发表的文献。
1.2文献检索策略 计算机检索EMbase、中国知网(CNKI)、Cochrane图书馆、PubMed、万方数据知识服务平台和维普网(VIP)数据库从建库至2020年4月有关艾司洛尔治疗脓毒性休克的RCT。同时采用网上数据库检索和手工检索,并对纳入文献的参考文献进行二次检索。检索策略根据不同数据库特点进行调整。英文检索词:Esmolol、Septic、Septic shock;中文检索词:艾司洛尔、休克、脓毒症等。
1.3文献筛选与数据提取 由2名研究员独立进行文献筛选和数据提取并交叉核对。如有争议,则通过与第三方协调解决。资料提取内容包括(1)纳入研究的基本信息:第一作者及发表时间、样本量、年龄;(2)干预措施:药物类型、剂量、干预时间、用法;(3)结局指标:病死率、心率、MAP、CVP、乳酸等;(4)偏倚风险评价相关因素。
1.4纳入研究的偏倚风险评价 采用Cochrane5.1.0版手册推荐的RCT风险偏倚评估工具对纳入的研究进行偏倚风险评估,由2名研究者独立进行评估并对结果进行交叉核对。
1.5统计学处理 采用STATA12.0软件进行Meta分析。分类变量采用风险比(RR)为分析统计量;连续型变量采用加权均值差(WMD)为分析统计量。纳入研究结果间的异质性采用χ2检验进行分析,同时结合I2定量判断异质性大小。若各研究结果间无统计学异质性,则采用固定效应模型进行Meta分析;若各研究结果间存在统计学异质性,则采用亚组分析或敏感性分析探索异质性来源,在排除明显临床异质性后采用随机效应模型进行Meta分析。结合漏斗图和Begg检验判断是否存在发表偏倚,Meta分析的检验水准设为α=0.05,以P<0.05为差异有统计学意义。
到了画圣林白轩这里,难倒是不难,就是花时间,三人由林师父领着,一张一张去看他由世间搜罗来的历代名画,由名画中挑出他的师父吴道子的大作,之后又由之前,他课上常常演习的“画山”、“画水”、“画风”中,演绎掌法,这道题跟雨鸾的自创剑法好像,一定是他们夫妻在枕边商量好的吧!袁安拟风,创的一招掌法名叫“春风狂似虎”,李离依照“画水”走了一路“波澜掌”,上官星雨只好去想“画山”,苦思半天,也只比画出一招“看山不是山”,白轩说:“星雨你这一掌,恐怕也只能拍死一只蚊子。”星雨心里想,鸡舌香师父,你这碧水滔天、水月无间,远水近山均老矣,不改眉眼盈盈的,我就是在学您老人家的那股子黏糊劲啊!
2 结 果
2.1文献筛选流程及结果 根据检索词初步检索出相关文献381篇,经逐层筛选后,最终纳入12项RCT[7,15-25],包括1 018例脓毒性休克患者。文献筛选流程及结果见图1。

注:*各个数据库检出文献数量具体为PubMed 60篇、Cochrane图书馆27篇、EMbase 105篇、CNKI 53篇、万方数据知识服务平台70篇、VIP 66篇。
2.2纳入研究的基本特征 见表1。

表1 纳入研究的基本特征
2.3纳入研究的偏倚风险评估 纳入研究的偏倚风险评价结果详见表2。
2.4Meta分析结果
2.4.128 d病死率 共纳入8项RCT[15-22],包括700例脓毒性休克患者。各研究间无异质性(I2=0.0%),采用固定效应模型进行Meta分析,结果显示:与对照组相比,试验组的28 d病死率更低,差异具有统计学意义(RR=0.76,95%CI:0.63~0.92,P<0.001),见表3。
2.4.2心率 共纳入10项RCT[7,16-21,23-25],包括730例患者。各研究间有异质性(I2=88%),随机效应模型Meta分析结果显示:与对照组相比,试验组的心率降低幅度更显着,其差异有统计学意义(WMD=-19.67,95%CI:-25.10~-14.23),P<0.001),见表3。
2.4.3MAP 共纳入9项RCT[7,17-21,23-25],包括630例患者。固定效应模型Meta分析结果显示:与对照组相比,试验组患者的MAP更高,其差异有统计学意义(WMD=0.64,95%CI:0.10~1.18,P=0.021),见表3。
2.4.4CVP 共纳入6项RCT[17,19-21,24-25],包括393例患者。纳入研究的异质性较大(68.6%),采用随机效应模型进行Meta分析,结果显示:与对照组相比,试验组患者的CVP更低,但差异无统计学意义(WMD=-0.42,95%CI:-1.14~0.30,P=0.254),见表3。
2.4.5乳酸 共纳入5项RCT[17,18,20,24,25],包括293例脓毒性休克患者。随机效应模型(I2=58.5%)Meta分析结果显示:试验组较对照组有更低的乳酸值,差异具有统计学意义(WMD=-0.87,95%CI:-1.45~-0.30,P=0.003),见表3。
2.4.6敏感性分析 针对以不同方式治疗脓毒性休克的试验组与对照组的心率比较的Meta分析进行敏感性分析,依次剔除每项研究后重新合并统计量,结果均未发生方向性改变,提示结果较稳定。剔除刘欢等[16]和杨圣强等[25]2项研究后异质性由88%降至24%,说明此2项研究是主要的异质性来源。见图2。

图2 针对试验组与对照组治疗脓毒性休克的心率比较的Meta分析中的敏感性分析
2.5发表偏倚 试验组与对照组心率比较的Meta分析纳入研究最多,且该结果异质性较大,故针对该指标绘制漏斗图,结果显示,各研究点左右分布对称性欠佳,Begg′s检验P=0.040,提示可能存在发表偏倚。见图3。
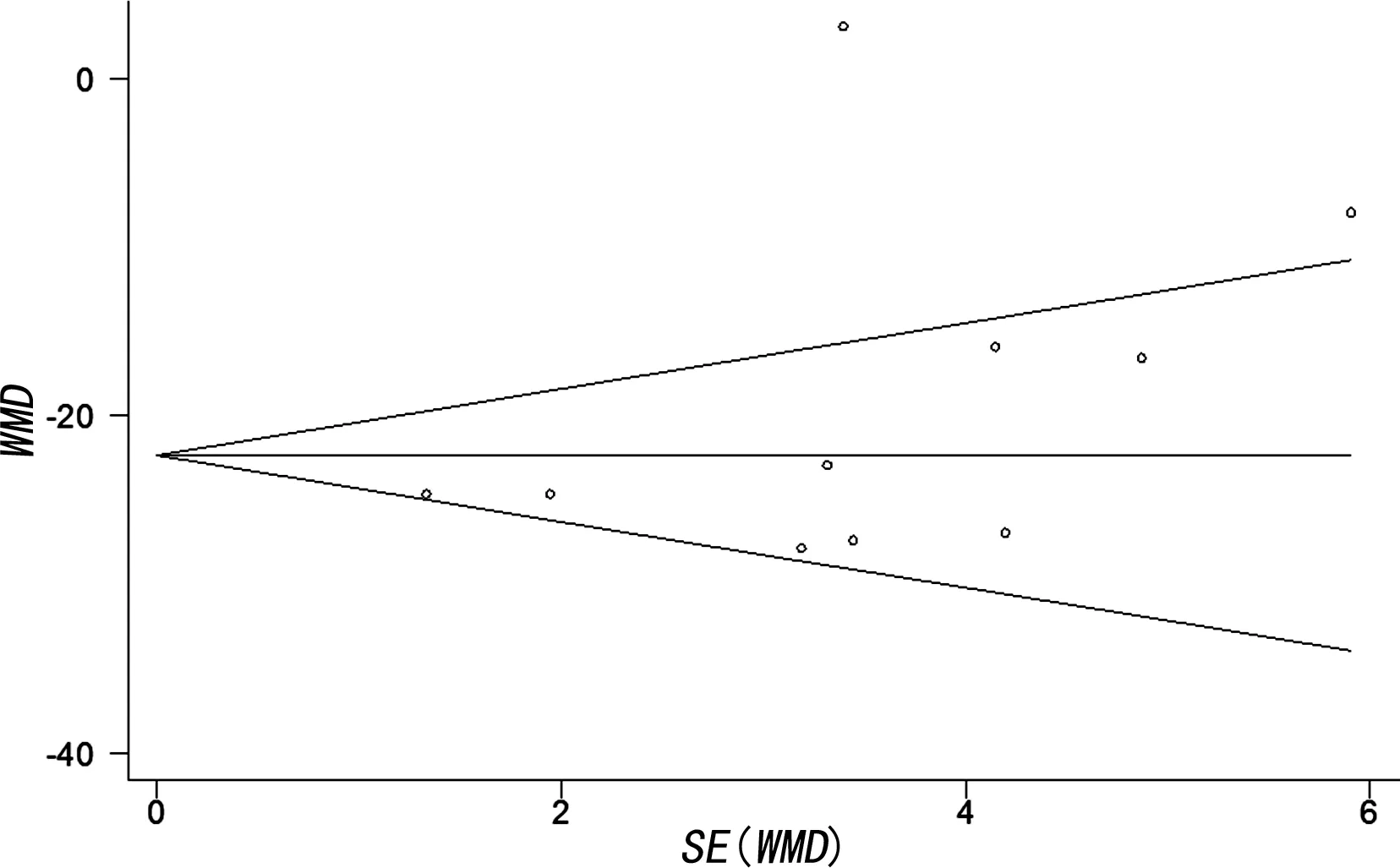
图3 针对试验组与对照组治疗脓毒性休克的心率比较的Meta分析的漏斗图
3 讨 论
脓毒症是机体感染后导致的全身炎性反应,引起患者循环和器官功能紊乱,如不及早发现并及时治疗,可导致休克、多器官功能衰竭,其中心脏受累最常见,脓毒症心肌损伤的发病率高达64%[6,26]。虽然早期液体复苏和应用血管升压药是脓毒性休克的一线治疗,但过多的液体负荷会导致毛细血管通透性增加和左心室舒张功能障碍[13];且尽管足够的液体复苏及使用升压药后,仍有20%的脓毒性休克患者循环不稳定,表现为心室率持续增加及心脏标志物水平升高,这表明可能存在脓毒症相关性心功能不全[27-28]。
脓毒症相关的心功能不全主要与长期接触儿茶酚胺和β-受体过度激活有关。脓毒症及脓毒性休克时交感神经过度激活,机体会产生并释放出大量的儿茶酚胺类激素,再加上治疗需要外源性补充β-肾上腺素的双重作用,可使机体持续心动过速,心肌氧耗增加,从而引发心肌劳损,严重者可致心肌细胞钙超载、坏死等。快速心室率也是对儿茶酚胺暴露的直接反应,心室率>95次/分可能导致冠状动脉供血不足造成心肌缺血加重心肌损伤[13]。研究表明,虽然短期β-肾上腺素刺激可增加心肌收缩力和心室率,但同时也增加心肌耗氧量,并可以直接损伤心肌细胞;长期过度刺激则可导致心肌能量供应失衡,特别是在循环系统紊乱的情况下,心肌细胞代谢被迫改变,以减少能量需求,导致“冬眠细胞”的出现,使心功能受到抑制[29-30]。
众所周知,β-受体阻滞剂可以抑制交感神经活性、减慢心率、减少心肌耗氧,也能降低慢性心力衰竭、心肌梗死等心血管疾病的病死率[31]。2013年MORELLI等[32]的研究表明,艾司洛尔可以降低脓毒性休克患者的心率,降低病死率,改善预后;2016年DU等[10]的研究也表明,艾司洛尔可使脓毒性休克患者的每搏输出量增加、降低心率,同时不影响组织灌注;2019年杨春等[17]的研究表明,艾司洛尔能够改善脓毒性休克患者的心功能,但对循环、组织灌注及病死率方面无明显影响。2017年LIU等[33]的Meta分析纳入5项RCT包括457例脓毒症或脓毒性休克患者,结果表明,艾司洛尔可以降低心率、提高生存率,对血流动力学无影响。近期的一项纳入6项RCT共363例脓毒症或脓毒性休克患者的Meta分析结果表明,艾司洛尔能够控制心室率、降低28 d病死率,同时对组织灌注无明显不良影响[13]。从上述研究结果可以得出,艾司洛尔可以降低脓毒症或脓毒性休克患者的心率,但对于循环、组织灌注及病死率方面的影响仍是有争议的。本次Meta分析纳入12项RCT,共计1 018例脓毒性休克患者,结果表明,艾司洛尔能够降低28 d病死率,降低心率,且对血流动力学无明显影响。
艾司洛尔能够降低脓毒性休克患者的病死率,改善预后的机制:艾司洛尔是一种超短效、高选择性的β1-受体阻滞剂,可以缓解机体高分解代谢状态,降低炎症因子的产生和释放从而起到抗炎的作用,有效减少患者血管内皮及心肌细胞损伤,在降低心率的同时也能减少心肌耗氧以达到保护心脏的目的[14]。同时其具有起效快、半衰期短,停药后药效消失快的特点,可根据血流动力学随时调整用药,避免引起低血压。乳酸为细胞无氧糖代谢的产物,与组织氧合有关,可反映组织灌注情况[34]。本研究结果表明,与对照组相比,艾司洛尔更能降低患者的乳酸水平,说明艾司洛尔不影响患者的组织灌注情况。有研究也表明,β1-受体阻滞剂并不增加脓毒症患者的组织氧消耗,也不影响肝脏、下肢及外周血管的血流,即可维持组织灌注[35],这与本研究结果基本一致。
本研究的局限性:(1)纳入研究的数量较少,且多数研究未描述是否使用分配隐藏和盲法等,可能存在选择性偏倚和实施偏倚;(2)本研究只纳入中、英文文献,未对其他语种及灰色文献进行检索,有可能存在语言偏倚、发表偏倚等;(3)纳入的RCT样本量较小,检验效能可能不足;(4)患者纳入标准、基础病因和干预时间并不统一,但结局指标比较分散,每个结局指标涉及的研究数较少,不能对各个结局指标均进行亚组分析和敏感性分析,未能找到全部异质性来源,这些都将影响Meta分析的准确性。
综上所述,当前证据表明,艾司洛尔能够降低脓毒性休克患者的28 d病死率,降低心率,且对血流动力学无明显影响。受纳入研究的质量和数量的影响,上述结论仍需更多高质量的研究予以证实。



