马云霞 吴雪媛
宫腔镜电切术为临床常见术式,被证实在子宫黏膜下肌瘤、子宫内膜息肉、异常子宫出血等疾病治疗中效果确切,且具有创伤小、并发症少、恢复快等特点[1-3]。但宫腔镜电切术治疗期间需应用大量灌注液,灌注液温度过低或过高均可能引发应激反应、体温波动等,导致子宫内膜血管收缩,影响术中操作,增加低体温、寒战、术后感染等并发症发生风险[4]。研究证实[5],在宫腔镜电切术治疗期间加强综合性保温护理,特别是液体保温,可减轻应激反应,预防相关并发症,促进术后恢复。但是,笔者查阅大量文献,发现临床针对宫腔镜电切术中灌注液温度选择仍存在一定争议。本次研究选取2018 年4 月—2019 年4 月92 例宫腔镜电切术患者,重点分析常规灌注液与灌注液加温(37℃)对术后恢复的影响,报道如下:
1 资料与方法
1.1 一般资料
随机抽样法选取2018 年4 月—2019 年4 月本院92 例宫腔镜电切术患者。纳入标准:(1)符合《妇产科学》[6]中相关宫腔疾病诊断标准;(2)行宫腔镜电切术治疗;(3)意识清楚;(4)知情同意。排除标准:(1)合并严重心、肝、肾脏器疾病;(2)合并严重精神疾病;(3)存在高血压、糖尿病等基础疾病。平行对照法分组:对照组(46 例)年龄25~56 岁,平均(36.71±2.15)岁;疾病类型:22 例子宫内膜息肉,13 例功能性子宫出血,11 例黏膜下肌瘤。研究组(46 例)年龄26~55 岁,平均(37.11±2.24)岁;疾病类型:21 例子宫内膜息肉,15 例功能性子宫出血,10 例黏膜下肌瘤。两组临床资料差异无统计学意义(P>0.05)。本研究通过医院伦理委员会审核批准。
1.2 方法
两组均采用宫腔镜电切术治疗,仪器为宫腔电切镜,由同一组操作医师、麻醉医师治疗,术中取膀胱截石位,灌注液为生理盐水,膨宫压力80~120 mmHg,灌注液流量240~260 mL/min。臀下端放置广口液体收集瓶,对宫颈溢出灌注液体进行收集。对照组实施常规护理,包括提供良好住院环境、完善手术准备、协助麻醉及手术医师完成相关操作、合理调节手术室温度、覆盖棉被保温、体弱者应用充气恒温毯、术后并发症早期观察和预防等,但不对灌注液采取任何处理。研究组则在对照组基础上加强灌注液温度护理,具体包括:灌注液应用前采用液体加温器加温至37℃,并置于恒温箱维持温度;应用灌注液期间加强灌注压及灌注液回收量监护;术中每隔15 min 检测1 次体温,绘制手术室体温波动图。
1.3 观察指标
(1)采用多功能检测仪连续检测患者术前(T0)、术中30 min(T1)、术毕(T2)、术后30 min(T3)时鼻咽温度。(2)比较两组手术状况,包括手术时间、术中出血量;(3)比较两组并发症,包括术中低体温(<36℃)、寒战(麻醉清醒后主诉存在寒冷症状或出现肢体颤抖)、苏醒延迟、术后感染等。
1.4 统计学方法
以SPSS 20.0 软件分析。计数资料行χ2检验。计量资料行t检验。P<0.05 为差异具有统计学意义。
2 结果
2.1 体温波动比较
T1、T2、T3 时,研究组体温高于对照组,差异有统计学意义(P<0.05)。见表1。
2.2 状况比较
两组手术时间、术中出血量对比,差异无统计学意义(P>0.05)。见表2。
2.3 并发症比较
研究组术中低体温、寒战、苏醒延迟、术后感染发生率低于对照组,差异有统计学意义(P<0.05)。见表3。
3 讨论
目前,宫腔镜电切术在妇科多种疾病诊疗中得到广泛应用,属于微创性手术,可减少手术创伤,促进术后恢复。但现今宫腔镜手术多采用非接触性内窥镜,术中需应用大量灌注液,冲洗过程中极易导致体温丢失,刺激子宫内膜血管收缩,这是诱发术中低体温的一个重要原因[7]。而围术期维持恒定体温被证实在保证手术操作顺利进行、减少并发症、促进术后康复等方面具有重要作用[8-9]。因此,临床加强宫腔镜电切术患者围术期护理,特别是术中灌注液温度监护,以预防相关并发症,促进术后恢复,具有重要意义。但既往常规护理中保温措施单一,多注重手术室温度调节、躯体棉被覆盖保温等,忽视灌注液温度调节,应用受限。
本研究在研究组患者围术期护理中加强灌注液温度护理,主要是在手术前,将灌注液经液体加温器加温至接近人体温度的37℃,并置于恒温箱维持保温,以便术中使用,还重视强化灌注压及灌注液回收量监护,加强围术期体温波动检测等。调查发现,研究组T1、T2、T3 时体温均较对照组高,差异具有统计学意义(P<0.05),说明术中灌注液加温可减少宫腔镜电切术患者围术期体温波动,有利于维持体温恒定,减轻应激反应。此外,术中低体温与较多并发症发生密切相关,如寒战、麻醉苏醒延迟、术后感染等。其中,寒战为临床常见应激反应之一,可导致肌肉痉挛或强直,增加代谢率、耗氧量,致使心率、呼吸加快,增加切口疼痛程度,且可能影响心电监测,不利于准确评估术后病情[10]。此外,患者长时间处于低体温状态,还可能影响麻醉药物代谢速度,延长麻醉苏醒时间,增加术后麻醉苏醒延迟发生风险[11]。术中低体温还可能导致出现血小板功能障碍,降低凝血功能,若不及时预防和处理,还可能降低抗感染能力,抑制免疫功能及血管收缩能力,导致药物代谢速度降低,增加术后伤口感染发生风险[12-14]。而本研究干预后,与对照组相比,研究组低体温、寒战、麻醉苏醒延迟、术后感染发生率均较低,差异具有统计学意义(P<0.05),分析是因宫腔镜电切术治疗期间,进行灌注液加温处理,可避免出现常温液体对患者体液的“冷稀释”作用,且能控制手术室低温环境对机体造成的影响,对机体总热量丢失进行弥补,有效预防低体温,降低相关并发症发生风险。此外,本次研究还发现,两组手术时间、术中出血量差异不显着。目前,临床虽提出低体温可能经由影响血小板功能、纤溶活性、凝血酶指标等,对凝血机制产生影响,但就是否可增加术中出血仍存在争议,今后仍需加大研究力度。
此外,本次研究检测患者围术期体温变化均采用鼻咽温度,与其他相关研究中肛温、耳温不同,主要是因鼻咽温度检测干扰因素少,能对机体真实温度进行反应,且接近核心温度,可提升体温波动判断准确性。
表1 两组不同时段体温变化对比(℃,)
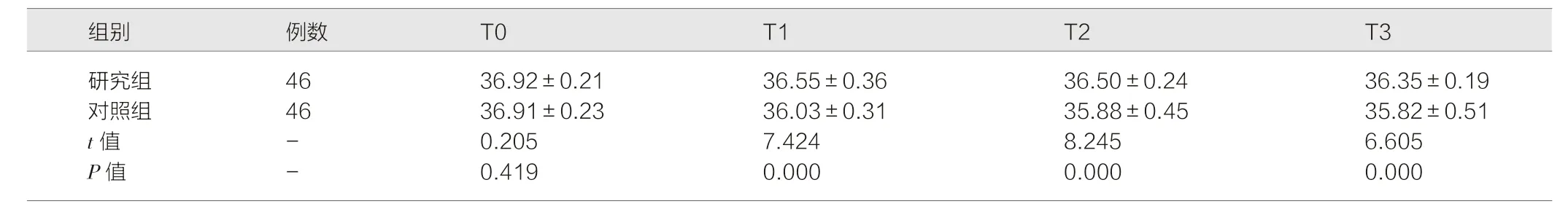
表1 两组不同时段体温变化对比(℃,)
表2 手术状况对比()
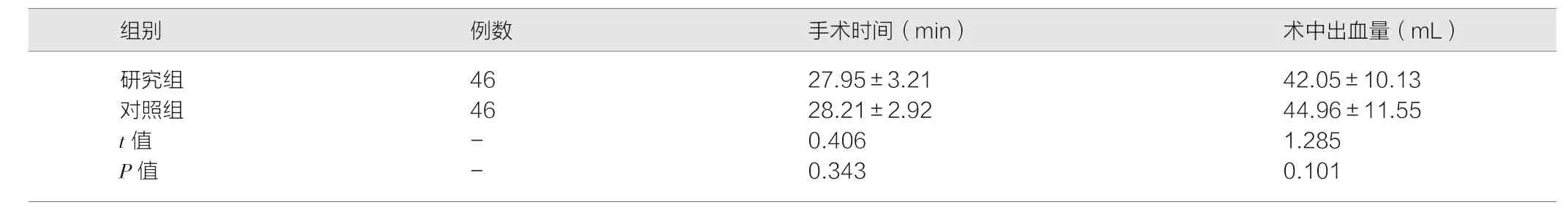
表2 手术状况对比()
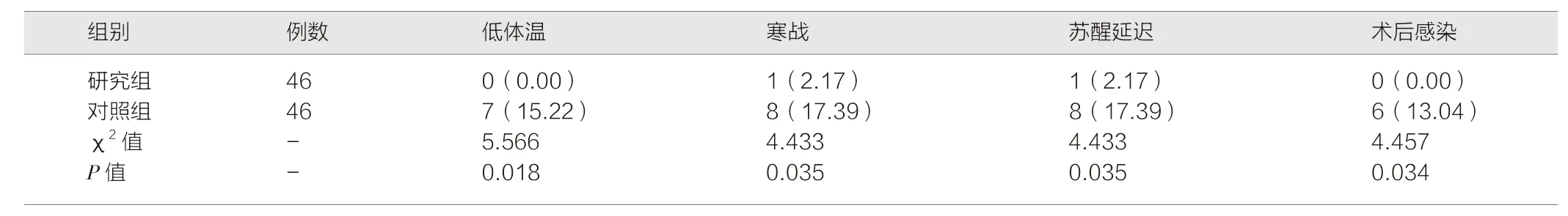
表3 两组围术期并发症发生情况对比 [例(%)]
综上所述,宫腔镜电切术中灌注液加温处理可维持体温恒定,减少低体温、寒战、麻醉苏醒延迟、术后感染等并发症发生,值得进行深入研究。



